 La pile à combustible : un générateur dénergie électrique durable?
La pile à combustible : un générateur dénergie électrique durable?
pdf. Page 51. L'avenir? Pour que la pile à combustible prenne vraiment toute sa place dans le développement durable il faudra inventer les piles de seconde.
 Les piles à combustible
Les piles à combustible
Simultanément création d'une différence de potentiel. Au cours de la réaction
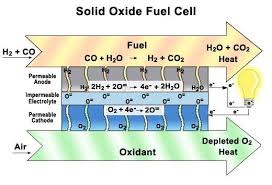 La pile à combustible
La pile à combustible
17 juin 2013 - n le nombre d'électrons échangés au cours de la réaction (ici n=2). - ΔE ... piles.pdf (valide à la date 10/04/2013). • www.adrien-girard.f ...
 UNIVERSITÉ DU QUÉBEC THÈSE PRÉSENTÉE À LUNIVERSITÉ
UNIVERSITÉ DU QUÉBEC THÈSE PRÉSENTÉE À LUNIVERSITÉ
Cette analyse nous a permis de confirmer la possibilité de démarrer la pile à combustible avec seulement sa chaleur générée au cours de son fonctionnement. En
 La pile à combustible
La pile à combustible
décentralisé fourni par les piles à combus- tible
 Chimie et conversion dénergie : piles à combustible et chaîne
Chimie et conversion dénergie : piles à combustible et chaîne
13 mai 2019 cours de part et d'autre des électrodes entre celles-ci et les électrolytes de la pile à combustible. [7]. Page 17. Germouty Julie
 Piles combustible membrane changeuse de protons
Piles combustible membrane changeuse de protons
caractéristiques électriques (tension intensité) de la pile deviennent stables au cours du temps. pdf). (11) US DOE office of trasportation (last updated ...
 Chapitre I Généralités sur les piles à combustible
Chapitre I Généralités sur les piles à combustible
- Bus : Au cours des dernières années beaucoup de bus à pile à combustible 21- [PDF] Advances in stat-portable fuel cell ..www.open- ‹ .. access.bcu.ac ...
 LHydrogène et la Pile à Combustible
LHydrogène et la Pile à Combustible
la technologie Hydrogène et Piles à Combustible ceci grâce aux financements au cours de décennies antérieures en particulier dans le domaine des composants
 Les piles à combustible
Les piles à combustible
2H2 + O2 ? 2H2O. Une PAC est un assemblage de cellules élémentaires comprenant deux électrodes (l'anode et la cathode) chargées en catalyseur (le plus souvent
 La pile à combustible : un générateur dénergie électrique durable?
La pile à combustible : un générateur dénergie électrique durable?
La pile à combustible : un générateur Différents types de piles à combustible. MCFC. Li2CO3/K2CO3 ... Evolution du cours du platine dans le temps.
 La pile à combustible
La pile à combustible
17 juin 2013 Les différents types de piles à combustibles et leur ... ?G la variation d'énergie de Gibbs ou énergie libre au cours de la réaction.
 Les piles à combustible
Les piles à combustible
Plan du cours. 1. Notions d'électrochimie. 2. Présentation générale des piles à combustible. 3. Les différents types de piles. 4. Le système pile à
 Modélisation et caractérisation de Piles A Combustible et
Modélisation et caractérisation de Piles A Combustible et
30 avr. 2013 Pile à combustible Electrolyseur
 Formations courtes sur lhydrogène-énergie
Formations courtes sur lhydrogène-énergie
22 oct. 2021 FONCTIONNEMENT DES PILES A COMBUSTIBLE. ... VEHICULES A PILE A COMBUSTIBLE. ... 6 heures de cours théoriques.
 Piles à Combustible : Techniques et avenir
Piles à Combustible : Techniques et avenir
fonctionnement de la Pile à Combustible (PAC). Les piles à combustible présentent plusieurs avan- ... qui abandonnera ce projet en cours de route.
 Etude conception et réalisation dune pile à combustible miniature
Etude conception et réalisation dune pile à combustible miniature
21 oct. 2005 1.2.3 Eléments constituant une pile `a combustible . ... Ceci doit être ajuster au cours du protocole de greffage. Pour éviter ce probl`eme ...
 La piLe à hydrogène
La piLe à hydrogène
Au cours de ce premier périple Energy. Observer était doté d'une pile à combustible conçue en collaboration avec le CEA
 AUTOBUS À PILE À COMBUSTIBLE :
AUTOBUS À PILE À COMBUSTIBLE :
Comme les projets JIVE sont en cours l'étude de cas couvre le processus d'installation des bus à pile à com- bustible
FACULTE DES SCIENCES
-le principe de fonctionnement : Dans les piles dites " acide ", l'hydrogène est oxydé à l'anode, c.-à-d. décomposé en protons et électrons. Les protons traversent ensuite l'électrolyte et se retrouvent à la cathode. Le déséquilibre en électrons crée un pôle positif et un pôle négatif entre lesquels circulent les électrons produisant ainsi de l'électricité. Simultanément à la cathode, les protons réagissent avec les électrons et l'oxygène et donnent de l'eau, seul sous-produit de cette réaction chimique.Oxydation(anode) :2H
2 4H + 4e0,00 V
Réduction(cathode) :O
2 + 4H + 4e 2H2O1,23 V
Réactionglobale :2H
2 + O 2 2H 2 O1,23 V
Rôle du catalyseur
Le principe de la pile à combustible a été démontré par l'Anglais William Grove, en 1839: le processus peut être
décrit comme l'inverse de l'électrolysede l'eau. En fait, il s'agit d'une combustion électrochimique contrôlée
d'hydrogène et d'oxygène, avec production simultanée d'électricité, d'eau et de chaleur, selon une réaction chimique
globale : 2H 2 + O 2 2H 2 OUne PAC est un assemblage de cellules élémentaires, comprenant deux électrodes(l'anode et la cathode) chargées
en catalyseur (le plus souvent du platine), séparées par un électrolyte , dont le rôle est de permettre la migration des ions d'une électrode à l'autre,sous l'effet du champ électrique créé. •L'anode(où se passe l'oxydation) est alimentée en combustible. (H 2, , CH 3OH,...)
•La cathode(où se passe la réduction) est alimentée en comburant. (O 2 , air,...)On voit donc que le combustible et le comburant n'entre pas en contact directdans la pile à combustible.
Principe de fonctionnementd'unePAC acideH
2 /O 2 .(ex : PEMFC) Pour que les deux demi-réactions soient possible, il faut un catalyseur (c.- à-d. un composé capable d'augmenter la vitesse de réaction, sans être consommé lui-même). Afin que le catalyseur puisse travailler efficacement, la création de zones activesdoit être assurée. Ces zones mettent en présence à la fois le ga z réactif, les électrons, les protons et le catalyseur, cela se réalise au niveau de l'interface électrode-électrolyte.FACULTE DES SCIENCES
Les piles à combustible
Les piles à combustible
Moteurs thermiquesMoteurs thermiques
Voie conventionnelle de production d'énergie électrique :Processus en plusieurs étapes :
•1. énergie chimique énergie thermique •2. énergie thermique travail (mécanique) •3. travail (mécanique) énergie électrique (générateur) A chaque étapede ce processus on observe des pertesénergétiques.
L'étape cruciale est la conversion de l'énergie thermique (chaleur) en travail (énergie mécanique). Le deuxième principe de la thermodynamique (S > 0) nous dit que la chaleur ne peut pas être entièrement récupérée sous une autre forme d'énergie. Le rendement théorique (maximal) est donné par l'efficacité de Carnot c c = (T s -T env )/T s < 1Piles conventionnellesPiles conventionnelles
Une réaction électrochimique s'écrit sous la forme : Ox 1 + Réd 2Réd
1 + Ox 2 Le potentiel de réaction est donné par l'équation de Nernst :A courant non-nul, les réactifs (Ox
1 et Réd 2 ) sont consommés et le potentiel diminue. Comme les réactifs (oxydant et réducteur) contenus dans la pile sont consommés, la pile doit être jetée et remplacée(batterie primaire) ou rechargée(batterie secondaire). De plus, les matériaux constituant les électrodes sont consommés. En effet, ilssontdégradésavecletempspourfinalementrendre leprocessusinactif: la la pilepileest est uséeusée. Les piles à combustibleLes piles à combustible•Définition :Une pile à combustible (PAC) est un générateur électrochimique qui permet de convertir
directementl'énergie chimique interne d'un combustible en énergie électriquesans passer par l'énergie thermique. Par conséquent, le rendement des PAC n'est pas limité par l'efficacité de Carnot. Dans les PACles réactifs sont renouvelés et les produits évacués en permanence, ce qui signifie qu'il y a production d'énergie électrique aussi longtemps que le système est alimenté en gaz réactifs (combustible et comburant). De même la structure(électrodes, électrolyte et sites réactifs) ne réagit pas et ne se dégrade pasau cours du temps. La durée de vie d'une pile à combustible est donc en théorie illimitée.FACULTE DES SCIENCES
On distingue plusieurs types de piles à combustible et on les classifie selon la nature de l'électrolyte utilisé. Celui-ci
détermine en même temps la température de fonctionnement. -AFC(AlkalineFuel Cell) -MCFC(MoltenCarbonate Fuel Cell) -SOFC(SolidOxideFuel Cell) -PAFC(PhosporicAcidFuel Cell) -PEMFC(Proton Exchange Membrane Fuel Cell) -DMFC(Direct MethanolFuel Cell) typeAFCPEMFCPAFCMCFCSOFCDMFC membraneéchangeuse de
protons (MEP)Mélange de Li2CO3
K2CO3 dans une
matrice LiAlO2MEP ou
H2SO4 charge transforméeOH-H H CO3 2- O 2- HTempérature de
fonctionnement ( 0 C)60-8080-100180-210630-650900-100070-100
H2 produit à partir
d'hydrocarbures CO2 oxydantsO2air/O2air/O2air/O2air/O2air/O2Rendement %645040607045
Santa Clara :
quotesdbs_dbs2.pdfusesText_2[PDF] cours politique monétaire pdf maroc
[PDF] cours pour devenir hacker pdf
[PDF] cours pour gps garmin
[PDF] cours pratique de maintenance informatique pdf
[PDF] cours pratique gestion commerciale
[PDF] cours préhistoire 6ème
[PDF] cours prepa physique
[PDF] cours primaire pdf
[PDF] cours principe de gestion pdf
[PDF] cours probabilité et statistique usthb
[PDF] cours probabilité pdf
[PDF] cours probabilité première s
[PDF] cours probabilité terminale s pdf
[PDF] cours probabilites et statistiques pdf

