 BREVET DE TECHNICIEN SUPÉRIEUR TRAITEMENTS DES
BREVET DE TECHNICIEN SUPÉRIEUR TRAITEMENTS DES
Expliquer pourquoi il faut impérativement se placer en milieu basique. 1.4.c standard apparent du couple (ClO– / Cl2). Démontrer la relation suivante : E ...
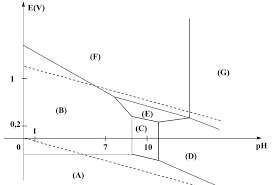 Diagrammes potentiel-pH
Diagrammes potentiel-pH
2 mai 2018 Figure 2 – Diagramme E-pH de l'étain. Exercice 3 : Corrosion du zinc. [♢♢0]. La corrosion désigne l'altération d'un ...
 «EXERCICES ET PROBLEMES CORRIGES DE
«EXERCICES ET PROBLEMES CORRIGES DE
Exercice I. C. 12. La combustion d'une mole d'éthylène dans les conditions standards suivant l'équation fournit au milieu extérieur 13878 kJ.
 Exercices sur le chapitre 2
Exercices sur le chapitre 2
14 sept. 2021 (aq) d'une eau de Javel de titre chlorométrique 90° chl est de 0
 Chimie Organique
Chimie Organique
milieu basique on a tout d'abord formation d'un enolate qui r eagit ensuite (ClO /Cl2). La premi ere partie du diagramme (pH. 4;5) a d ej a et e etudi ee ...
 V- EXERCICES :
V- EXERCICES :
1. Cette réaction d'oxydoréduction met en jeu les deux couples donnés ci-dessous. ClO-. (aq) / Cl2(
 C1 - Diagrammes potentiel-pH - TD Application directe du cours
C1 - Diagrammes potentiel-pH - TD Application directe du cours
2 ) Ecrire l'équation-bilan de la réaction en milieu acide en précisant le degré d'oxydation des espèces mises en jeu. Exercice 9 Le soufre en solution. 1 )
 Oxydoréduction
Oxydoréduction
Équilibrer les réactions suivantes en milieu acide et en milieu basique en utilisant les nombres d'oxydation. On s'intéresse aux espèces ClO– HClO(aq)
 V- EXERCICES :
V- EXERCICES :
Exercice 4 : Ecrire les demi-équations d'oxydoréduction relatives aux couples (aq) / MnO2(s) (en milieu acide) ... ClO-. (aq) / Cl2(g) et Cl2(g) / Cl-.
 BREVET DE TECHNICIEN SUPÉRIEUR TRAITEMENTS DES
BREVET DE TECHNICIEN SUPÉRIEUR TRAITEMENTS DES
L'usage de tout modèle de calculatrice avec ou sans mode examen
 Diagrammes potentiel-pH
Diagrammes potentiel-pH
2 mai 2018 On s'intéresse dans cet exercice à la corrosion du zinc. ... ClO–). Les ions chlorate ClO–. 3(aq) présents dans le milieu ne possèdent ...
 CORRIGÉ
CORRIGÉ
Exercice 1 – Etude de la déchromatation et de la décyanuration – 125 points Couple acido-basique Cr2O7 ... E° ClO-/Cl- = ½ (1
 Exercices sur le chapitre 2
Exercices sur le chapitre 2
L'eau de Javel est une solution aqueuse contenant des ions hypochlorite C?O?. (aq). Son efficacité dépend de la concentration de ces ions qui présentent
 Cours et exercices de chimie des solutions
Cours et exercices de chimie des solutions
Cours destiné aux étudiants de deuxième année des Classes Pour ClO. -. : = 1 ? CN = CM. Pour Cl2: = 2 ? CN = 2×CM ... 8 milieu basique !!!
 C1 - Diagrammes potentiel-pH - TD Application directe du cours
C1 - Diagrammes potentiel-pH - TD Application directe du cours
en milieu basique pour un pH compris entre 8 et Exercice 10 Diagramme du chlore et eau de Javel ... le potentiel standard E0 du couple Cl2(g)/Cl-.
 Oxydoréduction Oxydoréduction
Oxydoréduction Oxydoréduction
et Cr3+ forment un couple redox. Identifier l'oxydant et le réducteur. Écrire ensuite la demi-équation associée en milieu acide et en milieu basique.
 COURS DE CHIMIE Avec EXERCICES
COURS DE CHIMIE Avec EXERCICES
chapitre aux questions des exercices d'auto-évaluation. 3- Effets électroniques et propriétés acido-basiques des composés organiques .
 CORRIGE
CORRIGE
21 jui. 2018 Dans chaque exercice ou problème il y a des parties indépendantes (notamment dans le sujte de chimie organique).
Oxydoréduction
Sauf précision contraire, la température est de 25 ◦C, ce qui permet d"approximerRTF ln10 = 0,059V.ExercicesExercice 1 :
Équations bilan d"o xydoréduction[ ]
On s"intéresse aux couples MnO
-4/Mn2+, HClO(aq)/Cl2(g)et Cl2(g)/Cl-. On rappelle que MnO-4est l"ion perman- ganate et HClO est l"acide hypochloreux.1 -Écrire et équilibrer les demi-équations de chacun des couples en milieu acide.
2 -Lorsque la réaction est possible, écrire l"équation bilan de la réaction entre
?l"acide hypochloreux et l"ion manganèse; ?l"ion manganèse et l"ion chlorure; ?l"ion manganèse et le dichlore;?le permanganate et le dichlore; ?le permanganate et l"ion chlorure; ?le dichlore sur lui-même.Exercice 2 :
Nomb resd"o xydationdu chrome [ ]
Le chrome Cr a pour numéro atomiqueZ= 24, et il est moins électronégatif que l"oxygène.1 -Donner lenodu chrome au sein des espèces Cr(s), Cr2+et Cr3+.
2 -Sans représenter de schéma de Lewis, déterminer lenodu chrome dans les espèces CrO2-4et Cr2O2-7. On précise
qu"il n"y a pas de liaison Cr-Cr dans le dichromate.3 -Justifier que Cr2O2-7et Cr3+forment un couple redox. Identifier l"oxydant et le réducteur. Écrireensuitela
demi-équation associée, en milieu acide et en milieu basique.4 -Justifier que CrO2-4et Cr2O2-7ne forment pas un couple redox. Montrer qu"il s"agit d"un couple acide-base par
écriture d"une demi-équation.
Exercice 3 :
Nomb resd"o xydationdu soufre [ ]
Le soufre S est situé juste en dessous de l"oxygène dans le tableau périodique.1 -Déterminer sans construire de schéma de Lewis lenodu soufre dans les espèces chimiques SO2, SO2-4et SO3.
2 -Calculer par la même méthode lenodu soufre dans les espèces S2O2-3et S4O2-6.
3 -Écrire la formule de Lewis de S2O2-3et S4O2-6. Un atome de soufre est central dans l"ion thiosulfateS2O2-3, et l"ion
tétrathionate S4O2-6présente une liaison simple O-O.
4 -Que peut-on conclure de ces représentations à propos dunodu soufre? D"où vient le "problème»? Que représente
lenocalculé à la question 2?Exercice 4 :
Di smutationdu dio xyded"azote [ ]
En présence d"eau, le dioxyde d"azote NO
2(g)peut se dismuter en ions nitrates NO-
3(aq)et nitrites NO-
2(aq). Cette
réaction produit des protons H +, à l"origine des pluies acides.1 -Écrire les demi-équations de transfert électronique et la relation de Nernst pour les deux couples NO-
3(aq)/NO2(g)
(potentiel standardE◦1= 0,83V) et NO2(g)/NO-2(aq)(potentiel standardE◦2= 0,85V).
2 -Justifier à l"aide de diagrammes de prédominance que NO2se dismute. On choisirapNO2= 1baret une concen-
tration frontière 1mol·L-1à pH nul.3 -Écrire l"équation bilan de l"équation de dismutation.
4 -Exprimer sa constante d"équilibreK◦en fonction des potentiels standard et calculer sa valeur numérique.
1/4Étienne Thibierge, 2 mai 2018,www.etienne-thibierge.fr
TD TC5 : Oxydoréduction Langevin-Wallon, PTSI 2017-2018Exercice 5 :
Éthylotest [ ]Peu après avoir été consommé, l"alcool (éthanol de formule CH3CH2OH) passe dans le
sang au niveau de l"intestin grêle. Ensuite, des échanges gazeux s"effectuent dans les alvéoles
pulmonaires : le sang se charge en dioxygène et se libère du dioxyde de carbone ainsi que d"une
partie de l"alcool. Ces vapeurs sont expirées dans l"air avec une concentration en alcool 2100fois inférieure à celle du sang. Le seuil limite autorisé pour la conduite est de 0,50g d"éthanol
par litre de sang. Les alcootests jetables sont constitués d"un sachet gonflable de capacité 1L et d"un tube en verre contenant des cristaux orangés de dichromate de potassium K2Cr2O7en milieu acide.
Ceux-ci se colorent en vert au contact de l"alcool.Données :
?Potentiels standard : couple Cr2O2-7/Cr3+E◦1= 1,33V; couple CH3COOH/CH3CH2OHE◦2= 0,19V; ?Masses molaires atomiques :MH= 1g·mol-1;MC= 12g·mol-1;MO= 16g·mol-1;MK= 39g·mol-1; MCr= 52g·mol-1.
1 -Écrire l"équation de la transformation responsable du changement de couleur. Identifier l"espèce oxydée et l"espèce
réduite.2 -Calculer la constante d"équilibre de la réaction. Commenter.
3 -Déterminer la quantité de matière d"alcool expirée par litre d"air dans l"hypothèse d"une alcoolémie atteignant le
seuil de 0,50g d"alcool par litre de sang.4 -En déduire la masse de dichromate de potassium devant être placée avant le trait de jauge afin que celui-ci indique
le seuil limite.Exercice 6 :
Pi lea rgent-zinc[ ]
On s"intéresse à la pile schématisée parAg(s)|Ag+(c)?Zn2+(c?)|Zn(s)avecc= 0,18mol·L-1etc?= 0,30mol·L-1.
Le compartiment de gauche a un volumeV= 100mL, celui de droite un volumeV?= 250mL. Données :E◦(Zn2+/Zn) =-0,76VetE◦(Ag+/Ag) = +0,80V1 -Déterminer la f.é.m. de la pile. Identifier alors l"anode et la cathode.
2 -Écrire les réactions électrochimiques aux électrodes puis la réaction de fonctionnement qui se produit lorsque la
pile débite.3 -Schématiser le déplacement des porteurs de charge dans chaque partie de la pile lorsqu"elle débite du courant.
4 -Déterminer la composition de la pile lorsqu"elle est usée. Quelle quantité d"électricité, en coulombs, a-t-elle
débité?Exercice 7 :
Stabili sationdu cuivre (I) pa rp récipitation[ ]L"objectif de cet exercice est d"étudier la stabilisation du cuivre auno+I par précipitation, qui illustre plus
généralement l"influence de la précipitation sur l"oxydoréduction. Données :potentiels standards des couples Cu+/CuE◦1= 0,52Vet Cu2+/Cu+:E◦2= 0,16V.1 -Montrer à partir de diagrammes de stabilité que l"ion Cu+est instable. Pour simplifier, on prendra 1mol·L-1
comme concentration frontière. Qu"observe-t-on? Les ions cuivre (I) forment avec les ions iodure I -le précipité CuI(s), de produit de solubilitéKs= 10-11.2 -Écrire l"équation de dissolution du précipité, puis écrire les demi-équations redox pour les couples CuI/Cu et
Cu2+/CuI.
3 -En déduire la relation de Nernst pour les couples CuI/Cu et Cu2+/CuI en notant leurs potentiels standardsE◦3etE◦4. Exprimer alorsE◦3en fonction de pKsetE◦1, et de mêmeE◦4en fonction de pKsetE◦2. Calculer les valeurs
numériques.4 -Expliquer en quoi les ions cuivre (I) sont stabilisés en présence d"iodure.
2/4Étienne Thibierge, 2 mai 2018,www.etienne-thibierge.fr
TD TC5 : Oxydoréduction Langevin-Wallon, PTSI 2017-2018Exercice 8 :
Dosage colo rimétriqueen retour [ ]
On s"intéresse à un dosage colorimétrique d"une solution de dichromate de potassium par les ions fer (II) dans en
milieu sulfurique garantissant un pH très acide. On donne les potentiels standard E ◦1=E◦(Cr2O72-/Cr3+) = 1,33VetE◦2=E◦(Fe3+/Fe2+) = 0,77V. En milieu acide, l"ion dichromate est orange et l"ion chrome (III) est vert, alors que l"ion Fe2+est vert pâle et l"ion
Fe3+est jaune-orangé.
1 -Écrire l"équation bilan du titrage redox direct.
2 -Calculer sa constante d"équilibre. Cette réaction est-elle adaptée à un titrage? Pourquoi est-elle malgré tout peu
adaptée à un titrage colorimétrique?3 -Justifier qu"il serait possible de suivre la réaction par potentiométrie. Déterminer le sens du saut de potentiel qui
serait observé : est-il descendant ou montant?Pour contourner la difficulté sans montage de potentiométrie, on effectue un dosage en retour. Dans un bécher,
on verseV1= 4,0mLde la solution de dichromate de potassium dont on cherche la concentrationC1. On y ajoute
V2= 10,0mLd"une solution de sulfate de fer (II) en milieu sulfurique de concentrationC2= 0,10mol·L-1et
90,0mL d"eau. On verse ensuite par une burette une solution de permanganate de potassium de concentration
C3= 1,0·10-2mol·L-1. Une coloration violette, caractéristique du permanganate en solution, apparaît lorsque
V3E= 12mLont été versés.
4 -Comment peut-on s"assurer qualitativement que les ions fer (II) ont bien été apportés en excès par rapport au
dichromate?5 -Écrire l"équation bilan du titrage en retour.
6 -Déterminer la concentrationC1de la solution de dichromate de potassium.Annale de concours
Exercice 9 :
Pile à combustible à o xydesolide [écrit PT 2015, ]Le principe de la pile à combustible consiste à utiliser du dihydrogène pour stocker et transporter de l"énergie.
Une pile à combustible est un assemblage de cellules élémentaires, en nombre suffisant pour assurer la production
électrochimique d"électricité dans les conditions de tension et d"intensité voulues. De façon générale, le fonctionnement
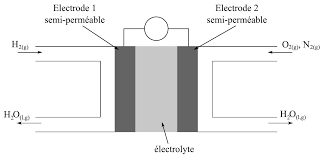
électrochimique d"une cellule élémentaire de pile à combustible peut être représenté selon le schéma figure 1.Figure 1-Schéma de principe d"une pile à combustible.
Chaque cellule élémentaire est constituée de deux compartiments disjoints alimentés chacun en gaz dihydrogène
et dioxygène. Les électrodes sont séparées par un électrolyte solide qui laisse passer les anions oxygène. Les couples
d"oxydoréduction mis en jeu dans la réaction sont H (aq)/H2(g)et O2(g)/H2O(liq).1 -Indiquer les configurations électroniques fondamentales des atomes constitutifs des réactifs et du produit. En
déduire les schémas de Lewis des trois molécules.2 -À partir des informations du schéma, attribuer et justifier le choix de la cathode et de l"anode aux électrodes 1
et 2, ainsi que le sens de circulation des électrons.3 -Écrire les demi-équations électroniques pour chaque couple mis en jeu, quand la pile débite.
4 -Le réactif qui est oxydé est appelé le combustible de la pile. Parmi les espèces chimiques présentes dans les
3/4Étienne Thibierge, 2 mai 2018,www.etienne-thibierge.fr
TD TC5 : Oxydoréduction Langevin-Wallon, PTSI 2017-2018 couples, laquelle constitue le combustible?5 -En déduire l"équation de la réaction modélisant la transformation ayant lieu dans la cellule de réaction.
Dans un véhicule motorisé fonctionnant grâce à une pile à combustible, on estime à 1,5kg la masse de dihydrogène
nécessaire pour parcourir 250km.6 -Calculer la quantité de matière de dihydrogène correspondant à cette masse, puis le volume occupé par cette
quantité de gaz à 20 ◦C sous pression atmosphérique.7 -Quel est l"avantage pour l"environnement de l"utilisation d"une pile à combustible au dihydrogène par rapport à
un carburant classique? Quel en est l"inconvénient majeur?Exercice 10 :
A ccumulateurlithium métal [o ralbanque PT, ]
On étudie ici l"accumulateur lithium-oxyde de manganèse, qui représente environ 80% du marché des batteries au
lithium. La première électrode est en dixoyde de manganèse MnO2, la deuxième en lithium Li. Ces deux électrodes
baignent dans un électrolyte organique contenant des ions LiDonnées :
?Numéro atomique du lithium :Z= 3; ?Masse molaire du lithium :M= 5,9g·mol-1; ?Potentiels standard :E◦1(Li+/Li(s)) =-3,03VetE◦2(MnO2(s)/LiMnO2(s)) = 0,65V.1 -Donner la configuration électronique du lithium. Indiquer sa position dans le tableau périodique. Pourquoi choisir
un électrolyte organique plutôt que de l"eau?2 -Écrire les réactions aux électrodes lorsque l"accumulateur fonctionne en générateur, ainsi que la réaction globale
de fonctionnement.3 -La pile contient elle un pont salin ou équivalent? Pourquoi?
4 -Déterminer la force électromotrice de la pile.
5 -Déterminer la capacitéCde la pile en A·h pour une masse initiale de 2g de lithium.
Exercice 11 :
Dosage d"une solution d" hypochloritede so dium[écri tPT 2016, ]Après avoir introduit un volumeV0= 2,00mLd"une solution commerciale d"hypochlorite de sodium (Na++ClO-)
dans une fiole jaugée de volumeVf= 100mL, on complète avec de l"eau distillée jusqu"au trait de jauge. À un
volumeV= 10,0mLde cette solution fille, on ajoute environ 10mL d"une solution d"iodure de potassium (K++I-)
à 15% en masse et 5,0mL d"acide éthanoïque CH3CO2H(aq)à 3,0mol·L-1. L"échantillon obtenu est titré par une
solution de thiosulfate de sodium (2Na++ S2O2-3) de concentrationC= 2,0·10-2mol·L-1. Le volume équivalent
est égal àV?= 16,0mL.Données :potentiels standards à 298K
E ◦(ClO-/Cl-) = 0,89VE◦(I2/I-) = 0,54VE◦(S4O2-6/S2O2-3) = 0,08V1 -Proposer une équation pour la réaction entre les ions hypochlorite ClO-et les ions iodure I-. Prévoir qualitati-
vement le caractère favorisé ou défavorisé de la réaction.2 -Proposer une équation pour la réaction de titrage du diiode I2par les ions thiosulfate S2O2-3. Prévoir qualitati-
vement le caractère favorisé ou défavorisé de la réaction.3 -Sachant que les ions iodure et l"acide éthanoïque sont introduits en excès, déterminer la concentration en ions
hypochlorite dans la solution commerciale.4/4Étienne Thibierge, 2 mai 2018,www.etienne-thibierge.fr
Transformations chimiques 5 - Correction des travaux dirigésLangevin-Wallon, PTSI 2017-2018OxydoréductionTransformations chimiques 5 - Correction des travaux dirigésLangevin-Wallon, PTSI 2017-2018
Oxydoréduction
Exercices
Exercice 1 :
Équations bilan d"o xydoréduction
1MnO -4+ 8H++ 5e-= Mn2++ 4H2O2HClO + 2H
++ 2e-= Cl2+ 2H2O Cl2+ 2e-= 2Cl-
2?Pas de difficulté :
10HClO + 2Mn
2+= 5Cl2+ 2H2O + 2MnO-4+ 6H+
?Pas de réaction entre Mn2+et Cl-car ce sont deux réducteurs. ?Comme Mn2+est un réducteur, Cl2intervient forcément en tant qu"oxydant : 2Mn2++ 8H2O + 5Cl2= 2MnO-4+ 16H++ 10Cl-
?Comme MnO-4est un oxydant, Cl2intervient forcément en tant que réducteur : 2MnO -4+ 6H++ 5Cl2+ 2H2O = 2Mn2++ 10HClO ?Pas de difficulté : 2MnO -4+ 16H++ 10Cl-= 2Mn2++ 8H2O + 5Cl2 ?Le dichlore intervient en tant qu"oxydant et réducteur (dismutation) : Cl2+ H2O = Cl-+ HClO + H+
Exercice 2 :
quotesdbs_dbs4.pdfusesText_8[PDF] Clonage 3ème SVT
[PDF] clonage de dolly + svt 3ème PDF Cours,Exercices ,Examens
[PDF] clonage génétique PDF Cours,Exercices ,Examens
[PDF] clonage svt 3eme PDF Cours,Exercices ,Examens
[PDF] cloner une machine virtuelle vmware PDF Cours,Exercices ,Examens
[PDF] closer PDF Cours,Exercices ,Examens
[PDF] closermag PDF Cours,Exercices ,Examens
[PDF] clostermann jacques PDF Cours,Exercices ,Examens
[PDF] clostermann pierre PDF Cours,Exercices ,Examens
[PDF] Clothes 6ème Anglais
[PDF] clothoide route PDF Cours,Exercices ,Examens
[PDF] clothoide route pdf PDF Cours,Exercices ,Examens
[PDF] cloture 3ème Mathématiques
[PDF] Clôture en triangle 6ème Mathématiques