 FACULTE DE CHIMIE DEPARTEMENT DE CHIMIE ORGANIQUE
FACULTE DE CHIMIE DEPARTEMENT DE CHIMIE ORGANIQUE
Pour cette raison on fait précéder le cours de thermodynamique chimique par Première équation de Maxwell. Soit l'équation principale de la thermodynamique :.
 «EXERCICES ET PROBLEMES CORRIGES DE
«EXERCICES ET PROBLEMES CORRIGES DE
de thermodynamique chimique» vise à mettre à la disposition des étudiants de première année des facultés des sciences un outil qui leur permettra d'acquérir.
 Faculté des Sciences Meknès Cours THERMOCIMIE-EQUILIBRES
Faculté des Sciences Meknès Cours THERMOCIMIE-EQUILIBRES
DEPARTEMENT DE CHIMIE. FILIERE SVTU/S1. MODULE CHIMIE GENERALE. COURS. THERMOCHIMIE/EQUILIBRES CHIMIQUES. Réalisé par : Pr. Hamid MAGHAT. ANNEE UNIVERSITAIRE :
 Introduction à la thermodynamique chimique
Introduction à la thermodynamique chimique
Energie interne et enthalpie. 1. Conservation de l'énergie. L'énergie totale d'un système isolé se conserve au cours de ses
 Cours-de-Thermodynamique-Chimique-2020-L2.pdf
Cours-de-Thermodynamique-Chimique-2020-L2.pdf
CHIMIQUE. Destiné aux étudiants de 2ème année Génie des Procédés. Dr. Rachida OUARGLI-SAKER. 2019-2020. Page 2. 1. SOMMAIRE. CHAPITRE I : RAPPELS EN
 Thermodynamique et Cinétique Chimique Cours de Chimie 2
Thermodynamique et Cinétique Chimique Cours de Chimie 2
Il s'adresse principalement aux étudiants de première et deuxième année SM domaine Génie Physique et. Technologie des Matériaux sans oublier les étudiants
 Chimie Générale (Chimie 1)
Chimie Générale (Chimie 1)
Dec 23 2020 - Cours de chimie 1er année médecine
 Cours Thermo Chahra
Cours Thermo Chahra
La thermodynamique chimique + les équilibres chimiques. Avant propos: Ce cours de thermodynamique est destiné aux étudiants de 1er années des sciences.
 COURS DE THERMODYNAMIQUE
COURS DE THERMODYNAMIQUE
Ce cours de thermodynamique est destiné aux étudiants de 1 ère année Relation entre l'enthalpie et l'énergie interne d'une réaction chimique………... 38.
 Introduction à la thermodynamique chimique
Introduction à la thermodynamique chimique
Energie interne et enthalpie. 1. Conservation de l'énergie. L'énergie totale d'un système isolé se conserve au cours de ses
 «EXERCICES ET PROBLEMES CORRIGES DE
«EXERCICES ET PROBLEMES CORRIGES DE
Exercices et problèmes corrigés de thermodynamique chimique. 9. AVANT-PROPOS. Cet ouvrage s'adresse aux étudiants de la première année des filières.
 Résumé de cours et recueil dexercices corrigés de
Résumé de cours et recueil dexercices corrigés de
corrigés de thermodynamique chimique » vise à mettre à la disposition des étudiants de première année des facultés des sciences un outil qui leur permettra
 FACULTE DE CHIMIE DEPARTEMENT DE CHIMIE ORGANIQUE
FACULTE DE CHIMIE DEPARTEMENT DE CHIMIE ORGANIQUE
Z.Khouba USTOMB
 Chimie des solutions et thermodynamique. Cours.
Chimie des solutions et thermodynamique. Cours.
1ère année Chimie 2. Chimie des solutions et thermodynamique. Cours. PROGRAMME. 1. Equilibres chimiques. 1.1. Equilibre
 Thermodynamique et chimie des solutions Cours et Exercices
Thermodynamique et chimie des solutions Cours et Exercices
Ce cours s'adresse particulièrement aux étudiants de première année LMD Licence. Génie Industriel. C'est un module de chimie du 2ème semestre nommé Chimie 2
 COURS DE CHIMIE GENERALE Semestre 1 SVI
COURS DE CHIMIE GENERALE Semestre 1 SVI
PARTIE II : THERMOCHIMIE. CHAPITRE I : INTRODUCTION A LA THERMODYNAMIQUE CHIMIQUE. I. INTRODUCTION. II. LE SYSTEME. III. LES VARIABLES D'ETAT
 Chimie Générale (Chimie 1)
Chimie Générale (Chimie 1)
Le chapitre (VI) concerne l'étude de la thermodynamique chimique en Cours de chimie 1er année médecine Pr. B. Legseir; Faculté de médecine; Université.
 Chapitre 1. Rappel des principes de thermodynamique
Chapitre 1. Rappel des principes de thermodynamique
année constituent la suite logique du cours de Thermochimie et. Thermodynamique de 1ère année SMPC semestre 1. Ouvrages conseillées.
 [PDF] COURS DE THERMODYNAMIQUE - univ-ustodz
[PDF] COURS DE THERMODYNAMIQUE - univ-ustodz
Ce cours de thermodynamique est destiné aux étudiants de 1 ère année d'enseignement supérieur de spécialité génie des procédés et science de la matière
 [PDF] Thermodynamique chimique - univ-ustodz
[PDF] Thermodynamique chimique - univ-ustodz
THERMODYNAMIQUE CHIMIQUE COURS ET APPLICATIONS Destinés aux étudiants de L3 Chimie Physique Sciences de la Matières et Chimie Industrielle
 [PDF] Thermodynamique chimique
[PDF] Thermodynamique chimique
Thermodynamique chimique 4/18 Le premier principe de la thermodynamique I Propriétés des grandeurs d'état On a vu dans le cours précédent qu'un système
 [PDF] Cours de Thermodynamique Chimique
[PDF] Cours de Thermodynamique Chimique
L'objectif de ce chapitre est de faire le lien entre les connaissances acquises en thermodynamique physique et le cours de thermochimie
 Thermodynamique 1 : Cours Résumés exercices et examens
Thermodynamique 1 : Cours Résumés exercices et examens
Thermodynamique 1 : Cours Résumés exercices et examens corrigés Le but de la chimique exercices corrigés 1ere année pdf # thermodynamique classique
 thermodynamique chimique exercices corrigés 1ere année pdf
thermodynamique chimique exercices corrigés 1ere année pdf
Étiquette thermodynamique chimique exercices corrigés 1ere année pdf Thermochimie : Cours-Résumés-Exercices-Examens corrigés
 Cours Thermochimie PDF Gratuit (S1 L1) - eBoikcom
Cours Thermochimie PDF Gratuit (S1 L1) - eBoikcom
Télécharger gratuitement le cours complet de Thermochimie PDF S1 SMPC Bachelor / Licence en Chimie Physique (1ère année PC / SMC) Pour les TD QCM
 [PDF] thermochimie/equilibres chimiques - Faculté des sciences de meknès
[PDF] thermochimie/equilibres chimiques - Faculté des sciences de meknès
MODULE CHIMIE GENERALE COURS THERMOCHIMIE/EQUILIBRES CHIMIQUES Réalisé par : Pr Hamid MAGHAT ANNEE UNIVERSITAIRE : 2017/2018
 [PDF] Cours de Thermodynamique
[PDF] Cours de Thermodynamique
13 fév 2019 · et d'autres ne peuvent être obtenues que par un calcul (énergie interne entropie po- tentiel chimique etc ) On distingue les variables
 [PDF] PREMIER PRINCIPE DE LA THERMODYNAMIQUE ENERGIE
[PDF] PREMIER PRINCIPE DE LA THERMODYNAMIQUE ENERGIE
DEPARTEMENT DE CHIMIE Filière sciences de la matière COURS DE THERMOCHIMIE SMP-SMC Semestre 1 Préparé par : Moulay Rachid LAAMARI Septembre 2016
Mohamed BOUDIAF »
Faculté de Chimie
Département de Génie des Matériaux
Destiné
aux étudiants de 1ère année Génie des ProcédésRachida OUARGLI-SAKER
2015-2016
Scientifique
COURS DE
THERMODYNAMIQUE
République Algérienne Démocratique Et PopulaireAvant propos :
Ce cours de thermodynamique est destiné aux étudiants de 1ère année érieur de spécialité génie des procédés et science de la matière. Le premier chapitre introduit les notions fondamentales et les premières définitions utilisées en .Le deuxième chapitre développe
premier principe. Le troisième chapitre est consacré à la chimie. Le quatrième et dernier chapitre présente le deuxième principe de la thermodynamique, les notions et les différentes expr ainsi introduction aux machines thermiques et les cycles thermodynamiques. Cette présentation résulte de la lecture de nombreux ouvrages et documents dont la plupart ne sont pas cités dans la bibliographie.Tables des matières
CHAPITRE I : Notions fondamentales de la thermodynamiqueI. 1. Introduction générale 01
I.1.1. Notion de la température 02
I.1.2. Notion de la pression 03
05I.1.4. Unités 05
06I.2.1. Définition du système 06
I.2.3. Evolution ou transformation du système 07 08 I.2.5. Représentations graphiques des évolutions du système 10I.2.6. 11
I.2.7. Principe zéro 12
CHAPITRE II : travail, chaleur, énergie interneII.1. Introduction 13
(U) 13II.2.1. 13
II.3. La chaleur (Q) 14
II.3.1. Chaleur sensible 14
II.3.2. Chaleur latente 15
II.3.3. Calorimétrie 16
II.4. Le travail (W) 19
II.5. Convention du 21
II.6. Le 1er principe de la thermodynamique 22
II.6.1. Enoncé du 1er principe de la thermodynamique 22 23II. 8. Capacité calorifique 24
II.9. Les transformations réversibles 26
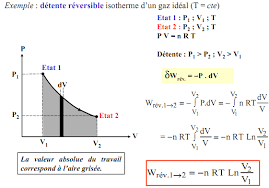
II.9.1. ransformationisochore (à volume constant) 26 II.9.2. ransformation isobare (à pression constante) 27 II.9.3. ransformationisotherme (à température constante) 29 II.9.4. ransformationadiabatique (chaleur Q constante) 30 CHAPITRE III : Thermochimie : Application du 1er principe à la chimie III. 1. Etat standard et chaleur de réaction 36III. 2. Relation entre 38
III.3. Enthalpie standard de réaction 39
III.4. Loi de HESS 40
III.5. Loi de KIRCHOFF 43
III.6. Energie de la liaison covalente 45
CHAPITRE IV : 2ème principe de la thermodynamiqueIV.1. Introduction 47
47IV.3. Enoncés du second principe 48
IV.3.1. Enoncé de CLAUSIUS 48
IV.3.2. Enoncé de KELVIN 48
IV.3.3. Enoncé mathématique 49
5153
IV.5.1. Transformation isotherme réversible 53
IV.5.2. Transformation isobare réversible 53
IV.5.3. Transformation isochore réversible 54
IV.5.4. Transformation adiabatique 54
5455
IV.7. 57
IV.8. 60
60IV.10. Les machines thermiques 62
IV.10.1. Machines thermodynamiques (T.D) 62
IV.10.2. Machines dynamo-thermiques (D.T) 63
IV.11. Cycles thermodynamiques 64
IV.11.1. Cycle de Carnot 65
IV.11.2. Cycle de Beau Rochas (OTTO) 66
IV.11.3. Cycle de Diesel 66
IV.11.4. Cycle de Rankine 67
IV.11.5. Cycle de Stirling 68
Références bibliographiques 71
1 CHAPITRE I : Notions fondamentales de la thermodynamiqueI. 1. Introduction générale
La thermodynamique est une science qui nait à la fin du 17ème siècle On rapporte que Denis PAPIN (Physicien français, 1647-1714 et ainsi fournir du travail. trouver les conditions optimales pour transformer la chaleur en travail. On trouve dans cette phrase les trois (03) mots fondateurs de la thermodynamique. Ce non (thermodynamique) vient du grec signifiant respectivement chaleur et force. On peut décrire la thermodynamique de deux (02) manières ou selon deux (02) aspects différents : a. : on s microscopique ou atomique en utilisant comme variables les grandeurs cinétiques thermodynamique classique ou statique. a. Thermodynamique classique Elle explique le comportement de la matière ou des systèmes en fonction de leurs variationsévolution et dresse le bilan énergétique du système. Le chemin suivi par la transformation du
système peut jouer un rôle (la notion de réversibilité des transformations). 2 b. Thermodynamique statique et la signification des variables macroscopiques (P, T) et chaleur.I. 1. 1. Notion de température
Vi des
molécules et donc leur énergie cinétique Ei du milieu est plus grand.A la température 0K (Zéro absolu à -273°C), les atomes et les molécules qui constituent la
matière sont figées.Exemple :
, les molécules du gaz se totalement aléatoire avec des vitesses Vi.Gaz dans une enceinte
Donc la température est définie par la relation suivante:Où :
M est la masse des particules.
V est la vitesse des particules qui constituent la matière. k est une constante.T est la température de la matière.
3 On peut définir plusieurs échelles de température, telle qui précède toute autre échelle. e (K) en kelvin en fonction du Celsius. selon une échelle prédéfinie. Il existe différents types de thermomètres utilisés dans la pratique, ci-dessous quelques exemples les plus utilisé :Les thermomètres à mercure.
Les résistances de platine utilisables entre de 200 à °C630.à 1300°C.
Les résistances à semi-conducteurs en Germanium (Ge) pour T< 77 KI. 1. 2. Notion de la pression
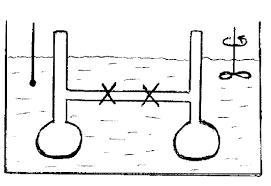
La pression est due aux nombreux chocs des atomes ou molécules de la matière sur les parois du récipient.Exemple :
a N molécules de gaz en agitation permanente.Pression dans une enceinte
4Soit ܖ
Donc, on définit la pression par la relation suivante:Où :
P est la nte.
M est la masse des molécules de gaz.
V est la vitesse des molécules de gaz.
On distingue entre pression absolue et relative et entre pression totale et partielleOù :
Pabs : Pression absolue.
Prel : Pression relative.
Patm : Pression atmosphérique.
Où :
Pi : Pression partielle.
Xi : Fraction molaire.
PT : Pression totale.
Donc :
5 I. 1. Les échanges de lde la matière se présentent sous deux formes possibles; la chaleur (Q) ou le travail (W). chelle microscopique comme une et des atomes sous forme désordonnée (chaleur Q), ou ordonnée (travail W).Déplacement du piston
Transfert de chaleur (Q) Transfert de travail (W) par déplacement du pistonI. 1. 4. Unités
La majorité des unités en Système international [S. I] utilisés dans ce cours sont les suivants :
Temps : en secondes [s]
Température : en degré Kelvin [K]
Pression : en Pascal [Pa] ou [N/m2]
1 Pa = 1 N/m2 ; 1atm = 1,013bar = 1,013105 Pa = 760 Torr = 76 cmHg
1 bar = 105 Pa = 750 Torr
Energie: en Joule [J] et
1 calorie = 4,184 Joules
Puissance : en Watt [W] et 1W = 1 J/s
6 I.I. 2. 1. Définition du système
Pour décrire thermodynamiquement un système, il faut à la fois : Définir le système en délimitant ses frontières par rapport au milieu extérieur.Le système est défini comme une partie de matière (de masse donnée) délimitée par rapport
space entourant le système.Milieu
Extérieur
Délimitation du système
Il existe différents types de systèmes thermodynamiques qui sont représentés dans le tableau
ci-dessous:Système Echange de
matière ExempleIsolé Non Non Calorimètre
Fermé Non Oui Piles électriques
Ouvert Oui Oui Être vivant
Système Système
7I. 2. 2. Etat du système
les macroscopiques (m, P, T, V,etc) dites aussi . possibles. des valeurs bien définies et constantes.On distingue alors selon le cas entre :
Variables ou grandeurs thermiques (P, V, T) ou calorifiques (U, H, W, Q, S). Variables extensives, -à dire proportionnelles à la quantité de matière telle que (m, V, U,..etc) ou variables intensives, -à dire indépendantes de la masse telle que (P,T, concentration,). On définit souvent des grandeurs massiques-à d système telle que : le volume massique. I. 2. 3. Evolution ou transformation du système système évolue et les variables dmodifiés. On dit que le système se initial (1) à un autre état final (2). (W ou Q cédés) Ou (W ou Q reçus)Evolution
Etat (1) Etat (2) (Q ou W) avec le milieu extérieurP1, V1, T1 P2, V2, T2
8 Au cours du système varient pour atteindre un autrequotesdbs_dbs5.pdfusesText_9[PDF] rendez vous de carriere education nationale
[PDF] notice rendez-vous de carrière
[PDF] rendez vous de carriere hors classe
[PDF] the napalm girl
[PDF] système thermodynamique ouvert
[PDF] exercices corrigés thermodynamique système ouvert
[PDF] système thermodynamique pdf
[PDF] grandeur thermodynamique définition
[PDF] système isolé thermodynamique
[PDF] système endocrinien schéma
[PDF] la petite fille de monsieur linh contexte historique
[PDF] système endocrinien powerpoint
[PDF] la petite fille de monsieur linh pdf gratuit
[PDF] projet de résolution copropriété

