 TP C5 Dissolution
TP C5 Dissolution
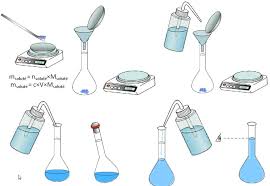
Q1. Nommer le soluté et le solvant pour préparer la solution aqueuse de sulfate de cuivre. Q2. Quelle verrerie permet de mesurer le volume de la solution
 TP-Préparation dune solution de sulfate de cuivre de concentration
TP-Préparation dune solution de sulfate de cuivre de concentration
En déduire la masse de sulfate de cuivre qu'il faut dissoudre pour préparer la solution souhaitée. 4. Déterminer la concentration molaire des ions sulfate
 TP4 : La bouillie bordelaise
TP4 : La bouillie bordelaise
Après avoir rappelé quelques formules fondamentales de la chimie la première solution sera préparée par dissolution de sulfate de cuivre
 Activité expérimentale
Activité expérimentale
d'un problème ici
 TP N°8 de chimie Nom
TP N°8 de chimie Nom
Avant dissolution l'espèce chimique peut être un solide Exemple : on a dissous m = 2
 Santé-TP n°7 : Préparation dune solution. Dilution
Santé-TP n°7 : Préparation dune solution. Dilution
Ce produit est à base de sulfate de cuivre de formule CuSO4 . 1°)Préparation par dissolution d'un solide. Préparer les solutions aqueuses de sulfate de
 TP Recyclage du sulfate de cuivre
TP Recyclage du sulfate de cuivre
Un exemple d'utilisation d'une solution de sulfate de cuivre est celui du raffinage du cuivre mentionnée dans le document 7. Or ( lors de la dissolution
 TP n°3 : Dissolution et dilution - mon cours de physique chimie
TP n°3 : Dissolution et dilution - mon cours de physique chimie
dissolution. 1) Calculer la masse de soluté à dissoudre ... 3) Calculer la concentration massique en sulfate de cuivre de la solution de sulfate de cuivre.
 TP n°1 : Préparation dune solution - mon cours de physique chimie
TP n°1 : Préparation dune solution - mon cours de physique chimie
Pour cela il dispose de sulfate de cuivre solide. Objectif : Préparer une solution de concentration molaire donnée par dissolution et dilution. TP n°1 :.
 TP n°12 - Dissolution + corrigé
TP n°12 - Dissolution + corrigé
Le sulfate de cuivre hydraté est un solide ionique dont la formule est : CuSO45 H2O. 1. Définitions. Une solution est un mélange liquide homogène dans lequel
 TP C5 Dissolution
TP C5 Dissolution
Q1. Nommer le soluté et le solvant pour préparer la solution aqueuse de sulfate de cuivre. Q2. Quelle verrerie permet de mesurer le volume de la solution
 TP-Préparation dune solution de sulfate de cuivre de concentration
TP-Préparation dune solution de sulfate de cuivre de concentration
On introduit pour cela du sulfate de cuivre solide CuSO4 dans de l'eau distillée. 1. Donner la nature des ions présents en solution après dissolution. 2. Ecrire
 TP Chimie Seconde N°12
TP Chimie Seconde N°12
a) Par dissolution de sulfate de cuivre solide : Il s'agit en s'inspirant de l'exemple précédent de préparer V = 100 mL d'une solution de concentration C
 TP CHIMIE
TP CHIMIE
TP 10-Principe de dissolution et dilution: Echelle de teinte. Objectif : 1) Préparation d'une solution mère de sulfate de cuivre par dissolution :.
 TP N°8 de chimie Nom
TP N°8 de chimie Nom
Une solution est obtenue par dissolution d'une espèce chimique dans un solvant. On dissout du sulfate de cuivre solide dans de l'eau : le solvant est ...
 TP CHIMIE
TP CHIMIE
TP 10-Principe de dissolution et dilution: Echelle de teinte. Objectif : 1) Préparation d'une solution mère de sulfate de cuivre par dissolution :.
 Santé-TP n°7 : Préparation dune solution. Dilution
Santé-TP n°7 : Préparation dune solution. Dilution
1°)Préparation par dissolution d'un solide. Préparer les solutions aqueuses de sulfate de cuivre suivantes : Masse à dissoudre. Volume de la solution.
 DE LA BOUILLIE MAIS PAS NIMPORTE COMMENT ! Les données
DE LA BOUILLIE MAIS PAS NIMPORTE COMMENT ! Les données
1-bouillie_bordelaise.pdf
 TP4 : La bouillie bordelaise
TP4 : La bouillie bordelaise
par dissolution de sulfate de cuivre puis la seconde par dilution de la solution précédente. L'étude d'un document permettra de conclure sur la réelle
 1S CH12 TP Extraction dune espèce en solution CORRIGE.pub
1S CH12 TP Extraction dune espèce en solution CORRIGE.pub
Par ailleurs le sulfate de cuivre est insoluble dans le cyclohexane; il restera en solution dans la solution aqueuse S. On remet la phase aqueuse du bécher A
 [PDF] TP-Préparation dune solution de sulfate de cuivre de concentration
[PDF] TP-Préparation dune solution de sulfate de cuivre de concentration
On introduit pour cela du sulfate de cuivre solide CuSO4 dans de l'eau distillée 1 Donner la nature des ions présents en solution après dissolution 2 Ecrire
 [PDF] TP C5 Dissolution - Labo TP
[PDF] TP C5 Dissolution - Labo TP
On souhaite préparer 500 mL d'une solution aqueuse de sulfate de cuivre de concentration Cm1 en dissolvant une masse de sulfate de cuivre de 025 g Q1 Nommer
 [PDF] TP n°12 - Dissolution + corrigé - Canal Blog
[PDF] TP n°12 - Dissolution + corrigé - Canal Blog
Le sulfate de cuivre hydraté est un solide ionique dont la formule est : CuSO45 H2O 1 Définitions Une solution est un mélange liquide homogène dans lequel
 [PDF] TP 10-Principe de dissolution et dilution: Echelle de teinte
[PDF] TP 10-Principe de dissolution et dilution: Echelle de teinte
L'échelle de teintes que l'on va réaliser sera composée de solutions de sulfate de cuivre à différentes concentrations molaires Nous l'obtiendrons en préparant
 [PDF] Sujet sur la préparation dune solution de sulfate de cuivre II
[PDF] Sujet sur la préparation dune solution de sulfate de cuivre II
OBJECTIF DU T P : Fabrication d'une solution ionique de concentration molaire donnée «Pendant le déroulement de ce TP le port de lunettes de sécurité
 [PDF] Activité expérimentale
[PDF] Activité expérimentale
Le but de ce projet est de réaliser l'ensemble des étapes qui permettent d'arriver à la résolution d'un problème ici la concentration en sulfate de cuivre
 [PDF] TP : Synthèse et analyse dun complexe de cuivre - CPGE Brizeux
[PDF] TP : Synthèse et analyse dun complexe de cuivre - CPGE Brizeux
TP : Synthèse et analyse d'un complexe de cuivre Synthèse du complexe 1 Placer 31 g de CuSO4 5H2O dans un erlenmeyer
 [PDF] TP Chimie Seconde N°12
[PDF] TP Chimie Seconde N°12
Il s'agit de préparer 100 mL de solution de sulfate de cuivre (II) de concentration fixée à partir de sulfate de cuivre solide de formule CuSO4
 [PDF] Préparation dune solution aqueuse par
[PDF] Préparation dune solution aqueuse par
Questions pour préparer le TP La bouillie bordelaise est un pesticide constitué d'un mélange de sulfate de cuivre et de chaux éteinte
 [PDF] PRÉPARATION DUNE SOLUTION ET ÉCHELLE DE TEINTE
[PDF] PRÉPARATION DUNE SOLUTION ET ÉCHELLE DE TEINTE
La concentration massique de la solution en sulfate de cuivre est : Cm = II) Préparation d'une solution par dissolution d'un solide dans l'eau
Comment faire une dilution TP ?
Réaliser une dilution consiste à diminuer la concentration molaire d'une solution en ajoutant de l'eau (le solvant). La solution initiale utilisée est appelée la solution mère. Le volume prélevé de la solution mère sera noté Vi et sa concentration molaire Ci. La solution finale préparée est appelée la solution fille.Quelle est l'équation de dissolution du sulfate de cuivre ?
Le solvant est l'eau et le soluté est le sulfate de cuivre(II) pentahydraté CuSO4 ,5H2O 1.2. Montre que la concentration en soluté apporté de la teinture mère est C0 = 4,00.10–1 mol. L–1. M(CuSO4 ,5H2O) = 63,5+32,0+(4x16)+(5x18) = 249,5g.Comment diluer le sulfate de cuivre ?
Le sulfate de cuivre doit d'abord être dilué, à raison de 200g de sulfate de cuivre pour 2 litres d'eau. La chaux éteinte est préparée à part en diluant 300g de chaux dans 4 litres d'eau froide. Une fois ces deux solutions réalisées, elles peuvent être mélangées en ajoutant à nouveau 4 litres d'eau.- Faire une dissolution
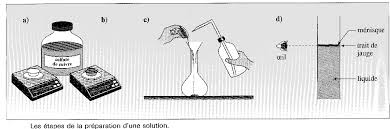
On verse le soluté dans une fiole. On ajoute de l'eau distillée aux 2/3 de la fiole environ et on agite la fiole pour dissoudre totalement le soluté On complète avec de l'eau distillée jusqu'au trait de jauge (en faisant attention au ménisque)