|
1 De la mécanique classique `a la quantique
RH = Ry hc rayon de Bohr a0 = r1 = 5 29 × 10−11 m = 0 529 ˚A Fréquence d'émission et énergie de transition Condition de résonance de Bohr: hν = ∆E = En2 |
|
Chapitre 55b – Le spectre de lhydrogène et le modèle de Bohr
r : Rayon de Bohr (rayon de l'orbite fondamentale) m 295 11 1 − = r Page Exemple : (l'énergie du photon en fonction de sa fréquence est hf E = γ ) |
|
CHAPITRE III : QUANTIFICATION DE LENERGIE
Le modèle de Bohr est une théorie physique cherchant à comprendre la constitution d'un atome et plus particulièrement celui de l'hydrogène et des ions |
|
La genèse de latome de Bohr
Par un calcul classique Bohr établit une relation entre la fréquence données q (latitude rayon vecteur azimut) et aux moments conjugués p |
|
Modèle de Bohr (1913)
Reste à démontrer théoriquement l'existence de la quantification Modèle de (rayon de Bohr) Dimension de ?? Expression de E totale en fonction du rayon |
|
Modele de bohr de latome dhydrogène
On se propose d'étudier le modèle de l'atome d'hydrogène proposé par Niels Bohr en 1913 Ce modèle est une continuité du modèle planétaire proposé par |
|
Modèle de Bohr
: 1er rayon de Bohr J s 10 1 05 2π h 34- = = ħ en utilisant (3) L'électron émet un rayonnement lorsqu'il passe d'une orbite permise stable d'énergie Ei à |
Comment calculer le rayon de Bohr ?
Le rayon de Bohr est une constante physique égale à la distance entre le noyau et l'électron d'un atome d'hydrogène à l'état fondamental.
Sa valeur est donnée par la formule ��₀ = 4����₀(ℎ barre)²/��_e (��_e)².Quel est le modèle de l'atome décrit par Bohr ?
La description du modèle de Rutherford-Bohr
L'atome est représenté par un espace presque vide avec, au centre, un noyau massif et dense contenant les protons.
Les électrons circulent autour du noyau de l'atome sur des couches électroniques.
Il peut y avoir plus d'un électron par couche électronique.C'est quoi le postulat de Bohr ?
Réponse.
Le modèle atomique de Bohr stipule que la quantité de mouvement angulaire �� d'un électron dans un atome est quantisé.
Plus précisément, cela implique que �� ne peut être qu'un multiple entier de la constante de Planck réduite ℏ .- Utilisez la formule ��_�� = ��₀ ��², où ��_�� est le rayon orbital d'un électron au niveau énergétique �� d'un atome d'hydrogène et ��₀ est le rayon Bohr, pour calculer le rayon orbital d'un électron qui est au niveau énergie �� = 3 d'un atome d'hydrogène.
|
DL n 14 : Atome de Bohr
D'apr`es Bohr l'électron a un mouvement circulaire de rayon r et de vitesse v autour de O. Le champ de pesanteur est négligeable `a l'échelle atomique et |
|
Chapitre 10: Atome de Bohr
rn = rayon de l'orbite de l'électron autour du noyau postulat de Bohr seules les orbites dont les rayons sont définis par. |
|
Modèle de Bohr (1913)
en fonction du rayon de Bohr Autre conséquence: On notera (sans démo) que le paquet s'élargi(ra) au cours du temps. |
|
Atome de Bohr
Cette condition est remplie par une série de rayon rn où n=12 |
|
Approche Documentaire : - Les inégalités de Heisenberg
[qui est] le rayon de Bohr de l'atome d'hydrogène. Naturellement le fait que l'on obtienne exactement dans ce calcul d'ordre de grandeur est un hasard |
|
Introduction à la mécanique quantique
uniforme de rayon r et à la vitesse v autour du proton. Fig. 1. Remarquons dès à présent que la condition de Bohr se trouve justifiée : dans une. |
|
MariePaule Bassez http://wwwiutschuman.ustrasbg.fr/chemphys/mpb
53 pm = rayon de la 1ère orbite de Bohr de l'hydrogène (n = 1). Le rayon de la 2ème orbite est: r (cf. démonstration dans ChimiePhysique Peter Atkins). |
|
MariePaule Bassez http://wwwiutschuman.ustrasbg.fr/chemphys/mpb
Calcul de probabilité de présence de l'électron dans une couche située au niveau du rayon de Bohr. Dans l'état fondamental l'électron de l'atome d'hydrogène |
|
Évolution Du paramètre exciton de BOHR EN FONCTION DES
27 avr. 2013 Le rayon de Bohr est une unité de mesure utilisée en physique atomique pour décrire le plus petit rayon possible d'un électron gravitant ... |
|
Chapitre 2 :Quantification de lénergie de latome dhydrogène
Niels Bohr a posé deux affirmations : Postulat mécanique : L'électron de l'atome II M odèle de Bohr de l'atome d'hydrogène ... rayon R et de vitesse V :. |
|
Modèle de Bohr (1913)
Hypothèse fondamentale de Bohr: Seules certaines orbites sont possibles le moment cinétique de l'électron est quantifiée en fonction du rayon de Bohr |
|
Chapitre 10: Atome de Bohr - ALlu
10 Atome de Bohr 121 Le modèle prévoit que les électrons orbitent à des rayons fixes autour du proton Ceci s'est avéré être faux après que Heisenberg eut |
|
DL n 14 : Atome de Bohr
D'apr`es Bohr l'électron a un mouvement circulaire de rayon r et de vitesse v autour de O Le champ de pesanteur est négligeable `a l'échelle atomique et |
|
Fiche explicative de la leçon : Modèle atomique de Bohr - Nagwa
Dans cette fiche explicative nous allons apprendre à calculer le rayon orbital d'un électron à différents niveaux d'énergie d'un atome d'hydrogène |
|
CHAPITRE III : QUANTIFICATION DE LENERGIE
Le modèle de Bohr est une théorie physique cherchant à comprendre la constitution d'un atome et plus particulièrement celui de l'hydrogène et des ions |
|
Formule des rayons de Bohr : démonstration - YouTube
30 jan 2017 · Démonstration de la formule des rayons de Bohr à partir de la mécanique classique et Durée : 11:24Postée : 30 jan 2017 |
|
ATOME DE BOHR ( 2016/2017)
Bohr a donné plusieurs postulats: 1- L'électron de l'atome d'hydrogène ne gravite autour du noyau que sur certaines orbites privilégiées (orbites stationnaires) |
|
Introduction à la mécanique quantique
Dans ce premier modèle « planétaire » classique l'électron présente un mouvement circulaire uniforme de rayon r et à la vitesse v autour du proton Fig 1 |
|
Niels Bohr le père de latome - OpenEdition Journals
1 déc 2013 · Ce problème conduit Niels Bohr à émettre en 1913 des hypothèses audacieuses : les orbites circulaires des électrons sont stables et leur rayon a |
|
CHAPITRE IV Modèles Atomiques Et Quantification Energétique
Cette valeur est notée a0 et appelé premier rayon de Bohr pour l'atome d'hydrogène ? Pour n=2 (premier état excité) r2 = 4r1 = 2116Å Le calcul du rayon d' |
Comment déterminer le rayon de Bohr ?
Le rayon de Bohr est une constante physique égale à la distance entre le noyau et l'électron d'un atome d'hydrogène à l'état fondamental. Sa valeur est donnée par la formule ��? = 4����?(? barre)²/��_e (��_e)².Quelle est la signification du rayon de Bohr ?
Dans le modèle de Bohr de l'atome d'hydrogène, le rayon de Bohr est la longueur caractéristique séparant l'électron du proton. C'est donc un ordre de grandeur du rayon des atomes.Comment faire le modèle de Bohr ?
Comment dessiner le modèle atomique de Rutherford-Bohr
1Déterminer le nombre de protons.2Déterminer le nombre d'électrons.3Distribuer les électrons sur les couches électroniques.4Vérifier la configuration électronique de l'atome dessiné- Le modèle de Bohr ne fonctionne pas pour les systèmes ayant plus d'un électron.
| TD N°3 Le Modèle de Bohr - Université Paris-Saclay |
| Chapitre 2 : Spectre des Hydrogénoïdes et Modèle de BOHR |
| DL no14 : Atome de Bohr - ac-bordeauxfr |
| ATOME DE BOHR ( 2016/2017) |
| 10 Atome de Bohr - archiveorg |
| Searches related to demonstration rayon de bohr filetype:pdf |
|
Chapitre 10: Atome de Bohr
Le modèle prévoit que les électrons orbitent à des rayons fixes autour du proton Ceci s'est avéré être faux après que Heisenberg eut établi son fameux principe d' |
|
DL n 14 : Atome de Bohr
D'apr`es Bohr, l'électron a un mouvement circulaire de rayon r et de vitesse v autour de O Le champ de pesanteur est négligeable `a l'échelle atomique et l' |
|
Atome de Bohr
Cette condition est remplie par une série de rayon rn où n=1,2,3, est le numéro de l'orbite appelé nombre quantique principal La longueur d'onde de l'électron |
|
Modèle de Bohr (1913) - LCPMR
en fonction du rayon de Bohr m e e 2 (4πεo ) 2 Autre conséquence: On notera (sans démo) que le paquet s'élargi(ra) au cours du temps (2) (2) (1) (1) (1) |
|
Modèles de latome - chimie-physique
53 pm = rayon de la 1ère orbite de Bohr de l'hydrogène (n = 1) Le rayon de la (cf démonstration dans ChimiePhysique Peter Atkins) Pour une particule se |
|
La genèse de latome de Bohr - Reflets de la physique
Bohr reste obsédé par la question du Cette idée, Bohr ne peut l'accepter, car elle est incompatible avec son projet d'utiliser le quantum de Planck pour noyau positif, en fonction du rayon de Reproduisons la nouvelle démonstration |
|
Latome dhydrogène
Le modèle de Bohr ✓ Trajectoire circulaire : (avec ) Une théorie non relativiste est donc adaptée α est la constante de structure fine est le rayon de Bohr |
|
Introduction `a la mécanique quantique
4 3 Discussion critique du mod`ele de Bohr o`u a0 est le rayon de Bohr défini par l'équation (71) et A est une constante de nor- malisation Remarquez que |
|
Introduction à la mécanique quantique
uniforme de rayon r et à la vitesse v autour du proton Fig 1 atomique Remarquons dès à présent que la condition de Bohr se trouve justifiée : dans une |
DL no14 : Atome de Bohr
D’apr`es Bohr, l’´electron a un mouvement circulaire de rayon r et de vitesse v autour de O Le champ de pesanteur est n´egligeable `a l’´echelle atomique et l’´electron n’est soumis qu’`a la force d’interaction ´electrostatique : −→ F = − e2 4π 0r2 −→e r
Les Modèles de latome
4 Le modèle de Bohr pour l'atome d'hydrogène et les ions hydrogénoïdes 5 La théorie ondulatoire des particules 5 1 La relation de Louis de Broglie 5 2 La diffraction des électrons 5 3 Onde stationnaire de Louis de Broglie 5 4 Le microscope électronique 5 5 Dualité ondecorpuscule
Physique quantique - Collège de France
Rayon de Bohr: Dipôle électrique moyen de la superposition des états circulaires n et n-1 : D=qn2a 0 /2 Durée de vie des atomes circulaires
phy432 amphi4 pdf - Département de Physique de lEcole
9Modèle planétaire de l’atome (Perrin, Rutherford): Rydberg Effondrement dû au rayonnement électromagnétique de l’électron ?: entiers positifs Le modèle de Bohr 9Trajectoire circulaire : (avec ) Une théorie non relativiste est donc adaptée αest la constante de structure fine est le rayon de Bohr 9Moment cinétique quantifié
6 v7 Quantité de mouvement et moment cinétique
Le modèle de Bohr pour l'H On considère un électron de charge -e et masse m en orbite circulaire autour du proton de masse M et charge +e On a m ~ M/2000 donc le CG est proche du proton A l'équilibre: F centrifuge = F Coulomb: r M m € k ee r2 =m v2 r E cinétique: € K= 1 2 mv2= r 2 mv2 r = r 2 k e2 r2 =k e2 2r E potentielle: € U(r
LA STRUCTURE ATOMIQUE
la perception humaine En 9e année, ils ont dessiné le modèle atomique de Bohr pour les 18 premiers éléments En 10e année, ils ont été initiés aux diagrammes de Lewis Enfin, en physique de 11e année, les élèves se sont familiarisés avec les termes longueur d’onde et fréquence, sujets dont on traite dans le regroupement sur les
Classe invers ee VI : Moment cin etique orbital et
2 3 Forme adimensionnelle de l’ equation radiale E ectuez les changements de variable ˆ = r=a 0 et 2 = E=E i, ou a 0 = ~ 2=m e ˇ0;53 A est le rayon de Bohr et E i = m e 2=(2~ ) ˇ13;6 eV est l’ energie d’ionisation On notera qu’on suppose ici E
Cours de mécanique quantique - UMR 5582 - Laboratoire de
1 Notes de cours sur la Mécanique quantique Université Joseph ourier,F Grenoble; Master Physique M1 (version : 11 novembre 2015) Frédéric Faure
La fonction d’onde et l’équation de Schrödinger
Chapitre 1 La fonction d’onde et l’équation de Schrödinger 1 1 Introduction En physique classique, une particule est décrite par sa position r(t)
|
Modèle de Bohr
[PDF] Modèle de Bohr fsr ac ma cours physique abdlefdil ComplChap pdf |
|
Chapitre 10: Atome de Bohr
[PDF] Chapitre Atome de Bohr lnw lu Departements %Atome%de%Bohr pdf |
|
L atome d hydrogène de Bohr
[PDF] L 'atome d 'hydrogène de Bohr meine mathe de Chimie eModules b bc modelebohr pdf |
|
DL n 14 : Atome de Bohr
[PDF] DL n Atome de Bohrwebetab ac bordeaux DL Atome Bohr pdf |
|
Chapitre 55 #8211; Le spectre de l hydrogène et le modèle de Bohr
[PDF] Chapitre Le spectre de l 'hydrogène et le modèle de Bohrprofs cmaisonneuve qc ca svezina NYC XXI Chap% pdf |
|
L atome d hydrogène - ENS-phys
[PDF] L 'atome d 'hydrogène ENS phys phys ens ~dalibard transparentsX cours pdf |
|
Quantification de l énergie des atomes - Le Repaire des Sciences
[PDF] Quantification de l 'énergie des atomes Le Repaire des Sciences lerepairedessciences sciences agregation lp pdf |
|
Atome d hydrogène et quot;hydrogénoïdes quot;
[PDF] Atome d 'hydrogène et quot hydrogénoïdes quot liphy ujf grenoble IMG pdf chapitre pdf |
|
Chapitre 6 LE MAGNETISME ATOMIQUE
[PDF] Chapitre LE MAGNETISME ATOMIQUEmaster p obspm phyquant annee LPGA PA pdf |
|
COURS L1 Chapitre 1 l atomedot
ATTENTION La formule du rayon de Bohr est exigible au concours Cette démonstration met ? mal l 'appréhension de la matière par les modèles classiques de |
- hypothèse quantique de bohr
- equation de bohr espace mort
- modèle de bohr exercices
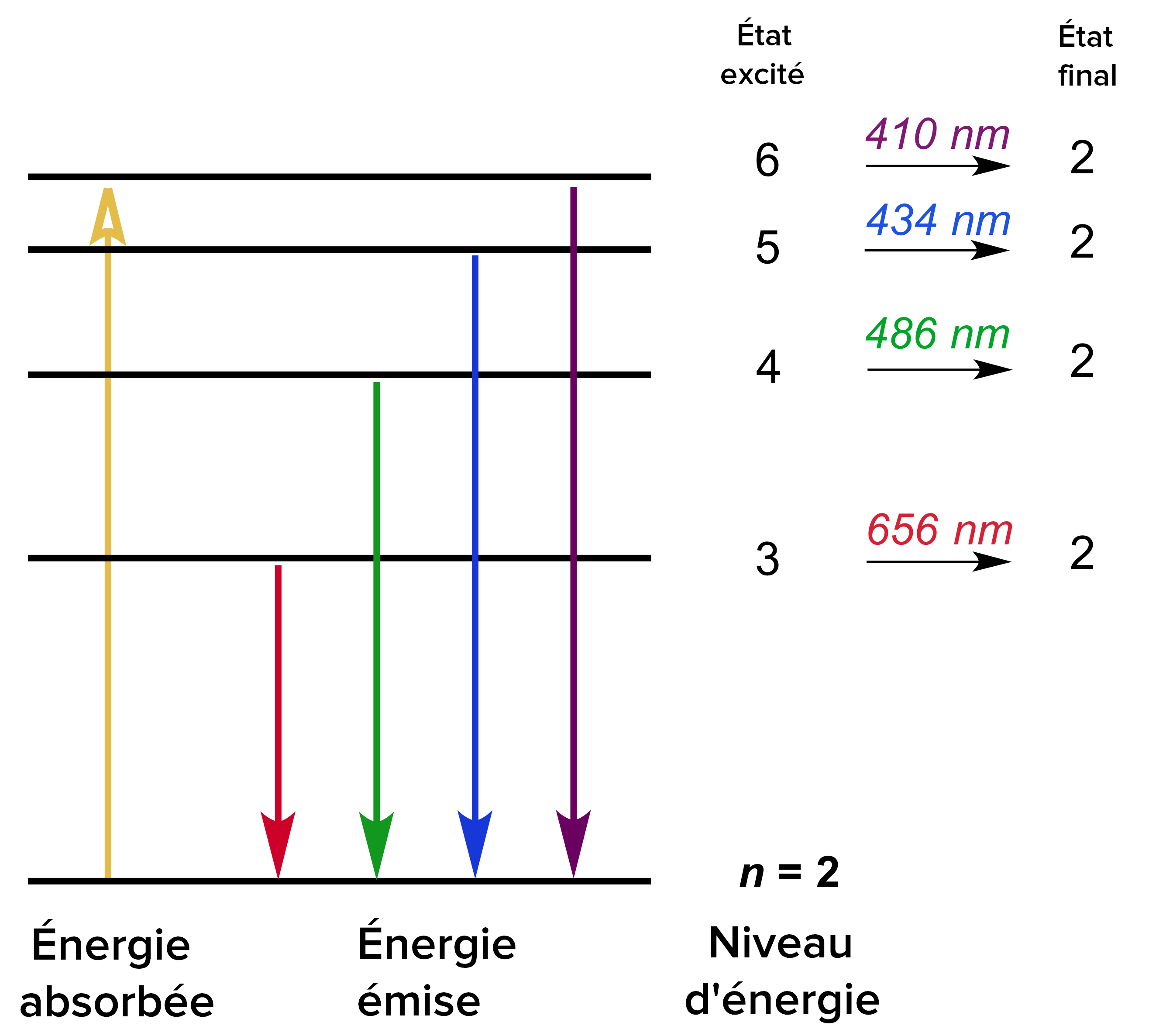
- interprétation du spectre de l'hydrogène
- hypothèse quantique de bohr pdf
- les postulats de bohr pdf
- quantification de l’énergie modèle de bohr pdf
- rayon du noyau de l'atome d'hydrogène
atome de bohr 2pdf
Source: Physique des particules
atome de bohr 2pdf
Source: Physique des particules
I Modèle atomique de Bohr-Sommerfeld - Claude Giménès
Source:https://cdn.kastatic.org/ka-perseus-images/284680f3cfc3e6865da65171d8a72ccfd6c75a14.png
Modèle de Bohr de l'atome d'hydrogène (leçon)
Source: Khan Academy
Modèle de Bohr de l'atome d'hydrogène (leçon)
Source: Khan Academy

Modèle de Bohr — Wikipédia
Source:https://upload.wikimedia.org/wikipedia/commons/thumb/f/fb/Onde_Corpuscule.png/260px-Onde_Corpuscule.png
modèle de bohr hydrogène
Modèle de Bohr
- modèle de bohr explication
- hypothèse quantique de bohr
- modèle de bohr cours
- hypothèse quantique de bohr pdf
- rayon de bohr valeur
- modèle de bohr exercices
- postulat de bohr
- interprétation du spectre de l'hydrogène
hypothèse quantique de bohr pdf
Niels Bohr, le père de l 'atome - BibNum
- modèle de bohr explication
- modèle de bohr hydrogène
- modèle de bohr pdf
- rayon de bohr valeur
- modèle de bohr cours
- modèle de bohr exercices
- postulat de bohr
- equation de bohr espace mort
rayon de bohr valeur
Chapitre 10: Atome de Bohr
- hypothèse quantique de bohr
- formule empirique de rydberg
- modèle de bohr exercices
- modèle quantique de l'atome exercices corrigés
- hypothèse quantique de bohr pdf
- atome de rutherford
- atome de schrodinger
- rayon du noyau de l'atome d'hydrogène
modèle de bohr exercices
TD N°2 L 'ATOME DE BOHR
- modèle de bohr pour l atome d hydrogène
- modèle de bohr cours
- exercice corrigé atome de bohr
- exercices corrigés de chimie générale pdf
- modèle quantique de l atome d hydrogène
- structure de la matière exercices corrigés pdf
- modèle de bohr explication
- postulat de bohr