|
Chapitre 12 Physique quantique
29 août 2013 · Les électrons d'un atome n'existe que sur certaines orbites autour du noyau L'état de la plus basse énergie est l'état fondamental |
|
Physique quantique et niveaux dénergie dun atome
24 mar 2022 · Pour les niveaux d'énergie d'un atome la coutume est d'attribuer au niveau fonda- mental d'énergie la valeur « zéro » et aux niveaux les plus |
|
Quantification des niveaux dénergie
Mots clés de recherche : quantification des niveaux d'énergie photon modèle de l'atome spectre de l'hydrogène Provenance : Académie d'Orléans-Tours Adresse |
|
Chapitre 2 :Quantification de lénergie de latome dhydrogène
Chaque état possède une énergie invariante (quantification des niveaux d'énergie de l'hydrogène) Postulat optique : La transition entre deux états accessibles |
|
NIVEAUX DENERGIE DE LATOME
Lors d'une transition d'un niveau d'énergie E à un niveau d'énergie E telle que n < p un atome d'hydrogène émet une longueur d'onde λ donnée par : hC λ |
Comment calculer l'énergie de l'atome ?
Atome d'hydrogène et ion hydrogénoïde : rappels
Si l'on calcule l'énergie de ce système, on trouve que les niveaux d'énergie possibles de l'atome d'hydrogène sont caractérisés par En = - R/n2 où n = 1, 2, 3, et où R est la constante de Rydberg qui vaut R = 13,6 eV.4 mar. 2005Quels sont les niveaux d'énergie d'un atome ?
Niveaux d'énergie des électrons atomiques
La mécanique quantique n'autorise qu'un nombre limité de valeurs de l'énergie ou niveaux.
Le niveau le plus bas (couche K) ne peut être occupé que par 2 électrons, le second niveau (couche L) par 8 électrons, le troisième (couche M) par 18 électrons.Comment déterminer les niveaux d'énergie ?
Dans un diagramme d'énergie, les énergies des différents niveaux sont exprimées en électronvolt : 1 eV = 1,601 × 10−19 J.
L'état le plus bas est appelé état fondamental.
Pour le lithium, l'énergie de l'état fondamental est de −5,39 eV.
Les autres états d'énergie sont appelés « états excités ».
|
Chapitre 2 :Quantification de lénergie de latome dhydrogène
L'électron de l'atome d'hydrogène ne possède qu'un nombre limité d'états accessibles. Chaque état possède une énergie invariante (quantification des niveaux |
|
Les niveaux dénergie des atomes de numéro atomique inférieur à 70
niveaux d'énergie sont effectués pour chaque atome |
|
Physique quantique et niveaux dénergie dun atome
Il est quand même assez facile de s'assurer de la pertinence des valeurs des niveaux d'énergie d'un atome et des longueurs d'onde des radiations émises en |
|
Niveaux dénergie dans les atomes. Défaut quantique - Effet décran
LES ATOMES. POLYELECTRONIQUES. La présence de plusieurs électrons complique le problème. : l'énergie d'un niveau électronique n |
|
6. Bandes dénergie semi-conducteurs
métal : 1 e- de conduction par atome. BV. BC. E. E f. E. Niveau de Fermi métal semi- conducteur. La conductivité varie différemment pour les métaux et les |
|
Exercice n°1 : (8 points) Ici absorption de ? à partir du niveau n=2
Les orbitales atomiques ayant la même énergie sont dites dégénérées. Une couche électronique n de l'atome d'hydrogène a une énergie En dépendant uniquement |
|
Cours de Chimie Structure de la matière
Le deuxième chapitre est consacré à l'étude de la structure de l'atome Mise en évidence ; V.1 Relation entre le nombre d'onde et les niveaux d'énergie ... |
|
CHAPITRE I : STRUCTURE DE LA MATIERE
2. la vitesse de l'électron pour l'état fondamental de l'atome d'hydrogène. • 3. les énergies qui correspondent aux trois premiers niveaux ( en eV). |
|
Spectres et niveaux dénergie
spectre solaire et les niveaux d'énergie de l'atome d'Hydrogène). Pré- requis : • Savoir que la lumière blanche est composée de lumières colorées. |
|
Chapitre II : Quantification de lénergie
Si n= ? l'e- a quitté l'atome on dit que l'atome est ionisé. I-2-5 Absorption et émission d'énergie. A chaque orbite permise correspond un niveau |
Comment calculer le niveau d'énergie d'un atome ?
Quels sont les niveaux d'énergie d'un atome ?
. Quand il passe d'un niveau A à un niveau inférieur B, l'électron va émettre un photon d'énergie égale à ?E.
Comment trouver le niveau d'énergie ?
|
Chapitre 2 :Quantification de lénergie de latome dhydrogène
Chaque état possède une énergie invariante (quantification des niveaux d' énergie de l'hydrogène) Postulat optique : La transition entre deux états accessibles s' |
|
Hydrogénoı̈des et méthode de Slater
atomique de l'élément chimique et e la charge élémentaire) L'énergie de l' électron d'un hydrogénoïde est donnée par l'expression : ( ) = −13,6 où n est le |
|
Cours4pdf
Atomes I Atome à deux électrons électron 2 électron 11 12 12 noyau +Ze Au contraire, les orbitales de valence ont des niveaux d'énergie proches de la |
|
S COMMISSARIAT A LENERGIE ATOMIQUE 1970 SERVICE
Les rapports du COMMISSARIAT A L'ENERGIE ATOMIQUE sont, à partir du n° niveau de la photocathode du photomultiplicateur est + 0,5°C On peut suivre |
|
UE 3 : Physique Fiche de cours & QCM - Tutorat Associatif Toulousain
Découvert par Rutherford en 1911, le noyau atomique représente le cœur de l' atome Situé au Par convention, l'état fondamental est au niveau d'énergie 0 |
|
Exercices résolus de Chimie Physique - 3ème édition - Cours
Le niveau n ∞ est celui qui correspond à la séparation de l'électron et de son atome, qui devient un ion Le niveau énergétique correspondant à cet état est pris |
|
Nature corpusculaire de la lumière, leffet photoélectrique
arrivée permanente d'électrons au niveau de la cathode pour arracher un électron à un atome, il faut une certaine quantité d'énergie; • seuls les photons |
|
6 CO2 + 12 H2O C6H12O6 + 6 O2 + 6 H2O
Chapitre 1 : Energie et cellule vivante chloroplastes sont concentrés au niveau du parenchyme palissadique localisé à la face supérieure de la feuille ce qui |
NIVEAUX D’ENERGIE DE L’ATOME
niveaux d’énergie d’un atome : Ø Le niveau d’énergie le plus bas correspond à l’état le plus stable de l’atome : on l’appelle le niveau fondamental Ø Les autres niveaux sont appelés niveaux excités Etat ionisé Etats excités Etat fondamental E 1 E 2 E 3 E 4 E 5 E 6 E∞ E (eV)
Niveaux d’énergie de l’atome ------------------- Terminale S
- Une désexcitation est une transition électronique d’un niveau d’énergie E n à un niveau E P telle que E P < E n - Une ionisation correspond au passage d’un atome du niveau fondamental (de plus basse énergie) vers l’infini II Application à l’atome d’hydrogène : II 1 – Niveaux d’énergie: a– Expression A l’état
CHAPITRE VII NIVEAUX DÉNERGIE DES ATOMES À N ÉLECTRONS
L'énergie de "sortie" wi correspondant à l'arrachement d'un électron à un atome, et donnée par wi = h νi est ce que l'on appelle l'énergie d'ionisation de l'atome Dans le domaine visible ou UV, l'effet photoélectrique ne se produit en général que sur l'électron le moins lié d'un atome donné : nous verrons que l'emploi de photons
Les niveaux d’énergie - Le Site Web de Jeff OKeefe
Pour un atome avec plus d’un électron, le niveau d’énergie des sous-couches électroniques ne sont pas le même comme ils le sont pour l’hydrogène Remarquez que le motif des raies spectrales sont le même que celui des niveaux d’énergie Les nombres 1s, 2s, et d’autres représentent les sous-couches électroniques
41-101 Quantification de lnergie des atomes
• L’électron d’un atome d’hydrogène ne possède qu’un nombre limité d’états, chacun d’énergie invariante et bien déterminée Ces états sont appelés niveaux d’énergie ou état quantiques • L’émission ou l’absorption d’une onde électromagnétique correspond à une transition entre deux états quantiques
ATOMISTIQUE --- MP-Spé --- Structure électronique des atomes
— À chaque fonction d’onde ψn,l,m(r,t) est associée une énergie qui correspond au niveau d’énergie de l’électron correspondant Lorsqu’il existe plusieurs fonctions d’onde associées à un même niveau d’énergie, on dit que le niveau est dégénéré 2 3 1 Les 4 nombres quantiques caractérisant un électron dans un atome :
Chapitre 21 Deux siècles d’énergie
a Les flèhes représentent des hangements de niveau d’énergie de l’ato me b La flèche représente l’asorption d’un photon par l’atome c La flèche représente l’émission d’un photon par l’atome d Cet atome peut émettre ou a sorer des photons dont l’énergie est E = 2,71 eV 5
COURS D’ATOMISTIQUE - Internet Archive
3 - Absorption et émission d'énergie Un électron ne peut absorber ou libérer de l'énergie càd rayonner qu'en passant d'un niveau (orbite) à un autre La quantité d'énergie absorbée ou émise est égale à la différence d'énergie entre les deux niveaux (relation de Planck) : ∆E = ⏐E f - E i⏐= hν E f: état final E i: état initial
I Absorption et émission quantique
niveau d’énergie E 1 à un niveau d’énergie supérieur E 2, en lui apportant exactement le quantum d’énergie ∆E requis pour effectuer la transition Pour faire passer un atome de son état fondamental à un état excité, plusieurs possibilités existent : l'absorption d'un photon d'énergie donnée le passage d'un courant électrique
|
Quantification de l énergie des électrons dans les atomes - Eduscol
[PDF] Quantification de l 'énergie des électrons dans les atomes Eduscoleduscol education rnchimie chi gen dossiers quant atome pdf |
|
CHAPITRE VII NIVEAUX D ÉNERGIE DES ATOMES À N - UPMC
[PDF] CHAPITRE VII NIVEAUX D 'ÉNERGIE DES ATOMES À N UPMC edu upmc physique licence pf IMG pdf LIC pdf |
|
quantification des niveaux d énergie - Sciences Physiques ac
[PDF] quantification des niveaux d 'énergie Sciences Physiques ac physique ac orleans tours observer quantification energie pdf |
|
Les niveaux d énergie des atomes de numéro atomique - Hal
[PDF] Les niveaux d 'énergie des atomes de numéro atomique Hal hal inria docs ajp jphysrad pdf |
|
Diagramme énergétique de l atome d Hydrogène a) Etat ionisé et
[PDF] Diagramme énergétique de l 'atome d 'Hydrogène a) Etat ionisé et poly prepas cours%radioactivité%II%(fin) pdf |
|
Lumière et énergie - Sciences Mont Blanc
[PDF] Lumière et énergie Sciences Mont Blancmontblancsciences free premiere eS eS ch photon pdf |
|
Spectres et niveaux d énergie - Jardin des Sciences
[PDF] Spectres et niveaux d 'énergie Jardin des Sciencesjardin sciences unistra Spectres et niveaux d e nergie pdf |
|
Chapitre 5 QUANTIFICATION DES ÉNERGIES ATOMIQUES
[PDF] Chapitre QUANTIFICATION DES ÉNERGIES ATOMIQUES master p obspm phyquant annee LPGA PA pdf |
|
Leçon #8211; L atome d hydrogène - Learn Alberta
[PDF] Leçon L 'atome d 'hydrogène Learn Alberta learnalberta ca content sfp java atom lesson pdf |
|
L atome polyélectronique - CINaM
bien déterminée il est placé sur un niveau atomique Pour l 'hydrogène les valeurs propres de l 'énergie ne dépendent que de n Pour un atome quelconque les |
- niveaux d'énergie des électrons dans un atomes
- quantification de l'énergie d'un atome 1ere s
- les niveaux d'énergie pdf
- niveaux d'énergie de l'atome d'hydrogène
- calcul niveau d'énergie d'un atome
- niveau d'énergie exercice corrigé
- exercices corrigés sur les niveaux d'énergie pdf
- niveau d'énergie formule

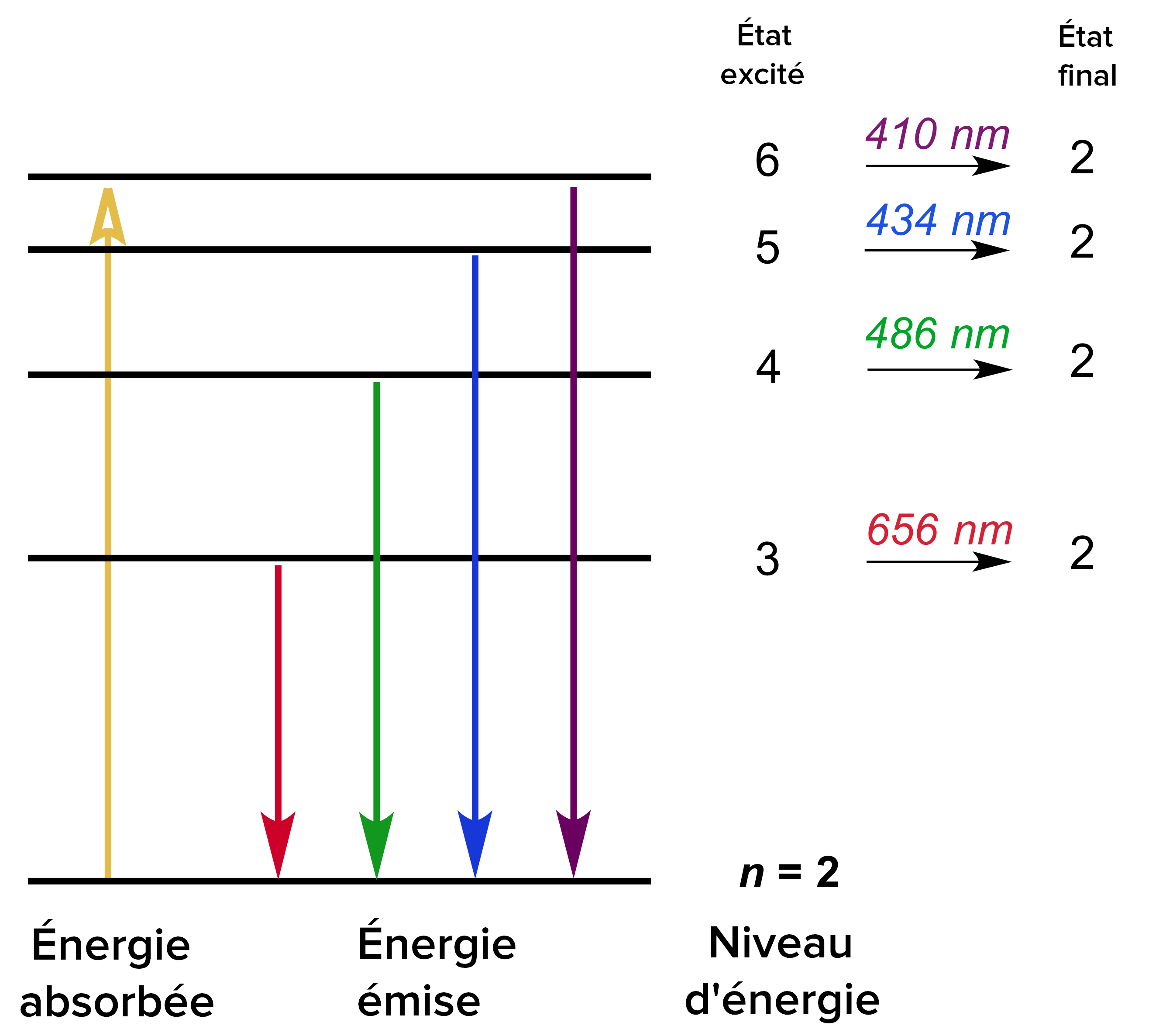
emc2 - Niveaux d'énergie de l'atome d'hydrogène - Emission et
Source:https://upload.wikimedia.org/wikipedia/commons/thumb/9/94/Energy_level_diagram-fr.svg/1200px-Energy_level_diagram-fr.svg.png
Niveau d'énergie — Wikipédia
Source:https://cdn.kastatic.org/ka-perseus-images/284680f3cfc3e6865da65171d8a72ccfd6c75a14.png
Modèle de Bohr de l'atome d'hydrogène (leçon)
Source: Khan Academy

Cours sur les niveaux d`énergie d`un atome en version pdf - E
Source:https://www.fichier-pdf.fr/2011/12/05/10-atome-de-bohr-2/preview-10-atome-de-bohr-2-1.jpg

10 Atome de Bohr par Änder - Fichier PDF
Source:https://s1.studylibfr.com/store/data/003170417_1-b311f2bc413981a054d79faec2ab3227.png

Télécharger le cours complet en pdf
Source:https://e.educlever.com/img/4/4/3/2/443270.jpg
niveau d'énergie exercice corrigé
exercices corriges photon - Picassciences
- exercices corrigés sur l'atome d'hydrogène
- niveau d'énergie formule
- niveau d'énergie exercice corrigé pdf
- spectre d'émission de l'atome d'hydrogène exercice
- exercice photon première s
- exercices corrigés interaction rayonnement matière pdf
- exercice niveau d'énergie 1s
- spectre d'émission de l'atome d'hydrogène pdf
niveau d'énergie formule
Quantification de l 'énergie des électrons dans les atomes - Eduscol
- quantification de l'énergie definition
- niveau d'énergie exercice corrigé
- niveaux d'énergie de l'atome d'hydrogène
- quantification de l'énergie 1ere s
- les niveaux d'énergie pdf
- exercices corrigés sur les niveaux d'énergie pdf
- energie ionisation hydrogène
- quelle est la valeur en ev du niveau d'énergie fondamental de l'ion hydrogénoïde li2+ (z = 3) ?
niveau d'expertise définition
Catégorisation et types d 'expertise Une étude empirique - Hal-SHS
niveau d'huile
Série 34 Voyants d 'huile - EMILE MAURIN
- voyant de niveau d'huile
- indicateur de niveau visuel
- bouchon indicateur de niveau d huile
- indicateur de niveau d'huile hydraulique
- voyant indicateur de niveau d'huile
- indicateur de niveau d'huile en laiton
- bouchon niveau huile compresseur
- indicateur de niveau ? colonne