|
Les acides et les bases
pH du sang = 740 4 On calcule les valeurs nécessaires a) On détermine la concentration en ions H3O+ [H3O+] = 10 −740 [H3O+] = 398 × 10 −8 mol/L b |
|
BACCALAURÉAT GÉNÉRAL PHYSIQUE-CHIMIE
30 mai 2023 · - partie 1 : Calcul des puissances développées par les cyclistes ; - partie 2 : Étude de la physiologie de l'effort et régulation du pH sanguin |
|
Chapitre Chimie N°4 : Les Acides et les Bases faibles en solution
en ions oxonium H3O* présent dans la solution par la relation : pH = -log [H₂O+] -> Remarques : [H3O+] = 10-PH Eau de mer 8 0 Sang Salive 7 35 7 0 Lait |
|
1 Calculer le pH de solutions dun acide faible HA (pKa = 375) aux
Calculer le pH d'une solution d'acide éthanoïque CH3COOH de concentration 0002 mol L-1 On donne: pKa (CH3COOH/CH3COO-) = 48 A : pH= 11 |
|
Cours et exercices de chimie des solutions
⇒ [H3O + ] = ⇒ pH = - log ( ) 8-7 Mélange de deux bases Le raisonnement adopté pour le calcul de pH des mélanges des acides sera le même dans le cas des |
|
PH dune solution aqueuse
2° - Calcul du pH : → La concentration en ions H+ est la quantité d'ions H+ [H3O + ] = 10 -pH mol L-1 exemple : * Il en résulte qu'une solution |
|
Chapitre 1 Acides et bases
— le pH final est déterminé par la concentration de solution titrante (prendre en compte un facteur de dilution entre 15 et 3 pour le calcul du pH final) |
|
Contrôle de léquilibre acido-basique
Le rapport sel alcalin (A-)/ acide faible (AH) est calculé en fonction de la constante de dissociation pKa et du pH par l'équation de Henderson-Hasselbalch : pH |
|
RÉACTIONS ACIDO-BASIQUES
Le pH et la concentration en ions oxonium H3O+ varient en sens inverse : lorsque [H3O+] augmente le pH de la solution diminue et inversement Ex : - si [H3O+] |
Comment calculer H3O+ avec Ho ?
Il faut calculer [H3O+] par la relation [H3O+]x[HO-]=10-14 d'ou [H3O+] = 10-14 [HO-] Puis, on applique la formule. -1.
Calculer le pH de chacune des solutions et préciser leur nature acide ou basique.Comment calculer le pH dans le sang ?
: on en déduit la formule du pH sanguin par l'équation d'Henderson- Hasselbach : pH = pKa + log ([Base] / [Acide]).
Comme pKaSg = 6,1, on obtient : pHSg = 6,1 + log ([HCO3 -] / [H2CO3]).
H2CO3 n'existe pas sous cette forme dans le sang : il est immédiatement dissous sous la forme : H2CO3 CO2 + H2O.Comment calculer le pH de H3O+ ?
Le pH d'une solution est lié à la concentration en quantité de matière d'ions oxonium.
Les relations entre le pH et la concentration en quantité de matière d'ions oxonium sont pH = –log[H3O+] et [H3O+] = 10–pH.L'état d'équilibre du à la réaction d'autoprotolyse de l'eau : 2 H2O Û H3O+ + OH- étant toujours atteint, si la concentration des ions H3O+ augmente, celle des ions OH- diminue de sorte que la relation Ke » [H3O+] [OH-] soit toujours vérifiée.
|
Contrôle du pH du sang
De cette activité résulte par ailleurs une production d'ions H3O+ et d'acides non négligeable largement suffisante pour faire descendre le pH sanguin à des |
|
Chapitre 1 Acides et bases
L?1 et comme indiqué dans la note pré- liminaire la concentration unitaire C0 est omise. Une solution aqueuse est dite : — neutre si son pH vaut 7 |
|
Mécanismes de régulation du pH sanguin
Pour montrer l'importance du rôle tampon imaginer une entrée d'acide chlorhydrique H3O+aq+Cl?aq de 1 |
|
Séance Chimie n°5 : Equilibres chimiques – Quotient de réaction
log [H3O+]éq. pKa1 = – log. + pH d'où : pH = pKa1 + log. 2) Calculer la valeur du rapport dans le sang artériel normal. Log. = pH – pKa1. |
|
Equilibre acidobasique
maintenir le pH du milieu extracellulaire à 740 pH = -log 10-7. pH = 7. Acide : cède des H+. Base : accepte des H+ ... Systèmes tampons sanguins. |
|
Terminale S – Partie 2 : Comprendre : Structure et transformation de
2. Influence de la production d'acide lactique sur le pH sanguin / 6pts. 2.1.+ Pour trouver la formule de l'ion lactate il faut enlever un proton H+ à. |
|
Sujet Felix Hoppe – Seyler Régulation du pH et fixation du
calculer la valeur du pH sanguin. de l'acidité et donc de la concentration en ions H3O+. Considérons un apport d'ions H3O+ de 20 mmol·L. ?1. |
|
FICHE ACIDO BASIQUE
[H+] tamponné par A- (tamponné par acides fermés). Résultats : (mEq/L d'ions H+/u de pH). Milieu fermé : Plasmatiques ( |
|
CORRECTION DES EXERCICES
C4_Réaction acide-base et pH. CORRECTION DES EXERCICES. Exercice 5 page 334 : 1. On utilise la formule pH = - log [H3O+]. On calcule : vinaigre : pH = 31 ;. |
|
Chimie analytique – Réactions acido-basiques :
et constitue une contrefaçon sanctionnée par les articles L.335-2 et suivants du Code de la propriété intellectuelle. CALCULS. ? pH = - log [H3O+] & [H3O+] |
| PH and H3O+ concentrations 2018notebook |
| Calculating pH and pOH worksheet - Everett Community College |
| Extra Practice: Acid and Base pH Calculations KEY |
| 4 Acid Base Chemistry - University of Texas at Austin |
| A GUIDE TO pH MEASUREMENT - Mettler Toledo |
| Searches related to ph sanguin H3O+ calcul filetype:pdf |
What is the pH of a solution of NaOH and HCl?
- pOH = -log[OH-] = -log(6.50 x 10-3) = 2.187 pH = 14.000 –pOH = 14.000 –2.187 = 11.813 4) -A solution is created by measuring 3.60 x 103moles of NaOH and 5.95 x 10-4moles of HCl into a container and then water is added until the final volume is 1.00 L.
How do you find the weight of HCl?
- Wt% HCl is first converted to molar concentration to determine the [H+].
. The weight of 1 liter of HCl is determined by multiplying the solution concentration (Wt%) by its specific gravity (SpGr) and by 1,000 (assuming that 1 liter of water weighs 1,000 grams).
What is the concentration of HCl in wt%?
- +Again, since the hydrogen ion concentration [H ] is equal to the molar concentration of HCl ([H+] = mol/L HCl), the concentration of HCl in Wt% can be determined as follows: (HCl mol/L)(36.47g/mol)(L/1,000g)(100%)/(SpGr) = Wt%
How do you measure the pH of foodstuffs?
- The qualitative determination of the pH value of foodstuffs is probably the oldest analysis method in the world.
. All foodstuffs are tested with the taste organs.
. Thereby some are noticed to be acidic and some to be alkaline.
. With modern pH electrodes these taste sensations can be measured in exact figures (see fig.
|
Contrôle du pH du sang
résulte par ailleurs une production d'ions H3O+ et d'acides non négligeable, largement suffisante pour faire descendre le pH sanguin à des valeurs rapidement incompatibles avec la valider par le calcul la valeur du pH normal du sang |
|
Examen du 28 mai 2009 - durée : 2 heures - lutesupmcfr
+ H3O+ Couple CH3CO2H/CH3CO2 - CH3CO2H: espèce acide NH4Cl NH4 2) Calculer le pH de chaque solution (la vérification des hypothèses n'est pas demandées) NaNO3 : c) En déduire le pH sanguin dans ces conditions |
|
FICHE ACIDO BASIQUE
Métabolisme Consomme sur place les H+, sans transport Calcul de l'excès de base fixe = défaut de concentration en acides fixes = distance verticale entre |
|
Chapitre 1 Acides et bases
acide si son pH est inférieur à 7, i e [H3O+]> 10−7 mol L−1 (à Voici par exemple l'alanine, de formule générale CH3 – CH(NH2)–COOH : CH3 – CH( NH3 Le plasma sanguin se comporte aussi comme un tampon : plusieurs mécanismes |
|
DÉSORDRES DE LÉQUILIBRE ACIDE-BASE - CUEN
14 sept 2018 · A Mesure du pH et de la gazométrie circulante sanguine ¢ h Acidémie (ou acidose décompensée) : pH sanguin < 7,38 (augmentation de [H+]) à TA plasmatique normal, la réponse rénale peut être évaluée par le calcul |
|
Séance Chimie n°3 : Equilibres chimiques
1) Donner la formule développée de l'acide lactique + H3O+ (aq) c Tracer le diagramme de prédominance du couple acide benzoïque / ion benzoate |
|
Tampons sanguins
pons sanguins d'assumer ce rôle et d'amortir les variations de pH au voisi- nage de la valeur 7,4 Définitions Les ions H+ associés `a l'acidité du CO2 sont dits acides volatils (il s'en produit environ 12 La formule de Henderson peut alors |
|
1 Réactions acido-basiques
[H3O+] et [HO-] désignent les valeurs des concentrations exprimées en mol L-1 3 main- tient le pH sanguin entre 7,35 et 7,45 ; En calculer la constante |
Chimie 8 : Titrages acido-basiques - AlloSchool
Comment varie le pH au cours du titrage ? 2 1 Ajout d'une solution de base Exploitons l' activitépréparatoire B, page 165 À l'aide d'un pH-mètre, on suit les variations du pH de la solution contenue dans le bécher lors de l'ajout de la solution de soude [Doc 3 La représentation graphique pH = f(VB) Doc 4 , d'allure croissante, fait
CHAP 13-ACT EXP Mesures de pH-CORRIGE - legtuxorg
D’où le pH : pH = 2 c) – Grace au pH que vous avez mesuré dans le 5 1 - Calculer la concentration noté [H3O + (aq)]f puis le nombre de moles d’ions oxonium nf(H3O + (aq)) dans l’état final - A l’aide du tableau d’avancement déterminer la valeur de xf - Calcul de la concentration en ions oxonium On a pH = 2 d’où : [H3O + (aq
Examen du 28 mai 2009 - durée : 2 heures - upmc
Exercice II: pH du sang et effort musculaire Le pH du sang est tamponné par le couple H 2CO 3/HCO 3- Dans le sang d’une personne au repos, les concentrations en HCO 3-et H 2CO 3 sont respectivement de C b = 0,0270 mol L-1 et C a = 0,0014 mol L-1 a) Que signifie le terme tamponné?
1 Calculer le pH de solutions d’un acide faible HA (pKa = 3
2 : En pH-métrie, l'unique condition pour qu'une solution aqueuse soit neutre est [H3O+] = 10-7 mol L-1 3 : Si les deux acidités d'un polyacide sont proches l’une de l’autre (ΔpK A < 2), seule la première
Séance Chimie n°3 : Equilibres chimiques
I pH du sang et maintien de sa valeur : Le sang est constitué d’un liquide plasmatique qui peut être assimilé à une solution aqueuse ionique dont le pH est quasiment constant et voisin de 7,4 De fortes fluctuations du pH nuiraient gravement à la santé Le pH d’un sang artériel « normal » est égal à 7,4 à 37°C
J¶©ä J äÈ ÃÓ Á%
Si pH > pKa, la forme déprotonée A- sera majoritaire Lors des variations de pH , les proportions des deux espè es varient mais la somme de leursconcentrations est constante Cette proportion est donnée par la formule : log ???? ???????? = pH − pKa Calcul du pH : -Acides forts : pH = - log [H30+] -Bases fortes : pH = 14 + log C
Fiche d exercices sur les acides, bases et pH (fiche n°11)
Fiche d’exercices sur les acides, bases et pH (fiche n°11) Remarque : Une correction succincte est proposée après les exercices Exercice 1 Deux élèves mesurent le pH d’un soda, ils trouvent un pH de 1 1) Nomme l’instrument que sert à mesurer le pH 2) Note le résultat de la mesure
QCMs Entrainement [UE11]
C) Avant même de faire un calcul, on sait que le pH de la solution est nécessairement entre 0 et 4,9 D) Avant même de faire un calcul, on sait que le pH de la solution est nécessairement entre 4,9 et 7 E) Aucune des propositions ci-dessus n’est exacte QCM 14 : PARMI LES PROPOSITIONS SUIVANTES CONCERNANT LE CALCUL DU PH DE CETTE SOLUTION,
|
Eléments de correction - Sciences Physiques ac-orleans-tours
[PDF] Eléments de correction Sciences Physiques ac orleans toursphysique ac orleans tours physique terminale Orleans TS COMPRENDRE correction pdf |
|
Chimie, Chapitre 1 Terminale S
[PDF] Chimie, Chapitre Terminale S lyc vinci st witz ac versailles ch reactions acido basiques el pdf |
|
Réaction chimique par échange de proton - Documents de physique
[PDF] Réaction chimique par échange de proton Documents de physique physiquechimie ts e monsite medias chap livre pdf |
|
15e #8211; pH du milieu biologique - Correction
[PDF] e pH du milieu biologique Correctiontspierrerouge e monsite c ts activitetamponcorrection pdf |
|
L EQUILIBRE ACIDE-BASE
[PDF] L 'EQUILIBRE ACIDE BASE md ucl ac be virtanes ac bs pdf |
|
réaction acido-basique ph et équilibre chimique - Free
[PDF] réaction acido basique ph et équilibre chimique Freecedric despax free physique chimie cours T cours PC pdf |
|
Les acides et les bases Corrigés des exercices
[PDF] Les acides et les bases Corrigés des exercicesbbiblio weebly les acides et les bases corrig des exercices pdf |
|
Terminale S_thème 2_Comprendre : Lois et modèles chapitre
[PDF] Terminale S thème Comprendre Lois et modèles chapitre sciences physiques cpge e monsite chp reaction chimique par echange de proton pdf |
|
exercice - Labolycée
[PDF] exercice Labolycéelabolycee Chimie Thema Chimie Dosages par titrages pdf |
|
Correction
) Lors d 'un effort physique, la concentration en dioxyde de carbone dissous dans le sang, au voisinage du muscle, augmente Comment devrait varier le pH du sang si il n 'y avait pas de régulation ? Calculer la constante d 'équilibre de la réaction + HO+ (aq) c Tracer le diagramme de prédominance du couple acide |
- la régulation du ph sanguin correction
- cours acide base terminale s pdf
- controle du ph du sang correction
- equilibre acido basique cours chimie
- le tampon bicarbonate du sang exercice
- chimie des solutions aqueuses pdf
- de l'hyperventilation à la syncope correction
- acide alpha aminé definition

Frottis sanguin \u0026 Formule leucocytaire*
Source:http://villemin.gerard.free.fr/Biologie/SangHer_fichiers/image045.jpg
groupes sanguins et hérédité
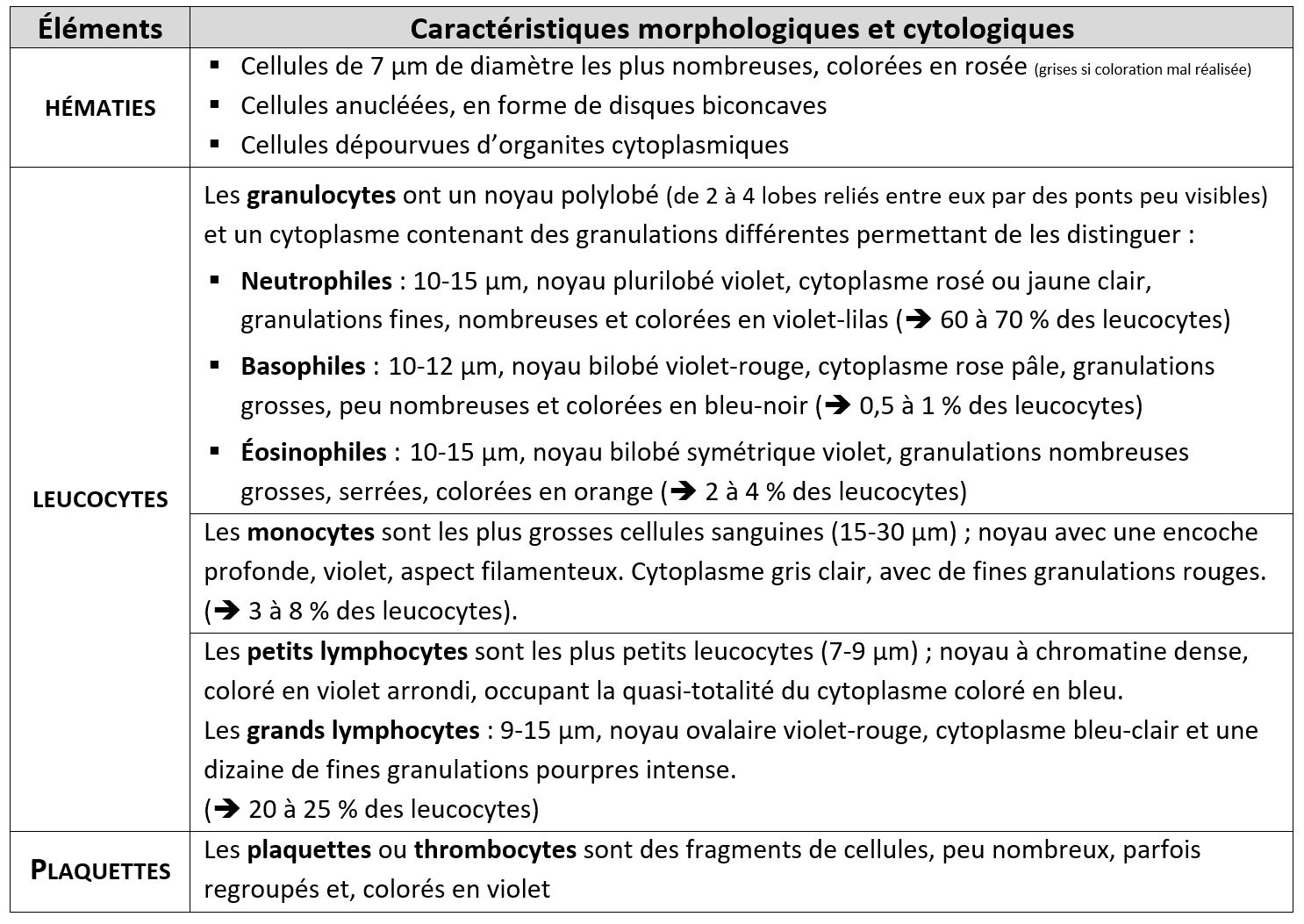
Source:http://droguet-sebastien.e-monsite.com/medias/images/tableau-morphologie-cellules.jpg

Frottis sanguin \u0026 Formule leucocytaire*
Source:http://villemin.gerard.free.fr/Biologie/SangHer_fichiers/image034.jpg

groupes sanguins et hérédité
Source:http://slideplayer.fr/slide/4147277/13/images/1/NUMERATION+FORMULE+SANGUINE.jpg

NUMERATION FORMULE SANGUINE - ppt video online télécharger
Source:https://www.fichier-pdf.fr/2020/06/22/comprendre---la-cratinine---pdf/preview-comprendre---la-cratinine---pdf-1.jpg

COMPRENDRE - LA CRÉATININE - PDF par Salim Djelouat - Fichier PDF
Source:http://droguet-sebastien.e-monsite.com/medias/images/01.jpg
ph suc intestinal
l 'appareil digestif - Infirmierscom
- anatomie et physiologie du système digestif pdf
- cours appareil digestif aide soignant
- suc intestinal acide ou basique
- sécrétion digestive définition
- anatomie et physiologie de l'appareil digestif ppt
- suc intestinal définition
- regulation hormonale de la digestion
- physiopathologie digestive pdf
pH, acides; bases
Révisions sur les acides et les bases - Nicole Cortial
- les acides et les bases
- acide fort
- acide base cours
- acide fort base forte
- acide base cours pdf
- acides et bases en solution aqueuse exercices corrigés
- acide base ph
- acide fort pka
Ph-Ch Masse de Cuivre dans une pièce
concours général des lycées #8212 session 2015 - mediaeduscol
phaedra act 2 scene 5
phèdre, tragédie - Théâtre classique
- phèdre racine pdf
- phedre racine piece complete
- phèdre racine résumé
- résumé de phèdre court
- phèdre analyse pdf
- phèdre acte 1 scène 3 analyse
- phèdre racine analyse
- phèdre racine résumé par acte