|
B) Fonctionnement de la pile Daniell : c) Réaction aux électrodes
Au cours du fontionnement de la pile: □La masse de l'électrode de zinc diminue elle se consomme ceci est due à l'oxydation du zinc selon la demi-équation: |
|
Oxydo-réduction et Piles électrochimiques SMPC2 fsr 2015
On considère une pile constituée d'une lame de zinc plongée dans une On a oxydation à l'anode (fer) et réduction à la cathode (Cuivre) Ceci permet d |
|
TS2 Piles électrochimiques EXERCICE n°1 : Pile cadmium-argent
EXERCICE n°3 : Réalisation d'une pile zinc–fer Pour réaliser une pile zinc-fer le laborantin fournit : – une lame de fer de masse m1= 710 g ; – une lame |
|
04
Les électrons sont donc libérés par la réaction Zn → Zn + 2 Le zinc est oxydé : l'électrode de droite est donc l'anode Les ions Ag sont réduits selon Ag + |
|
PILES DU TYPE PILE DANIELL Chapitre 7
Introduire dans le premier une lame de zinc et dans le second une tige de fer toutes les deux bien décapées Relier les deux demi- piles par un pont salin III/ |
|
10pilespdf
La pile Daniell (ou pile cuivre-zinc) est constituée de deux demi- piles : l'une formée d'une plaque de cuivre plongée dans une solu- tion de sulfate de cuivre |
|
Piles électrochimiques
- Plonger dans le bécher une lame de zinc et une lame de cuivre préalablement polies avec du papier émeri et rincées à l'eau - Attendre une minute et observer |
|
Exercice 1 : une pile zinc-fer
DM 17 : les piles-Correction Exercice 1 : une pile zinc-fer Soit une pile zinc-fer qui met en jeu les couples Zn2+ (aq) / Zn(s) et Fe2+ (aq) / Fe(s) Cette |
La pile est composée de deux électrodes – un pôle positif (ou cathode) et un pôle négatif (ou anode) – plongées dans une solution faisant office de conducteur.
Lorsque ces électrodes sont reliées par un fil conducteur à un consommateur électrique, une ampoule par exemple, cela ferme le circuit.
Quelle est la polarité de la pile ?
On détermine, à partir des sens dans lesquels se déroulent les demi-équations électroniques, la polarité de la pile sachant que : Le pôle négatif est celui qui libère les électrons.
Le pôle positif est celui qui capte les électrons.
Pourquoi le zinc est plus réducteur que le fer ?
Un atome de fer ne peut pas céder 2 électrons à un ion zinc Zn2+.
Seul le zinc a agi comme réducteur.
On dit que le zinc est plus réducteur que le fer.
|
Exercice 1 : une pile zinc-fer
DM 17 : les piles-Correction. Exercice 1 : une pile zinc-fer. Soit une pile zinc-fer qui met en jeu les couples Zn2+. (aq) / Zn(s) et Fe2+. (aq) / Fe(s). |
|
Chapitre 4 :La corrosion
On considère donc une limite pour laquelle il y aurait L/mol1 de fer oxydé Le zinc métal n'a pas de domaine commun avec l'eau ... A) Piles de corrosion. |
|
La corrosion humide
On forme ainsi une pile appelée pile de corrosion. Magnésium Zinc Aluminium Fer Plomb Etain Nickel Cuivre Acier Argent Titane Or Platine. |
|
Étude de la corrosion dans lagar-agar
Corrosion laboratoire |
|
Étude de la corrosion dans lagar-agar
Corrosion laboratoire |
|
TD3: Corrosion et moyens de protection (correction)
La pièce en zinc joue le rôle negative de cette pile qui est constitue l'anode. La partie en fer joue le rôle de cathode sera le siège d'une réaction de |
|
BREVET DE TECHNICIEN SUPERIEUR TRAITEMENTS DES
de zinc sert à protéger le fer et les aciers de la corrosion). Exercice 1 - Etude thermodynamique – 4 L'association fer-zinc est assimilable à une pile. |
|
TS2 Piles électrochimiques. EXERCICE n°1 : Pile cadmium-argent
a) Écrire l'équation chimique de la réaction entre le zinc métallique et les ions fer (II). b) Calculer te quotient de réaction initial Qui. c) En déduire le |
|
Piles électrochimiques
cuivre 0.1 mol/L et 20 mL de sulfate de zinc 0.1 mol/L. Partie 2 : Echange indirect d'électrons – Réalisation d'une pile (pile de. Daniell). |
|
Les piles et loxydo-réduction :
2 - Indiquer le signe des pôles de la pile formée ainsi que le sens de passage du courant. Le couple du fer est oxydant vis à vis de celui du cuivre (. |
|
Chapitre 10 : LES PILES
DM 17 : les piles-Correction Exercice 1 : une pile zinc-fer Soit une pile zinc-fer qui met en jeu les couples Zn2+ (aq) / Zn(s) et Fe2+ (aq) / Fe(s) Cette pile |
|
TS2 Piles électrochimiques EXERCICE n°1 : Pile cadmium-argent
Couples Fe2+(aq)/Fe(s) ; Zn2+(aq)/Zn(s) • Constante d'équilibre de la réaction entre le zinc métal et Les ions fer (II) : K = 6,5 ×1010 |
|
TD1 – Léquilibre rédox - Chamilo
à l'état de sulfate de fer (II) (FeSO4 totalement dissocié en Fe 2+ la demi-pile ( 1) constituée d'une électrode de zinc Zn plongée dans une solution aqueuse |
|
STOCKAGE DE LÉNERGIE ÉLECTRIQUE : LES PILES - Mediachimie
Activité expérimentale Fonctionnement de la pile électrique Compétences Considérons les couples oxydant/réducteur Zn2+(aq) / Zn(s) et Cu2+(aq) /Cu(s) |
|
10-Les piles électrochimiques - Physagreg
Il y a eu un transfert d'électrons direct entre les atomes de zinc de la lame et les ions Nous allons nous intéresser à la pile Daniell (pile Cu-Zn vue dans le |
|
Thème : MATERIAUX - Physique et Chimie - Académie de Lyon
Zn 2+ (aq) Ion hexacyanoferrate(III) [Fe(CN)6]3- HO - (aq) phénolphtaléine → Analyser une pile constituée par l'association fer – zinc de la seconde |
|
Chapitre 4 :La corrosion
On considère donc une limite pour laquelle il y aurait L/mol1 de fer oxydé, Le zinc métal n'a pas de domaine commun avec l'eau A) Piles de corrosion |
|
Oxydo-réduction et pile : commentaires scientifiques décrivant les
de la pile, appelé également force électromotrice (f e m ) Mais que Le potentiel standard de réduction de l'électrode de zinc G = - n F E = - n F E° + RT ln Q |
|
Chimie 12e année - Manitoba Education
un disque de zinc sur le dessous de la pile avec un papier filtre trempé dans une La galvanisation est un procédé où le fer est recouvert d'une couche de zinc |
|
04 - Étude dune pile Ag Zn - Chimie - PCSI
Attention : les deux volumes sont différents, il faut impérativement faire le bilan de matière en quantité de matière et non pas en concentrations La réaction évolue |
Palmeton Zinc Pile Case Study - US EPA
Palmerton Zinc Pile, Palmerton, Carbon County, Pennsylvania, Superfund Case Study 3 ECOLOGICAL REVITALIZATION OF CONTAMINATED SITES CASE STUDY on the adjacent Blue Mountain Process residue and other plant wastes were disposed of in a cinder bank, which is a 2 5-mile, 255-acre waste pile located behind the east smelter at the base of Blue Mountain
CoatingSheet PileStructures: AnOverview
nent sheet pile structures USACE also specifies an epoxy zinc-rich primer for marine applications The nominal two-coat thickness of CTE is 18 mils USACE also allows the use of two- and three-coat epoxy polyamide systems on sheet pile Polyamide systems may also be enhanced by application over an epoxy zinc-rich primer 3 Other coating
FINAL REPORT EVALUATION OF ANODES FOR GALVANIC CATHODIC
One uses expanded zinc mesh, which is secured within a cement grout/fiberglass jacket system that wraps around the piles to be protected 7 In effect, this system is a combination of the conventional grout jacket, which would restore any loss in the cross section of a concrete pile and then some, and galvanic CP, which would prevent steel corrosion
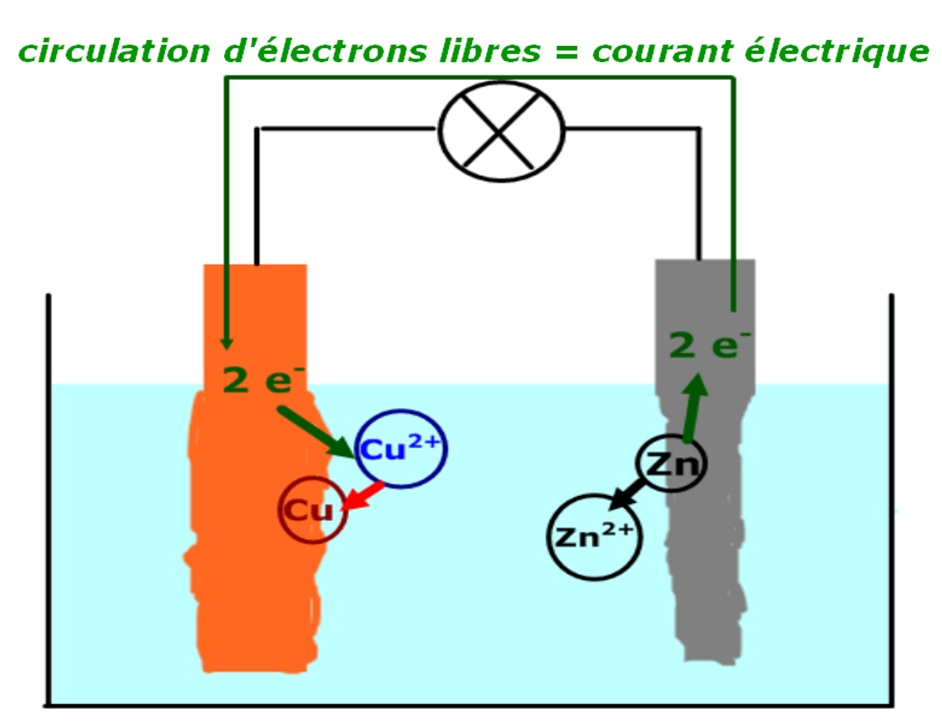
1) La pile Daniell : a)Description
de zinc (Les électrons circulent alors dans ce circuit extérieur de la plaque de zinc vers la plaque de cuivre) La plaque de cuivre qui représente le pôle positif de la pile s'appelle: la cathode La plaque de zinc qui représente le pôle négatif de la pile s'appelle l'anode c) Réaction aux électrodes: Au cours du fontionnement de la
FDOT Cathodic Protection Practices in floridappt
expanded zinc mesh anode jacket sacrificial c p jacket is placed around the pile and connected directly to the reinforcement without an external power supply the zinc mesh anode is pre-installed inside the form to provide an annular space of 50 mm which is later filled with mortar
1S CH20 TP PILES ET OXYDOREDUCTION corrige
I / PILE DANIELL On réalise une pile à l’aide d’une plaque de cuivre dans une solution de sulfate de cuivre et une plaque de zinc dans une solu-tion de sulfate de fer reliés par un pont salin 1°) La tension indiquée par les voltmètre est U= 1 05 V Les dispositif est un générateur qui fournit une
PILE ÉLECTROCHIMIQUE ET ÉNERGIE CHIMIQUE
1 - Lors de l'utilisation de cette pile, le zinc et les ions cuivre disparaissent 2 - Le métal cuivre et les ions zinc se forment lors du fonctionnement de la pile 3 - En introduisant de la poudre de zinc dans un tube à essai contenant une solution de sulfate de cuivre, la transformation chimique est obtenue différemment
1S CH20 TP PILES ET OXYDOREDUCTION bis
I / PILE DE DANIELL Cuivre-Zinc Réaliser le montage suivant : dans un bécher A, introduire 50 mL d’une solution de Zinc, (Zn 2+ +SO 4 2-), de concentration C=0 10 mol L-1 et une plaque de zinc décapée munie d’une pince crocodile Dans un bécher B, introduire 50 mL d’une solution de Cuivre II, (Cu 2+ +SO 4
Engineering Design Manual - Helical Anchors Inc
Page 4 EDM Rev 02 ©2014, Helical Anchors Inc Definition of Terms Resistance - A force developed in opposition to a load applied to a structural system Capacity – The maximum resistance a system can mobilize; usually used in relation to
This machine has been engineered to our own rigid safety and
13 9900081 nut #8-32 keps zinc plate 2 14 1572421 anchor-spring 1 15 7802073 anchor-spring 1 16 4721035 screw-#8-18 x 38-lgm 1 17 7802024 delivery pan 1
|
Chapitre 10 : LES PILES
[PDF] Chapitre LES PILESnputhinier free DM TS DM corrige pdf |
|
Exercices de révision- Oxydo-réduction et Piles - FSR
[PDF] Exercices de révision Oxydo réduction et Piles FSR fsr ac ma Oxydo reduction%et%Piles%electrochimiques%SMPC%fsr |
|
Oxydo-réduction et corrosion
[PDF] Oxydo réduction et corrosionzim web free Chap bts pdf |
|
Piles électrochimiques et potentiel d oxydoréduction
[PDF] Piles électrochimiques et potentiel d 'oxydoréduction esffm S Chapitre Potentiel d oxydoreduction pdf |
|
Corrigés des exercices
[PDF] Corrigés des exerciceszerrouki free Doc corrchi pdf |
|
Chap4 Pile électrochimique et énergie chimique
[PDF] Chap Pile électrochimique et énergie chimique ac grenoble college rostand la chimie chap pdf |
|
Pile cadmium-argent 2 Ag+
[PDF] Pile cadmium argent Ag+bremond bernard free gestclasse documents Cexopiles pdf |
|
Constitution d une pile - L Etudiant
[PDF] Constitution d 'une pile L 'Etudiant letudiant fiche defibac constitution d une pile |
|
Corrosion et anode sacrificielle - MChristian MARIAUD
[PDF] Corrosion et anode sacrificielle M Christian MARIAUDchristian mariaud pagesperso orange Corrosion et anode sacrificielle pdf |
|
TD1 #8211; L équilibre rédox - Chamilo
? l 'état de sulfate de fer (II) (FeSO totalement dissocié en Fe + la demi pile () constituée d 'une électrode de zinc Zn plongée dans une solution aqueuse |
- pile fer cuivre
- pile daniell exercice corrigé pdf
- exercice pile oxydoreduction 1ere s
- calcul capacité pile
- calcul fem pile
- notation pile électrochimique
- exercices corrigés sur les piles électrochimiques pdf
- pile electrochimique exercices corrigés pdf

Les piles et les accumulateurs - Maxicours
Source:https://docplayer.fr/docs-images/41/22620338/images/page_8.jpg
CHAPITRE 05 LES PILES - PDF Free Download
Source:http://pccollege.toile-libre.org/wp-content/uploads/2013/02/pilecuznbilan.jpg

Chapitre VI - Les piles - Physique-Chimie au Collège
Source:https://e.educlever.com/img/3/8/9/6/389630.jpg

Les piles et les accumulateurs - Maxicours
Source:https://upload.wikimedia.org/wikipedia/commons/3/3b/Electrochemical_element_with_salt_bridge.png

Pont salin — Wikipédia
Source:https://docplayer.fr/docs-images/41/22620338/images/page_5.jpg

CHAPITRE 05 LES PILES - PDF Free Download
Source:https://www.f-legrand.fr/scidoc/figures/sciphys/electrochim/piles/figF1.png
pile ou face simulation
PILE OU FACE - Maths-et-tiques
- algorithme pile ou face algobox
- pile ou face s'telle pdf
- algorithme probabilité pile ou face
- simulation d'un lancer de dé avec excel
- simulation pile ou face excel
- exercice probabilité pile ou face
Pile usagée
Les piles électrochimiques
- pile electrochimique 3ème
- pile électrochimique définition
- pile électrochimique pdf
- pile électrochimique cuivre fer
- pile électrochimique zinc cuivre
- pile électrochimique wikipedia
- pile electrochimique 3ème exercices
- pile electrochimique exercices corrigés
pilotage pédagogique définition
Culture de l 'évaluation et pilotage pédagogique
- piloter un établissement scolaire
- esenesr
pilote de guerre saint exupéry brevet
épreuve de français - mediaeduscoleducationfr
- pensez vous qu'on puisse faire preuve de solidarité dans une situation difficile correction
- pilote de guerre saint exupéry résumé
- peut on encore faire preuve de solidarité dans une situation difficile
- dnb pondichéry 2014 français
- redaction brevet pondichery 2017
- correction brevet français pondichéry 2017
- corrigé dnb français pondichéry 2014
- correction francais pondichery 2017