acide base cours pdf
|
Fiche de révisions sur les acides et les bases
Pour les couples acide / base on définit une constante d’acidité K A [acide] [H O ][base] K 3 A + = ou [acide] [base] pH =pK A +log Conséquence: pH = - log [ H 3 O + pK A = - log K A] [ acide ] > [ base ] [ base ] > [ acide ] 1°) Solution d’acide fort (AH) de concentration molaire Ca pH =−logCa |
|
Chapitre 1 : Les transformations acide-base
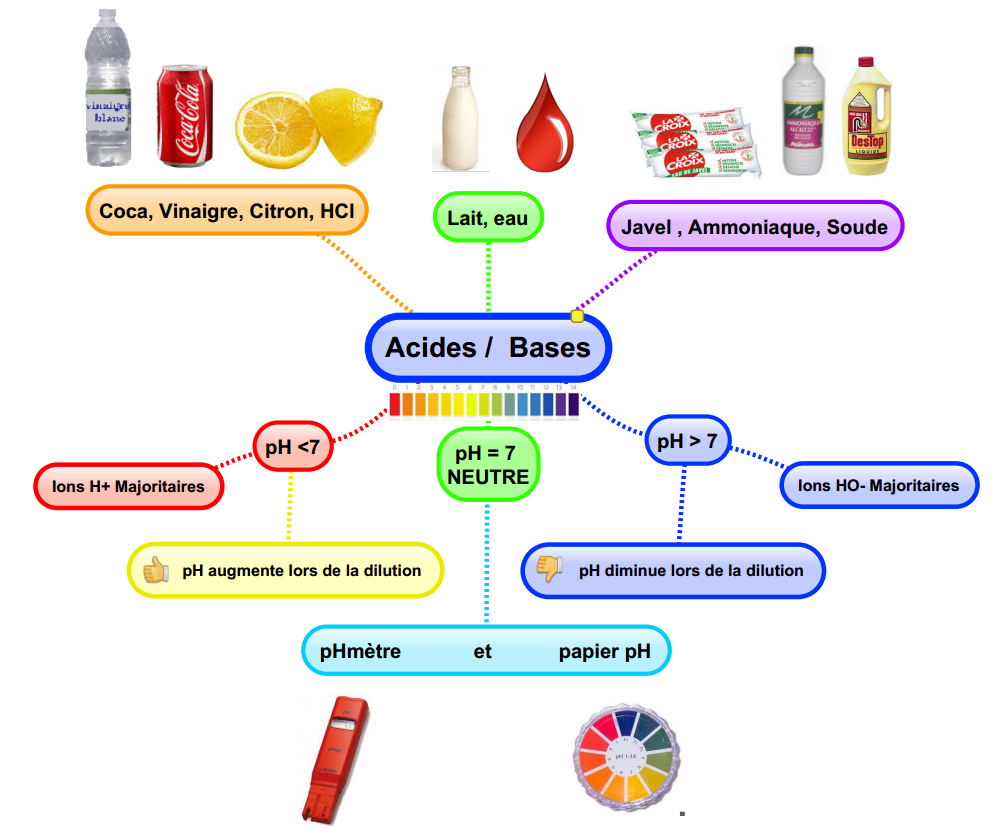
2 2 Mesure du pH : Le pH se mesure avec un indicateur coloré ( à quelques unités près) avec un papier pH ( à 1 unité près) ou avec un pH-mètre ( à 005 unité près) Remarque : Un pH-mètre doit être au préalable étalonné avec 2 solutions étalons Milieu basique ou alcalin [H3O +] < [HO –] Milieu neutre |
|
Chap TS acide-base
CH3COOH + NH3 = CH3COO- + NH4 + 2) Couples acide-base : L’acide et sa base conjuguée forme une couple acide-base Exemples : CH3COOH/CH3COO- L’acide éthanoïque et sa base conjuguée l’ionhanoate ét Ou NH4 +/NH3 l’ammoniac et son acide conjugué l’ion ammonium Remarque : on écrit toujours l’espèce acide à gauch e et la base |
|
Chapitre 1 Acides et bases
Une solution aqueuse est dite : — neutre si son pH vaut 7 i e [H3O+] 7 1 = 10 mol:L (à 25 C) ; — acide si son pH est inférieur à 7 i e [H3O+] > 10 7 mol:L 1 (à 25 C) ; — basique si son pH est supérieur à 7 i e [H3O+] < 10 7 mol:L 1 (à 25 C) Quelques exemples : Acide Neutre |
|
LES REACTIONS ACIDE-BASE 1 Le pH
Ces deux espèces appartiennent aux couples acide/base suivants : CH3COOH/CH3COO− et H2O/HO− On a les demi-équations acide/base suivantes : CH3COOH = CH3COO− + H+ HO− + H+ = H2O On additionne les demi-équations (1) et (2) et on obtient la réaction acide-base suivante : CH3COOH + HO− CH3COO− + H2O |
|
Semestre 2 – Chapitre 2 : Réactions acido-basiques
Une réaction acide-base est une réaction d'échange d'ion H+ entre un donneur de H+ (acide) et un accepteur d'ion H+ (base) Exemple : Écrire la réaction entre l'ammoniac et l'acide acétique puis entre l'acide phosphorique et la soude |
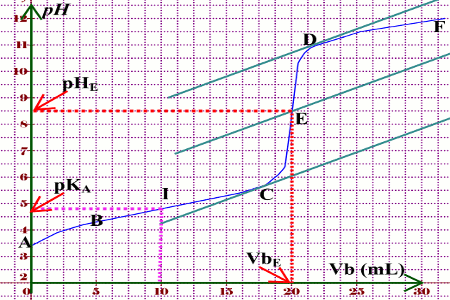
Quelle est l'équivalence du dosage d'un acide faible par une base forte ?
Remarque : A l'équivalence du dosage d'un acide faible par une base forte le pH noté pHE est supérieur à 7,0. En effet, à l’équivalnce, il y a présence de l’ion CH3COO- qui est une espèce basique. la demi équivalence, l'acide CH3COOH et sa base conjuguée CH3COO- sont présents en quantités égales dans le mélange.
Quels sont les différents types d’acides chimiques ?
Exemples : CH3COOH/CH3COO- L’acide éthanoïque et sa base conjuguée l’ion hanoate ét Ou NH4 +/NH3 l’ammoniac et son acide conjugué l’ion ammonium Remarque : on écrit toujours l’espèce acide à gauch e et la base à droite. Comme l’eau est une espèce chimique qui peut être oit s acide soit basique, c’est un ampholyte.
Comment calculer la prédominance d'une espèce acido-basique ?
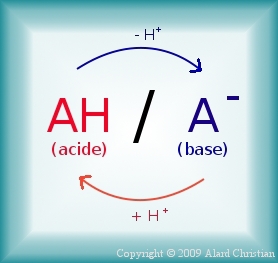
Un diagramme de prédominance indique en fonction du pH l'espèce acido-basique majoritaire. Pour le couple AH/A-, établir l'expression du pH en fonction du pKa et des concentrations des différentes espèces. pH = pKa+log [ AH ] On considère qu'une espèce est prédominante si sa concentration est au moins dix fois supérieure à celle des autres espèces.
2- Réactions acido-basiques :
Une réaction acide-base est une réaction d'échange d'ion H+ entre un donneur de H+ (acide) et un accepteur d'ion H+ (base). Exemple : Écrire la réaction entre l'ammoniac et l'acide acétique, puis entre l'acide phosphorique et la soude. f2school.com
3- L'eau : une espèce amphotère :
Expliquer pourquoi l'eau est une espèce amphotère. Écrire la réaction acide-base associée aux couples de l'eau. Quel nom porte cet équilibre ? Quelle est la constante d'équilibre associée à cette réaction ? f2school.com
1- Méthode de la réaction prépondérante :
Positionnement du problème : On introduit une ou plusieurs espèce(s) chimique(s) ayant des propriétés acido-basiques en solution aqueuse. On chercher à connaître les concentrations de toutes les espèces à l'équilibre, en particulier celle de H3O+. Une première méthode consiste à écrire les équations liant les concentrations à l'équilibre : Une cons
IV- Solutions tampon :
Rappeler ce qu'est une solution tampon. Un solution tampon est généralement réalisée en mélangeant un acide et sa base conjuguée en proportions égales. Quel est le pH imposé par le tampon en fonction du pKa du couple utilisé ? f2school.com
Semestre 2 – Chapitre 2 : Réactions acido-basiques
Les équilibres acido-basiques s'inscrivent dans la plus vaste problématique des équilibres chimiques, abordés au premier semestre. Le phénomène d'acido-basicité est important, par exemple dans l'organisme humain où des systèmes complexes contrôlent l'acidité du sang. Les acides et les bases sont en outre importants dans l'industrie : la grande quan
Définitions :
Rappeler la définition d'un acide fort, acide faible, base forte, base faible. Acide fort : acide qui réagit totalement avec l'eau. L'espèce AH n'existe pas dans l'eau. Base forte : base qui réagit totalement avec l'eau, la base A- n'existe pas dans l'eau. Acide faible : acide qui réagit partiellement dans l'eau, l'espèce AH existe dans l'eau, la r
K b=[ BH+][HO−]
[B ]c° b=[ → K Acide][ HO−] [base] d- Rappeler l'expression du pKa, par analogie en déduire l'expression de pKB. f2school.com
1- Méthode de la réaction prépondérante :
Positionnement du problème : On introduit une ou plusieurs espèce(s) chimique(s) ayant des propriétés acido-basiques en solution aqueuse. On chercher à connaître les concentrations de toutes les espèces à l'équilibre, en particulier celle de H3O+. Une première méthode consiste à écrire les équations liant les concentrations à l'équilibre : Une cons
IV- Solutions tampon :
a- Rappeler ce qu'est une solution tampon. Une solution tampon est une solution dont le pH est peu influencé par un apport extérieur de constituants acido-basiques ou par la dilution. b- Un solution tampon est généralement réalisée en mélangeant un acide et sa base conjuguée en proportions égales. Quel est le pH imposé par le tampon en fonction du
|
Chapitre 1 Acides et bases
On peut par exemple identifier un composé dans une solution de concentration connue en mesurant le ou des pKa au cours d'un dosage acido-basique. Une autre |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
Force des acides et des bases. 1.5. Constantes d'acidité et de basicité. 1.6. Coefficient de dissociation d'un acide faible : 2. CALCUL DE PH DES SOLUTIONS |
|
Cours de chimie en solution Les acides et les bases
Acides et bases. Dr. Ouksel. 2. II.1. Définition. Selon la théorie de Brönsted (1923) : - Un acide est une espèce chimique (molécule ou ion) capable de |
|
Fiche de révisions sur les acides et les bases
donc la base la plus forte dans l'eau. Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et. 14. 10. |
|
Chap TS acide-base
Réactions Acide-Base. I. définition du pH. L'acidité d'une solution est mesurée par rapport à l'espèce ionique H3O. +. l'ion oxonium ou hydronium. |
|
Cours de chimie en solution Les acides et les bases
couple acide/base. Selon la théorie de Lewis (1875) : - Un acide est une espèce chimique dont un des atomes la constituant possède une. |
|
Item 265 - DÉSORDRES DE LÉQUILIBRE ACIDE-BASE
Sep 14 2018 Au cours de l'hypercapnie chronique (acidose respiratoire chronique) la réabsorption des bicarbonates est augmentée de façon appropriée limitant ... |
|
COURS-Acide-Base.pdf
Les acides et les bases sont aussi très présents dans l'alimentation dans les médicaments |
|
Cours de Résidanat Sujet : 68
Cours commun de Résidanat Aout 2020. Sujet 68 : Troubles acido- A tout acide correspond une base conjuguée et vice versa. La relation entre les deux ... |
|
Chapitre II : Les acides et les bases CHIMIE II
Cours de Chimie II-L1 Cet équilibre chimique correspond à l'échange d'un proton entre l'acide AH et la base A ... conjugué (ou forme acide) de la base A. |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
Couple acide-base conjugués 1 4 Force des acides et des bases 1 5 Constantes d'acidité et de basicité 1 6 Coefficient de dissociation d'un acide faible |
|
Révisions sur les acides et les bases - Nicole Cortial
donc la base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et 14 10 |
|
Les acides et bases en solution aqueuse - Groupe Transition
distribuer gratuitement un ou plusieurs fichiers PDF ou ZIP complets et sans modification Les concepts d'acide et de base ont évolué au cours des siècles |
|
R E A C T I O N S A C I D O – B A S I Q U E S
I – LES COUPLES ACIDE-BASE 1-1 Ionisation des composés moléculaires dans l'eau Nous savons, depuis le cours précédent, que les composés ioniques, |
|
Chapitre 1 Acides et bases
Deux espèces chimiques AH et A– forment un couple acide/base si et seulement si mesurant le ou des pKa au cours d'un dosage acido-basique Une autre |
|
Chap TS acide-base
Réactions Acide-Base I définition du pH L'acidité d'une solution est mesurée par rapport à l'espèce ionique H3O + , l'ion oxonium ou hydronium Le pH |
|
Cours 5 - Equilibres Acido-basiques
Transfert de protons Objectifs : Définir un couple acide/base Exprimer une constante d'acidité K A /pK A Savoir calculer le pH d'une solution acide |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
1 Transformations chimiques en solution aqueuse Chapitre SA1_PSI : Réactions acide-‐base Cours de chimie de seconde période de PCSI PSI |
|
PH et pKa - Eli Zysman-Colman
choisir le “bon acide” ou la “bonne base” Par exemple lors de l'acétylation de la 4-bromo-aniline: Br NH2 Acide 4 Table de pKa http://evans harvard edu/ pdf /evans_pKa_table pdf Tables de pKa de vos notes de cours Keq = ? Formule |