acide faible ou fort
|
Fiche de révisions sur les acides et les bases
Dans l’eau l’acide le plus fort est donc l’ion hydronium H 3 O + TOUTES les bases fortes sont aussi fortes les unes que les autres dans l’eau L’ion hydroxyde OH − est donc la base la plus forte dans l’eau Les couples acide faible / base faible ont tous des constantes d’acidité comprises entre 1 et 10 − 14 |
|
§ 7 (suite) Calcul du pH de solutions
l’approximation lorsque pour un acide faible pc < pK a – 1 Pour une base faible la condition préliminaire est pc < pK b –1 On vérifiera a posteriori que l’approximation était justifiée en calculant les valeurs de [A–] et [BH+] pour respectivement le cas d’un acide faible ou d’une base faible |
|
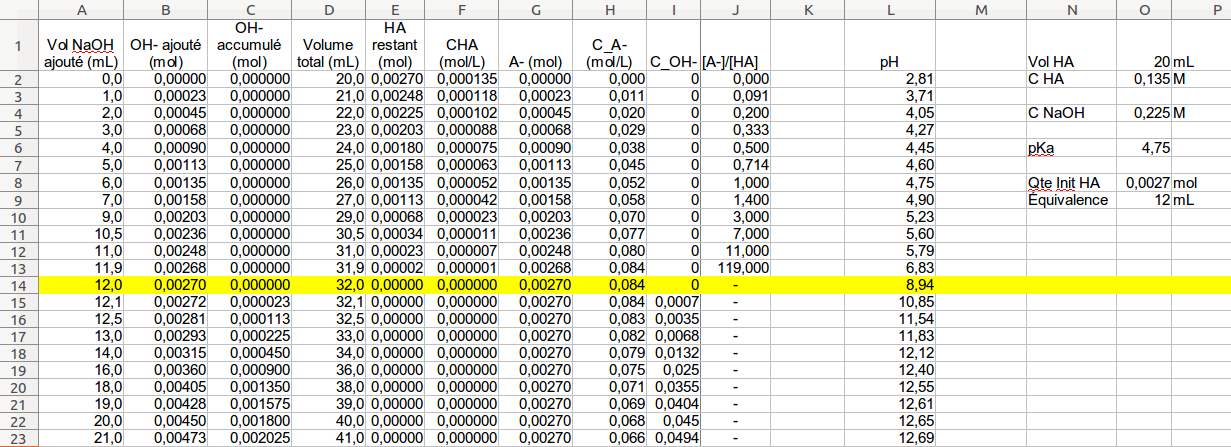
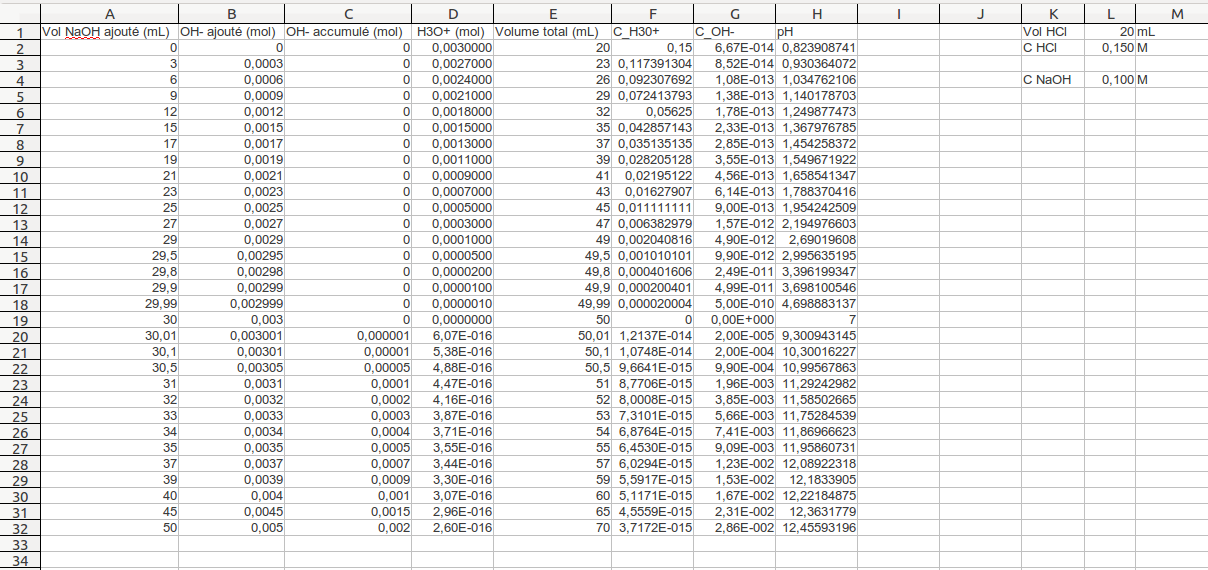
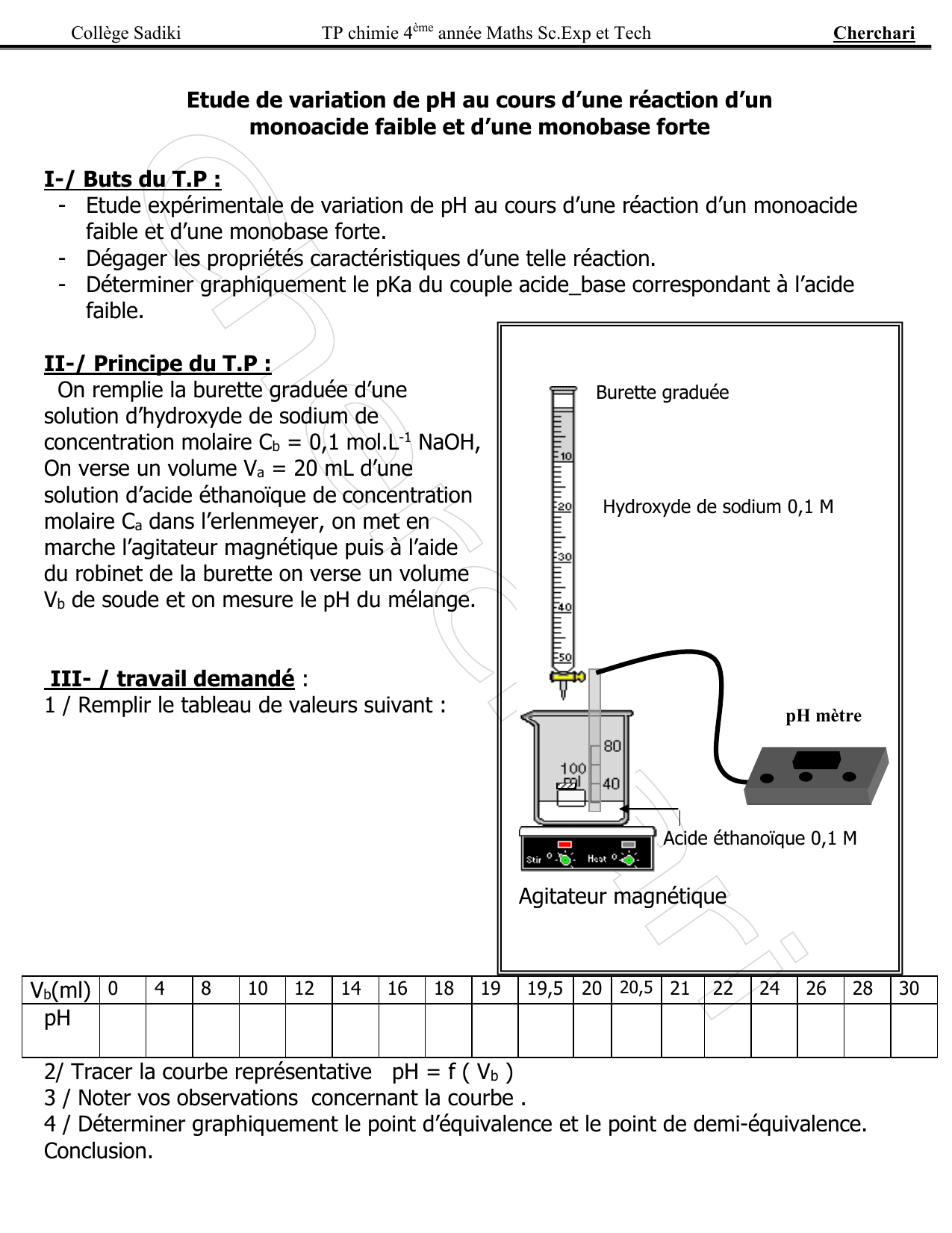
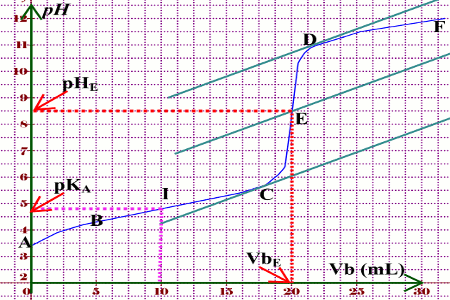
§ 7 (suite) Titrages acide-base
Considérons le titrage d’une solution d’un acide faible tel que l’acide acétique par exemple par une base forte comme NaOH La fonction pH = ƒ(!) dans ce cas est du 3e degré |
|
Les acides et les bases
• dans un couple acide/base conjuguée si un acide est fort sa base conjuguée est très faible et vice versa • l’ion H 3 O+ est l’acide le plus fort qui peut exister en solution aqueuse • un acide plus fort réagirait avec H 2 O ex ; HCl(aq) + H 2 O(l) H 3 O+(aq) + Cl-(aq) |
Quels sont les acides faibles ?
Exemple de bases faibles : les ions carboxylates (fonction ), c'est-à-dire les bases conjuguées des acides carboxyliques. • Un acide fort est un acide réagissant totalement avec l’eau. Si sa concentration est c, alors . • Un acide faible AH réagit avec l’eau selon une réaction limitée .
Comment calculer le pH d’un acide fort ?
Donc, si on dissout n moles d’un acide fort dans l’eau, alors il va se former n moles d’ qui vont se combiner avec l’eau pour former n moles d’ions oxonium . Estimation du pH : soit c (en mol/L) la concentration d’un acide fort dissous dans l’eau. On a . Comme le pH est donné par , il vient : (avec c diluée mais pas trop)
Quelle est la différence entre un acide et une base ?
acide : espèce chimique capable de libérer un (ou plusieurs) proton (s). base : espèce chimique capable de capter un (ou plusieurs) proton (s). Attention ! solution acide ≠ acide acide faible : c’est un acide dont la réaction sur l’eau n’est pas totale. base faible : c’est une base dont la réaction sur l’eau n’est pas totale.
Quelle est la différence entre un acide fort et une base forte ?
• Un acide fort est un acide réagissant totalement avec l’eau. Si sa concentration est c, alors . • Un acide faible AH réagit avec l’eau selon une réaction limitée . • Une base forte réagit avec l’eau selon une réaction totale. Pour une concentration c, on a . • Une base faible A– réagit avec l’eau selon une réaction limitée .

Acide FORT ou acide FAIBLE ? 🎯 Exercice BAC Chimie Chimie Terminale spécialité

Cours 7

Quest-ce quun acide fort ? Comment le reconnaître ?
|
Déterminer si un acide est fort ou faible
On connait le pH et la concentration de la solution. Pour savoir si l'acide est fort ou faible il faut : 1. Déterminer [H3O+] par la relation [H3O+]=10- |
|
Acide phosphorique
L'acide phosphorique est un triacide minéral. La première fonction est celle d'un acide fort la deuxième celle d'un acide faible et la troisième celle d'un |
|
Fiche de révisions sur les acides et les bases
acide fort : c'est un acide qui réagit entièrement avec l'eau base forte : c'est une base qui réagit totalement avec l'eau acide faible : c'est un acide |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
Cas d'un mélange d'un acide fort et d'un acide faible. Page 4. 3. 2.6. Cas d'un mélange de deux acides faibles. |
|
PH et pKa
Une solution contenant un acide fort a un pH inférieur à celui d'une solution de même concentration d'un acide faible. ([HCl] 0.1 M pH < 1; [CH3COOH] 0.1 M |
|
Fiche de synthèse n°2 : réactions acido-basiques en solution aqueuse
Soit un acide faible AH qui réagit avec l'eau selon la réaction d'équation : dissocié dans l'eau le pH d'une solution d'acide fort de concentration. |
|
PH dune solution de chlorure dammonium pH = 5.6
Le chlorure d'ammonium NH4Cl est un sel soluble qui se dissocie dans l'eau suivant la réaction : NH Cl NH. Cl. 4. 4. ?. ?. +. ?. +. Cet acide faible |
|
VI..Etude sommaire des mélanges
l'acide faible possède une constante d'acidité et une concentration assez faibles) La réaction entre un acide fort et une base faible est complète si la. |
|
§ 7 (suite) Titrages acide-base
Le pH du point d'équivalence est encore égal à 7. Le titrage d'une base faible par un acide fort est également le symétrique du cas du titrage d'un acide faible |
|
Dosage acide faible – base forte
un acide suffisamment faible et pas trop dilué Ceci implique que l'acide ne soit pas trop fort ou trop dilué pour que sa. |
|
Révisions sur les acides et les bases - Nicole Cortial
Exemples de réactions de dissolution de bases et d'acides forts : • L'acide acide faible : c'est un acide dont la réaction sur l'eau n'est pas totale base faible |
|
PH et pKa - Eli Zysman-Colman
pKa = -log Ka Plus la valeur de pKa est faible, plus le Ka est grand, plus l'acide est fort 4 Table de pKa http://evans harvard edu/ pdf /evans_pKa_table pdf |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
Cas d'un mélange d'un acide fort et d'un acide faible Page 4 3 2 6 Cas d'un mélange de deux acides faibles |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0 Dans le cas d'un acide fort, totalement dissocié dans l'eau, la concentration finale |
|
Le pH 3 Le pH des acides et bases forts - théorie - 2014
Déterminer si une espèce chimique est un acide fort, un acide faible, une base forte ou une base faible aussi bien à partir d'une formule brute que du nom de l' |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
7 II – LA REACTION ACIDE/BASE 8 1 LES ACIDES FORTS ET LES BASES FORTES 8 2 LES ACIDES FAIBLES ET LES BASES FAIBLES : CONSTANTE |
|
VIEtude sommaire des mélanges
2) Acide fort 1 + acide faible 2 On calcule souvent le pH en négligeant l'acide faible Cette approximation grossière n'est justifiée que si l'apport d'ions |
|
Propriétés des acides et des bases
•pKa faible « Ka élevé : acide fort •pKa élevé « Ka faible : acide faible Les acides faibles en solution aqueuse se dissocient seulement partiellement, |
|
Les acides et bases en solution aqueuse - Groupe Transition
Coefficient d'ionisation (de dissociation) d'un acide ou d'une base faible Pourcentage effet, HCl est un acide fort totalement ionisé en solution aqueuse |