acide fort ou faible pka
|
§ 7 (suite) Calcul du pH de solutions
Si la concentration d’un acide faible HA ou d’une base faible B en solution est suffisamment grande et leur pK a ou pK b également suffisamment grand la fraction de l’acide dissocié A– ou de la base protonée BH+ peut être négligée vis-à-vis de la concentration de l’acide non-dissocié ou de la base non-protonée |
|
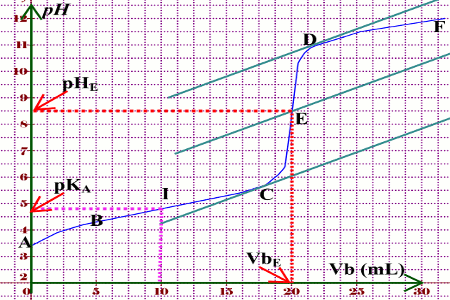
§ 7 (suite) Titrages acide-base
On a une solution contenant ca· \"a du sel de la base conjuguée de notre acide faible (de l’acétate de sodium dans notre exemple) Nous avons donc une solution d’une base faible et le pH peut être estimé à partir de l’équation approchée : pH = 7 + 1/2 pKa + 1/2 log ( ca· \"a / c0 ) |
|
Tables des pKa
II – Acide faible et base conjuguée faible : Acide faible Base conjuguée faible pKa HO+ 3 H2O - 175 HClO3 − ClO3 0 Acide picrique HB B− 038 Acide trichloracétique HB B− 066 Acide benzène sulfonique HB B− 07 HBrO3 − BrO3 07 HIO3 − IO3 077 HSCN SCN− 08 H2CrO4 − HCrO4 08 H2P2O7 − HP2O7 085 Acide sulfamique HB B− 10 |
|
PH et pKa
Si pKa1 < pKa2 l'acide A1 est plus fort que l'acide A2 l'acide A1 est plus faible que l'acide A2 les acides A1 et A2 sont de force moyenne Dans la théorie de Brønsted un acide est un : donneur de proton(s) capteur de proton(s) donneur ou capteur de proton(s) selon le cas Une solution est acide quand |
Quelle est la différence entre le premier et le deuxième pKa d’un acide polyprotique ?
Si la différence entre le premier et le deuxième pKa d’un acide polyprotique est suffisamment grande, la contribution à la concentration en protons du deuxième équilibre et des suivants peut être négligée. Le problème revient ainsi à traiter le cas d’un monoacide faible ou fort.
Comment trouver le lien entre la concentration d'un acide fort et le pH ?
Problématique : si on sait facilement trouver le lien entre la concentration d'un acide fort et le pH, les choses sont plus délicates avec un acide faible. On pourrait penser utiliser le taux d’avancement final (pourcentage de molécules AH passées sous forme ). Toutefois, dépend de la concentration initiale en acide :
Quels sont les acides faibles ?
II – Acide faible et base conjuguée faible : Acide faible Base conjuguée faible pKa HO+ 3H2O - 1,75 HClO3 − ClO30 Acide picrique HB B−0,38 Acide trichloracétique HB B−0,66 Acide benzène sulfonique HB B−0,7 HBrO3 − BrO30,7 HIO3 − IO30,77 HSCN SCN−0,8 H2CrO4 −
Qu'est-ce que le pKa ?
Le pKa Définition : De la même manière que l’on définit le pH par et , on définit le par ou . Comme le , le est sans dimension. Échelle de : Le , et par extension le sont de bonnes « étiquettes » afin de cataloguer les couples acide/base. On construit alors une échelle de :
|
PH et pKa
Plus la valeur de pKa est faible plus le Ka est grand |
|
Déterminer si un acide est fort ou faible
On connait le pH et la concentration de la solution. Pour savoir si l'acide est fort ou faible il faut : 1. Déterminer [H3O+] par la relation [H3O+]=10- |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0. Dans le cas d'un acide fort totalement dissocié dans l'eau |
|
Fiche de synthèse n°2 : réactions acido-basiques en solution aqueuse
? = 1 correspond à un acide totalement dissocié donc fort. Exemple : Pour un acide faible de pKa = 5 et C0 = 10-3 mol.L-1 |
|
§ 7 (suite) Titrages acide-base
pH = pKa + log { ! / (1–!) } Titrage d'un acide faible par une base forte point d'équivalence. pH = 7 + 1/2 pKa + 1/2 log ( ca· "a / c0 ). |
|
Chapitre 8 : Propriétés acide-base.
Base faible : (. ) (. ) 1. 1. 7 log. 7. 1.92 1 7.46. 2. 2. pH. pKa. C. = +. +. = +. ? = f) HClO4. Acide fort. 1. pH = . g) H2NNH2. Base faible. |
|
Chapitre 4. Force des acides et des bases
4.1.3 Relation entre le pH et le pKa . 4.3.1 Acide fort ou faible - Base forte ou faible . ... On définit également le pKA d'un couple acide-base :. |
|
Les acides et bases en solution aqueuse.
est une base plus faible que C2N5NH2. b) HClO est un acide plus fort que C2H5NH3. +. : VRAI. En effet pKa ( |
|
CHAPITRE 5 : Acidité basicité et pKa
Force de liaison. - Plus la liaison H-X est forte plus l'acide est faible. - Habituellement |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0 Dans le cas d'un acide fort, totalement dissocié dans l'eau, la concentration finale |
|
Révisions sur les acides et les bases - Nicole Cortial
Exemples de réactions de dissolution de bases et d'acides forts : • L'acide nitrique acide faible : c'est un acide dont la réaction sur l'eau n'est pas totale pKA H3O + H2 O H2 O OH - KA Bases de plus en plus fortes Acides de plus en |
|
Propriétés des acides et des bases
contraires : •pKa faible « Ka élevé : acide fort •pKa élevé « Ka faible : acide faible Les acides forts en solution aqueuse se dissocient complètement Acide fort |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
2 5 Cas d'un mélange d'un acide fort et d'un acide faible Constantes d'acidité et pKa des couples acide/base usuels, en solution aqueuse, à 25°C Acide |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
CLASSEMENT DES ACIDES ET DES BASES SUR UNE ECHELLE DE PKA 10 4 plus pKA est petit, plus l'acide AH est fort et sa base conjuguée A-‐ faible |
|
Force des acides et des bases - Lycée dAdultes
4 1 3 Relation entre le pH et le pKa 4 3 1 Acide fort ou faible - Base forte ou faible 4 3 3 Composition finale d'une solution d'acide faible |
|
1 Calculer le pH de solutions dun acide faible HA (pKa = 3,75) aux
A : une solution très basique B : une solution au pH négatif C : un mélange de deux acides forts D : un mélange d'acide et de sa base conjuguée Page 2 6 Un |
|
VIEtude sommaire des mélanges
éloigné de la base pour que la différence de leurs pKa dépasse 3 2) réaction entre un acide fort et une base faible Un acide fort fournit en solution aqueuse |