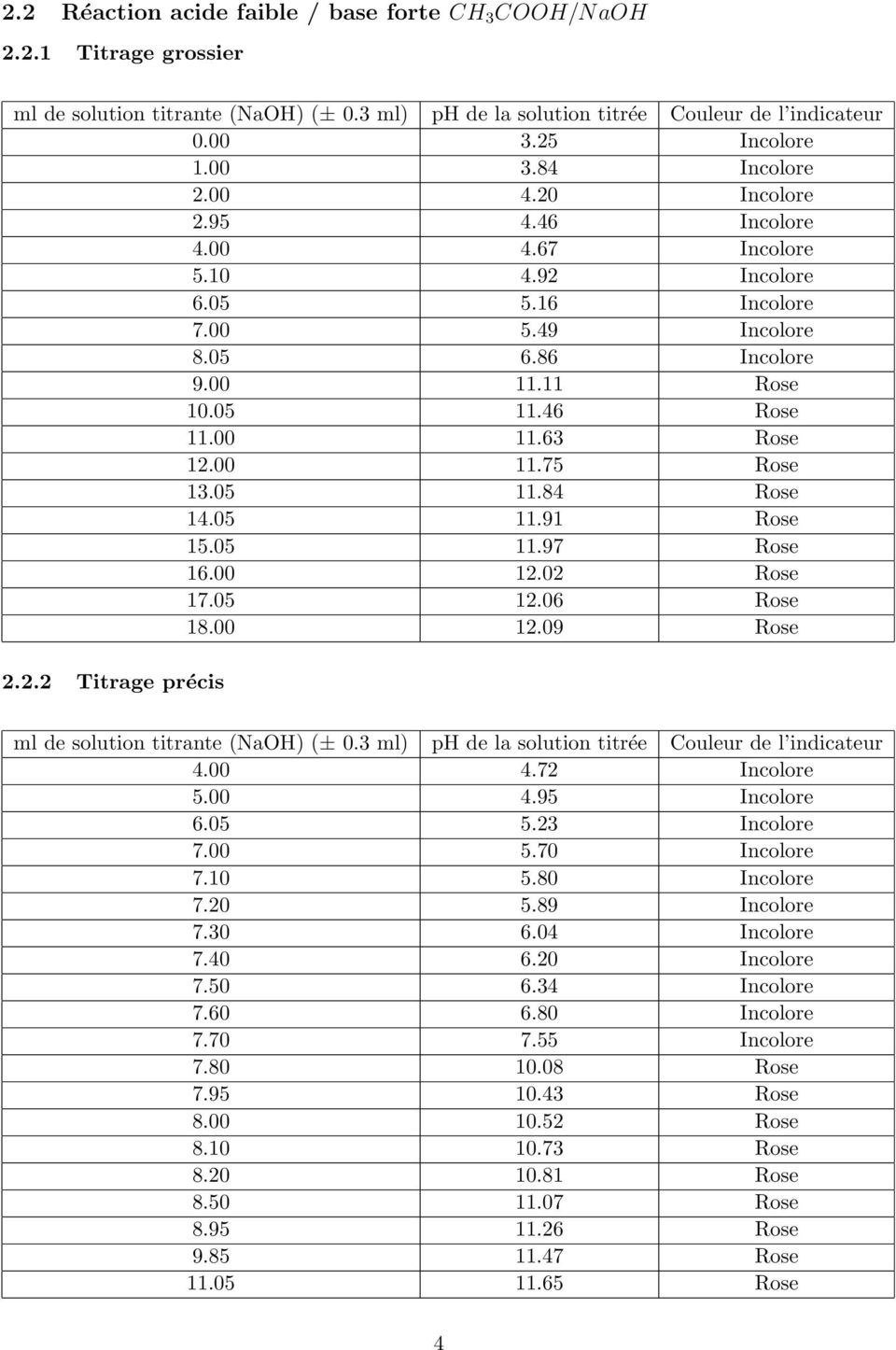
acide fort ph
|
§ 7 (suite) Calcul du pH de solutions
On a alors pour les solutions de l’acide fort et de la base forte respectivement : [H3O+] ≈ ca et [OH–] ≈ ca ⇒ [H3O+] ≈ Ke⋅(c0)2 / ca Si au contraire ca est très petit et en particulier |
|
§ 7 (suite) Titrages acide-base
Dans le cas particulier du titrage d’une acide fort (HCl par exemple) par une base forte (NaOH par exemple) : – pour 0 < ! < 1 il y a un excès d’acide et le pH est donné par pH ≈ – log (c / c0) ⇒ pH = – log { c a⋅(1– !)· V 0 / [c0· (V 0 + V titr)] } = – log { c a⋅(1– !)· \"a / c0 } |
|
Acid-Base pH Titration Introduction
The data will be displayed in the following format showing appropriate values for the slope (m) and y-intercept (b) y = mx + b m: 0 11 b: 12 35 (these are just example values) Cor = 0 98 20 Record the equation in your notebook in Data Table for pH vs Volume in the following format pH = 0 11V + 12 35 |
|
TITRE ACIDE FORT – BASE FORTE OS 3 Moyens
Monoacide : HCl acide chlorhydrique ; HBr acide bromhydrique ; HI acide iodhydrique ; HNO 3 acide nitrique Diacide : H 2SO 4 acide sulfurique 3° pH d’un acide fort Le pH d’un monoacide fort de concentration C a est donné par la relation suivante : pH = – log C a II) Base forte 1° Etude de la solution aqueuse d’hydroxyde de sodium |
|
PH et pKa
Définition La définition que nousutiliserons : Brønsted-Lowry (1923) Un acide est une espèce qui a tendance à perdre un proton [H2O] est très grand et ~constant Constante d’acidité Plus la valeur de pKa est faible plus le Ka est grand plus l’acide est fort 3 pKa = -log Ka Table de pKa http://evans harvard edu/ pdf /evans_pKa_table pdf 4 |
Comment calculer la réaction d’un acide fort avec l’eau ?
Pour une réaction d’un acide fort avec l’eau, l’équation chimique générale ci-dessus s’applique, sauf que le symbole d’équilibre est généralement remplacé par une flèche à sens unique pour indiquer que la réaction est entièrement terminée : donne des quantités de H3O+ et de A- qui représentent une ionisation bien inférieure à 100 %.
Quels sont les acides forts ?
donne 100 % de H3O+ et de A- lorsque l’acide s’ionise dans l’eau ; la figure 5.3.1 énumère plusieurs acides forts. Si nous commençons avec 0,1 M HCl, à l’équilibre nous obtenons 0,1 M H3O+ et 0,1 M Cl–. Selon la définition de Brønsted-Lowry, en tant qu’acide fort, le HCl est un très bon donneur de protons.
Comment mesurer le pH d’un acide faible ?
En examinant le pH de chaque solution à 0,1 M de chaque acide faible, il est important d’apprécier l’ampleur considérable de la différence d’acidité entre les divers acides faibles. Par exemple, les valeurs de Ka pour HCO2H et CH3COOH ne semblent pas très différentes, et leurs valeurs de pH ne diffèrent que de 0,5 unité.
Comment mesurer le pH d’un titrage acide-base ?
Le pH à chacun de ces points est généralement différent de 7. Lors d’un titrage acide-base, on détecte le point d’équivalence (fin de la réaction de neutralisation) en mesurant le pH à l’aide d’un pH-mètre ou en employant un indicateur coloré qui change de couleur dans une zone de pH donnée.

Chimie en solution ep4 : calcul du pH

Calcul de pH : FORMULES & CONDITIONS

Acides forts bases fortes pH et solutions tampons
|
PH et pKa
Une solution contenant un acide fort a un pH inférieur à celui d'une solution de même concentration d'un acide faible. ([HCl] 0.1 M pH < 1; [CH3COOH] 0.1 M |
|
§ 7 (suite) Titrages acide-base
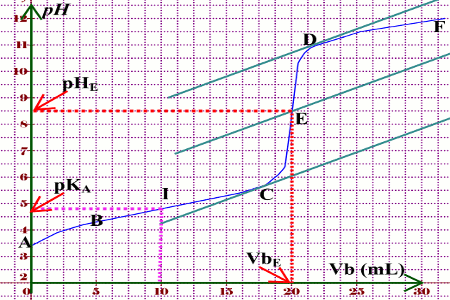
Un indicateur est un acide faible dont la forme acide HIn est caractérisé par Titrage d'un acide fort par une base forte. pH ! "a = V0 / (V0 + Vtitr). |
|
Dosage acide fort - base forte
Etant donné la valeur du pH à l'équivalence la zone de virage de l'indicateur coloré devra contenir la valeur de. pH=7. La précision du dosage est d'autant |
|
VI..Etude sommaire des mélanges
Acides et bases. Chapitre VI. 80 b) Mélanges d'acides. 1) Acide fort 1 et acide fort 2. Le pH se calcule en sachant que les deux acides sont entièrement |
|
Rappel sur les Acides et les Bases
H3O+ On évalue l'acidité d'une solution en utilisant le pH (pour Par définition un acide fort est totalement dissocié en solution (Ka >> 103). |
|
Fiche de synthèse n°2 : réactions acido-basiques en solution aqueuse
Lien entre le pH et le pKa d'un couple. Le pH d'une solution contenant un acide faible AH et sa base conjuguée A? est lié au pKa du couple AH/A?par la |
|
Solutions tampons
Ainsi les solutions d'acide fort ou de base forte ne constituent pas de bonnes d'un acide faible par une base forte |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
3.4. Calcul du pH de ST. 4. Titrages acide-base. 1.1. Titrage d'un acide fort par une base forte. |
|
Chapitre 1 Acides et bases
suivante entre concentration apportée en acide c et pH : pH = ?log (c). La base conjuguée d'un acide fort est dite “indifférente dans l'eau” |
|
Dosage acide faible – base forte
un acide suffisamment faible et pas trop dilué. ? ou un acide pas trop faible x=0 ; vb=0 ; solution d'acide faible. )clog. pK(. 2. 1. pH. |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
CALCUL DE PH DES SOLUTIONS AQUEUSES 2 1 Cas d'un acide fort 2 2 Cas d'un acide faible 2 3 Cas d'une base forte 2 4 |
|
Révisions sur les acides et les bases - Nicole Cortial
donc la base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et 14 10 |
|
PH et pKa - Eli Zysman-Colman
pKa = -log Ka Plus la valeur de pKa est faible, plus le Ka est grand, plus l'acide est fort 4 Table de pKa http://evans harvard edu/ pdf /evans_pKa_table pdf |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0 Dans le cas d'un acide fort, totalement dissocié dans l'eau, la concentration finale |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
7 II – LA REACTION ACIDE/BASE 8 1 LES ACIDES FORTS ET LES BASES FORTES 8 2 LES ACIDES FAIBLES ET LES BASES FAIBLES : CONSTANTE |
|
Propriétés des acides et des bases
•pKa = -log (Ka) ou Ka =10 (- pKa) montre que pKa et Ka varient en sens contraires : •pKa faible « Ka élevé : acide fort •pKa élevé « Ka faible : acide faible |
|
VIEtude sommaire des mélanges
b) Mélanges d'acides 1) Acide fort 1 et acide fort 2 Le pH se calcule en sachant que les deux acides sont entièrement ionisés Exemples: 1) mélange de 500 |
|
Déterminer si un acide est fort ou faible
Un acide est fort s'il de dissocie totalement lors de sa mise en solution On a alors la relation [H3O+]=C • Un acide est faible s'il se dissocie partiellement lors de |
|
Dosage acide fort - base forte
Acide fort - base forte 1 Dosage acide fort – base forte Acide fort HA : titré, Base forte NaOH titrant, concentration cb, volume vb (à verser à la burette) : − |
|
Acide phosphorique - INRS
L'acide phosphorique est un triacide minéral La première fonction est celle d'un acide fort, la deuxième celle d'un acide faible et la troisième celle d'un acide |