conclusion titrage acide base
|
§ 7 (suite) Titrages acide-base
On a un mélange équimolaire de HCO3– et CO32– dont le pH = pKa2 = 10 32 Pour ! = 2 la deuxième acidité est à son tour totalement neutralisée On a une solution de concentration ca· \"a de CO32– une base dont le pH est donné par : pH = 7 + 1/2 pKa2 + 1/2 log (ca· \"a / c0 ) Pour pH ≈ 11 7 |
|
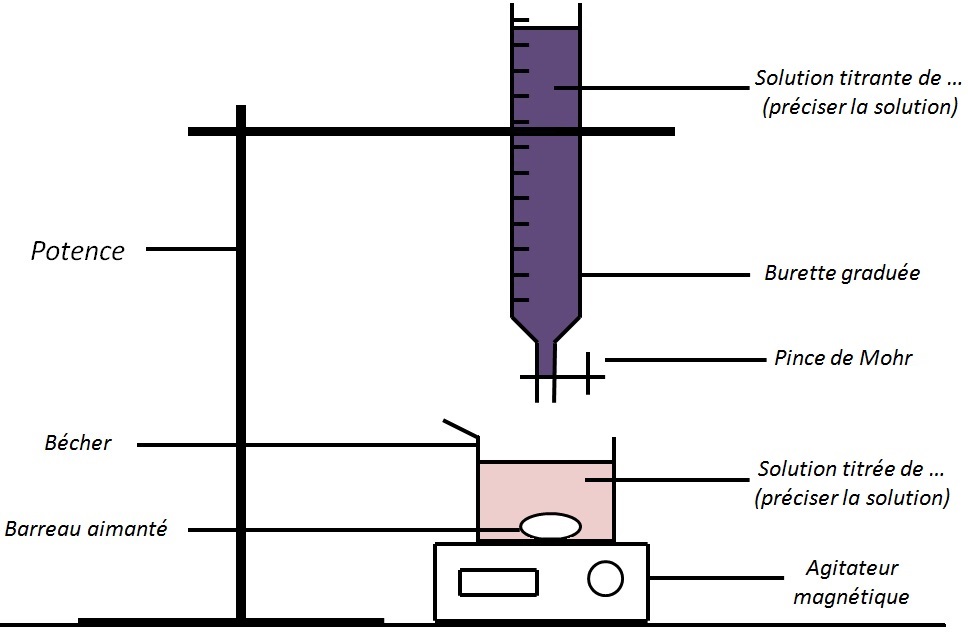
TP n 2 : Titrages
A +B !C (titrage) Exemple : titrage du fer par le cérium Titrage indirect On titre la quantité de C formée par réaction entre A et B A +B !C (1) C +D !E (titrage) Exemple : Dosage du dioxygène par la méthode de Winkler Titrage/dosage en retour On fait réagir A avec B en excès puis on titre la quantité de B n’ayant |
|
Chapitre 8 : Titrages acido-basiques
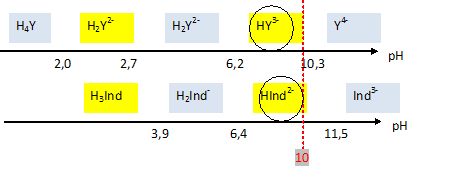
3) Conclusion : critère de choix de l’indicateur coloré pour un dosage (3): a La règle à respecter : L’indicateur coloré choisi pour suivre un titrage acido-basique doit être introduit en très petite quantité (quelques gouttes car c’est un couple acide-base qui pourrait perturber la réaction étudiée) et |
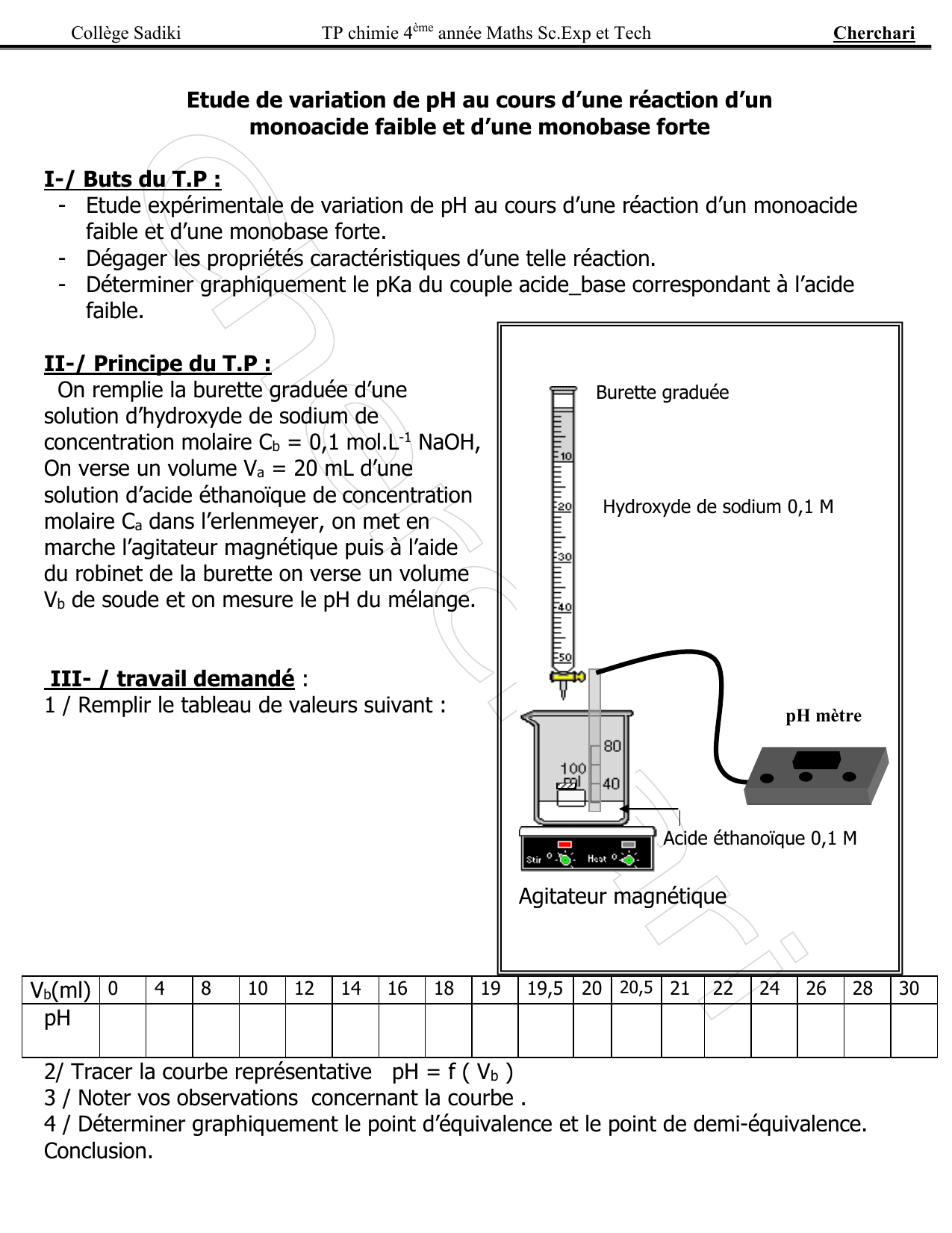
Comment titrage-t-on une solution d'un acide faible ?
Considérons le titrage d’une solution d’un acide faible, tel que l’acide acétique par exemple, par une base forte, comme NaOH. La fonction pH = ƒ(!) dans ce cas est du 3e degré. Les approximations présentées jusqu’ici s’appliquent toutefois aux différents domaines de la courbe : – Pour ! = 0 , l’acide faible est pur.
Comment déterminer le point d'équivalence d'un titrage acide base ?
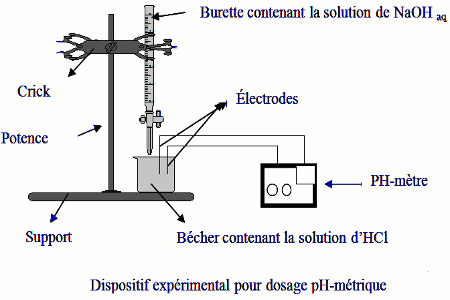
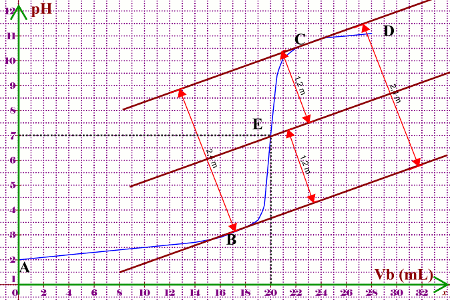
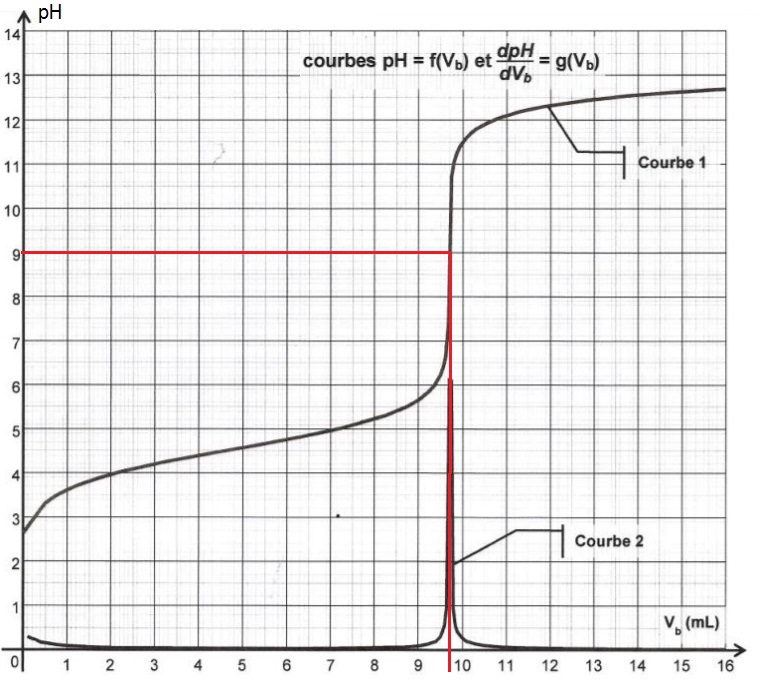
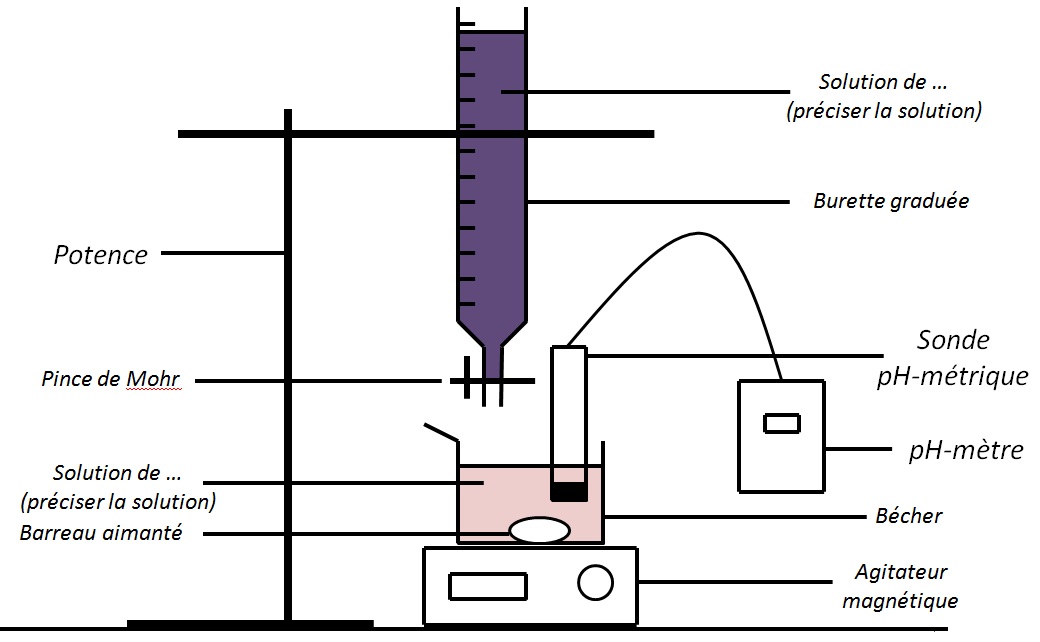
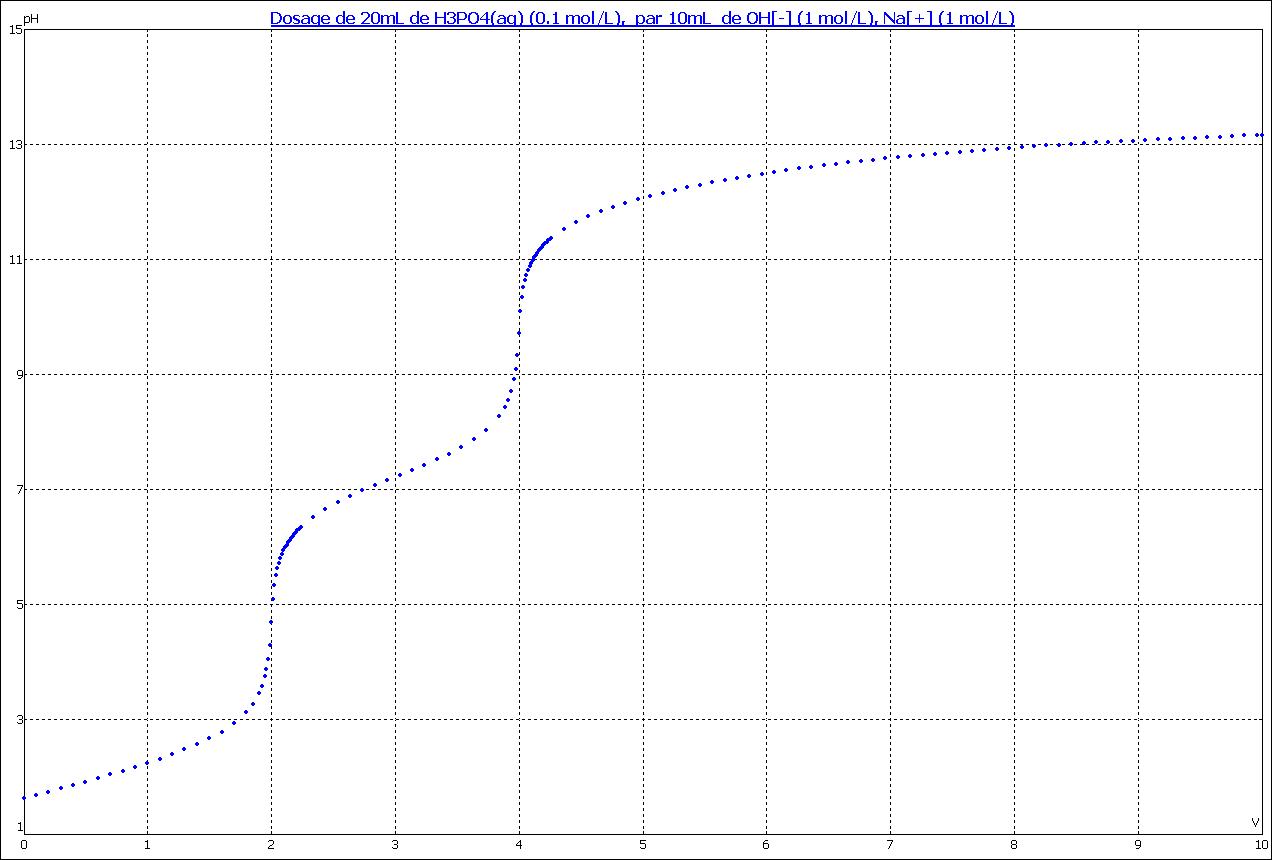
Il existe deux façons courantes de déterminer le point d’équivalence d’un titrage acide base. soit en utilisant un pH mètre pour mesurer le pH et tracer la courbe de titrage. Le milieu de la zone verticale de courbe correspond au point d’équivalence (voir courbe)
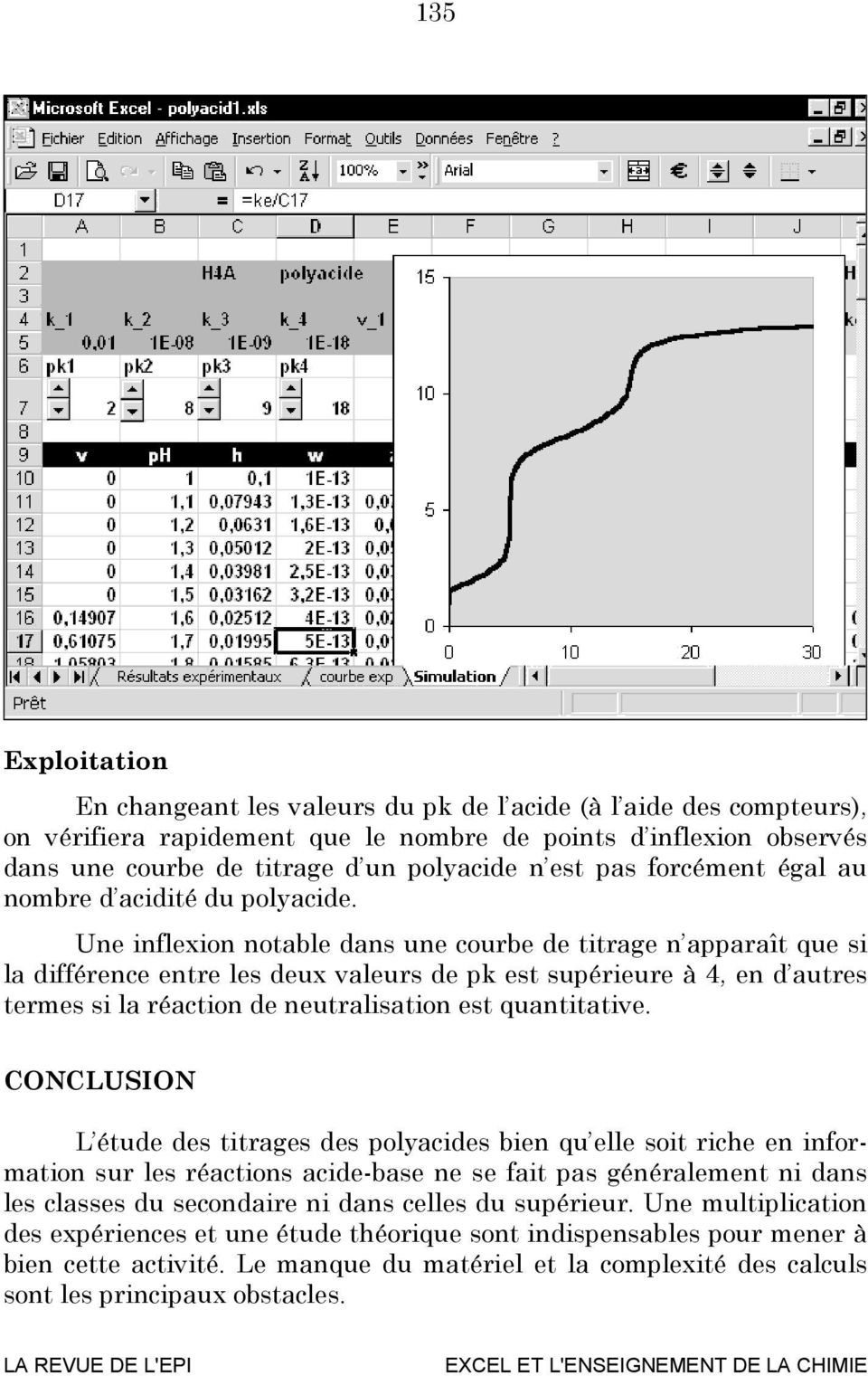
Comment l'identité d'un acide affecte-t-elle la forme de la courbe de titrage ?
Cependant, dans les titrages d’acides faibles ou de bases faibles, l’identité de l’acide faible ou de la base faible titrée affecte fortement la forme de la courbe de titrage. Lorsque l’acide ou la base titrée devient plus faible (son pKa ou pKb augmente), la variation du pH autour du point d’équivalence diminue de manière significative.
|
§ 7 (suite) Titrages acide-base
Que peut-on éventuellement conclure à propos de la température à laquelle le titrage a été effectué ? pH. Vtitr / mL. Vtitr = 795 mL. Acides aminés. Un acide |
|
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
Sa forme acide réagit donc avec la base HO. - lors du titrage et augmente donc Conclusion : c'est la proposition 3 qui convient pour ce titrage. 2.3. Pour ... |
|
LES TITRAGES ACIDES-BASES
On peut conclure que: ▫ Le dosage d'un acide fort par une base forte est est basée sur un titrage acide base. ❖ Soufre = le soufre présent dans les ... |
|
Chapitre 8 : Titrages acido-basiques
titrage acide-base. (3). Montrer qu'un indicateur coloré convenablement 3) Conclusion : critère de choix de l'indicateur coloré pour un dosage. (3). : a. La ... |
|
Étude dune réaction : titrage des ions fer II par les ions permanganate
Pour que ce soit le couple. MnO4. -(aq) / Mn2+(aq) qui interviennent le mélange réactionnel doit être acide d'où l'ajout d'acide dans la solution à titrer. 3 |
|
Comportement détudiants effectuant un titrage acide-base à partir
3 avr. 2020 La mise en place d'un tel étayage nécessite la détection automatique du comportement et du besoin en temps réel. CONCLUSION ET PERSPECTIVES. |
|
Conclusion générale & Perspectives
basique et acide et au cours du temps ceci indique donc une bonne stabilité ... acides aminés |
|
Sans titre
L'interprétation des résultats et la conclusion. La note tiendra compte des 2- Dosage TITRIMETRIQUE de l'acide sulfurique (solution inconnue) par la base. |
|
Conclusion générale
25 sept. 2019 Ce dernier se divise en différents domaines composés chacun de trois bases d'ARN appelés codons. Le premier acide aminé incorporé est toujours ... |
|
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
À quel couple acide/base appartient l'ion hydroxyde HO– ? 3.5. Écrire l'équation de la réaction support de titrage. 3.6. Quelles caractéristiques doit posséder |
|
TRAVAUX PRATIQUES DE CHIMIE I
Principe de la manipulation. Il s'agit de déterminer la concentration en acide lactique (de formule CH3CHOHCOOH) d'un lait en réalisant un dosage acidobasique ( |
|
Problème 1 : Titrage dune solution dacide oxalique
28 avr. 2016 La réaction entre l'acide oxalique et les ions permanganate fait ... les concentrations de l'acide et de la base sont égales ce qui est. |
|
Conclusion générale
L'utilisation des solides mésoporeux comme catalyseur de réactions acide-base nécessite l'insertion d'aluminium dans la structure des MCM. Il a été montré que c |
|
THESE DOCTORAT DE LUNIVERSITE BORDEAUX 2 ET DE L
Elle porte sur les « titrages » acide/base les notions de pH et de Enfin dans la conclusion générale nous essaierons de répondre aux différentes ... |
|
Exercice avec correction : dosage dun vinaigre
Couple acide/base. (H3O+/H2O). (CH3COOH/CH3COO-). (H2O/HO-) 2.1 Dosage de l'acide éthanoïque du vinaigre ... Conclusion : la réaction est quasi totale. |
|
Solutions tampons
de la concentration (voir dosage acide fort - base forte) et ces solutions ne sont donc pas des tampons satisfaisants vis à vis de la dilution. |
|
Conclusion générale & Perspectives
part nous avons conçu des biocapteurs basés sur un mime peptidique du VEGF |
|
Dosages de mélanges dacides
Le deuxième montre une méthode de dosage d'un mélange de deux acides forts : acide nitrique et acide chlorhydrique. En pratiquant un dosage acido-basique |
|
TP 3: Acides et Bases
5 oct 2007 · INTRODUCTION Ce travail ou naturels Enfin, la troisième partie est le titrage de l'acide acétique en solution diluée et de pur ou complété par du HCl ou du NaOH (acide et base forts) à des volumes divers notés dans |
|
Les titrages acido-basiques en Terminale S - Aix - Marseille
3 mai 2007 · expérimentale pour laquelle le titrage acido-basique est toujours un grand classique chaque an- née Philippe Jeanneret 1 Introduction 3 Soit par exemple le titrage d'une solution d'acide éthanoïque CH3CO2H (aq) |
|
TRAVAUX PRATIQUES DE CHIMIE I - Université Ibn Khaldoun de
II Introduction Le dosage acidobasique est utilisé afin de déterminer la concentration inconnue d'une solution composée d'un acide ou d'une base, ou d' un |
|
Dosage pH-métrique dun acide fort par une base forte
Figure 72 : effet de dilution sur la courbe de titrage acide fort - base forte comme conclusion ici quels sont les caractères de la réaction du dosage ? |
|
8-Titrages acido-basique - Physagreg
Réaliser par suivi pH-métrique le titrage d'un acide ou d'une base en solution aqueuse 3) Conclusion : critère de choix de l'indicateur coloré pour un dosage |
|
Informatique Titrage acide/base - Cours dinformatique
17 avr 2013 · Réalisa- tion du graphique de l'évolution du pH en fonction du volume de réactif introduit 1 Titrage d'un acide fort par une base forte 1 1 |
|
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
Savoir repérer précisément l'équivalence dans un titrage pH-métrique (méthode des tangentes parallèles À quel couple acide/base appartient l'ion hydroxyde HO– ? 3 5 Conclusion : c'est la proposition 3 qui convient pour ce titrage 2 3 |
|
TP CHIMIE-1 & TP CHIMIE-2 - Université Larbi Ben Mhidi OEB
I-Quelques recommandations en guise d'introduction 2 TP II : Le dosage acido-basique (cas d'un acide fort par une base forte) 14 |
|
TP Chimie n° 3
Dosage acido-basique en présence d'indicateurs colorés (Dosage de l'acide acétique contenu dans le vinaigre) 1 Introduction Le vinaigre de vin est un produit |