La dissolution du composé 1ère Physique
|
Chimie Générale (Chimie 1)
23 déc 2020 · Une molécule est une union de deux ou plusieurs atomes liés entre eux par des liaisons C'est la plus petite partie d'un composé qui a les mêmes |
|
Exercices de physique-chimie Première Spécialité
Écrire l'équation de réaction de dissolution dans l ?eau de chacun des composés ioniques suivants 1 le chlorure de cuivre (II) CuCl2(s) 2 l'iodure de |
|
Physique-Chimie 1re Spdf
composé est organique c Les doubles liaisons sont conjuguées les groupes dissolution Extraction du sulfate de cuivre et du rouge de méthyle d'un |
|
PHYSIQUE-CHIMIE
Objectif Préparer un volume v de solution de concentration C par dissolution d'un composé de masse molaire M La masse m à dissoudre vaut m=M C V (m en g ; M |
Quelles sont les 3 etapes de la dissolution ?
La dissolution d'un solide ionique s'effectue en trois étapes : - La dissociation (destruction du cristal par les molécules d'eau (sous l'action des forces électrostatiques). - l'hydratation des ions -la dispersion des ions: Les ions sont entourés d'un cortège de molécules de solvant qui les isole les uns des autres.
Quel sont les étapes de la dissolution ?
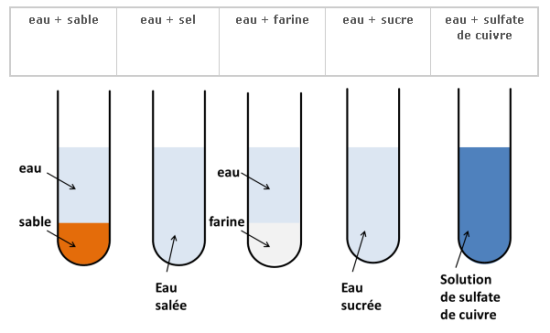
La dissolution est un procédé qui consiste à mettre un soluté dans un solvant dans le but de préparer une solution constituée d'une seule phase (mélange homogène).
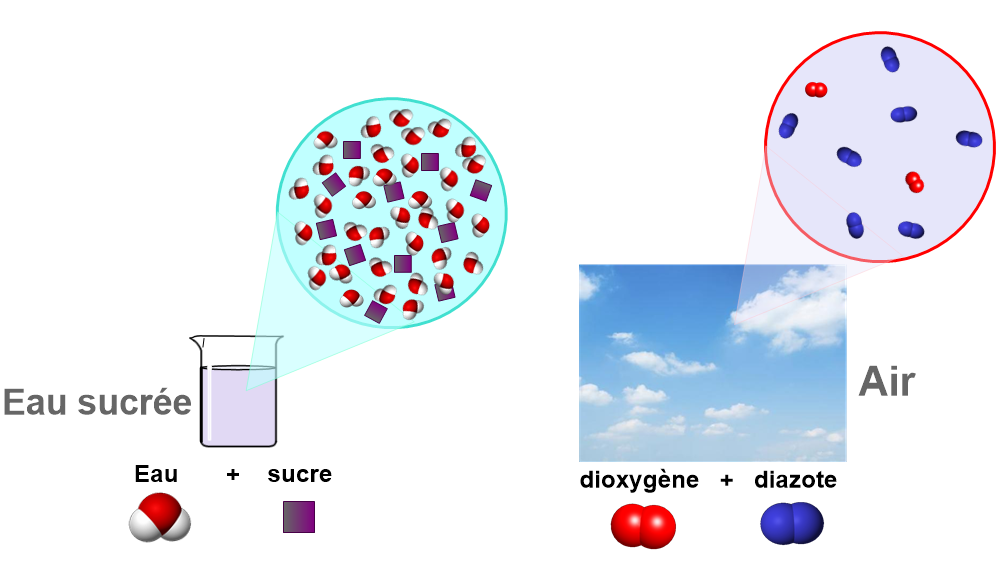
Lorsqu'on mélange un soluté et un solvant, les molécules de soluté se déplacent jusqu'à ce qu'elles soient réparties de manière uniforme dans l'eau.Comment expliquer la dissolution ?
Une substance solide, liquide ou gazeuse se dissout dans un liquide mis à son contact quand elle disparaît dans la masse de ce liquide pour donner un tout homogène.
La dissolution est un processus physique, sans réaction chimique.
Elle peut néanmoins s'accompagner d'une variation de température.
|
Programme de physique-chimie de première générale
réinvestis pour rendre compte d'opérations courantes au laboratoire de chimie : dissolution d'un composé solide ionique ou moléculaire dans un solvant et |
|
Dissolution de composés ioniques ou moléculaires
Dissolution de composés ioniques ou moléculaires. I). Comment prévoir si un solvant est polaire ? 1) Définitions. Une …………………………………….. est obtenue par |
|
Correction exercices Précis de Physique-Chimie chapitre1 à 4
Précis d'électrotechnique – Tome 1 – 1ère année – Michel Pinard Physique-Chimie ainsi que sur la correction des exercices n'hésitez pas à m'en faire ... |
|
Dossier 6 dissolution des espèces chimiques et développement
Objectif Relier la structure d'une espèce chimique à quelques-unes de ses propriétés physiques. 1ère générale - enseignement de spécialité. Constitution et |
|
Exercices de physique-chimie Première Spécialité
Calculer la masse molaire des esp`eces chimiques ou composés ioniques sodium fabriquée par dissolution de 10 g de bicarbonate de sodium NaHCO3 dans ... |
|
LA DISSOLUTION DUN SOLIDE IONIQUE DANS LEAU
Un solvant polaire est un solvant constitué de molécules présentant un moment dipolaire telles que l'eau. sciences physiques et chimiques – Première S http:// |
|
HYDROCARBURES PÉTROLIERS : CARACTÉRISTIQUES
Les hydrocarbures sont composés principalement d'alcanes saturés non cycliques et l'émulsification la dispersion naturelle |
|
PHYSIQUE-CHIMIE- TECHNOLOGIE
A / Première partie En sciences physique et chimique l'enseignement ne doit pas se limiter à ... la dissolution d'un composé solide (voir§1 ; doc. |
|
Spé Physique 1ère - Chapitre 6 : Cohésion et dissolution des solides
Dans un cristal ionique les ions exercent les uns sur les autres des forces d'interaction électrostatique soit attractives (entre deux ions de charge de. |
|
Td corriges biochmv 2014-2015.pdf
Dans un bécher dissoudre ce composé dans de l'eau La première chose à faire est de déterminer s'il s'agit d'un acide faible ou d'un acide fort. |
| Spé Physique 1ère - Chapitre 6 : Cohésion et dissolution des solides |
| Dissolution de composés ioniques ou moléculaires |
| Chapitre 5 - EXERCICES |
| LA DISSOLUTION DUN SOLIDE IONIQUE DANS LEAU - Free |
| 1- On fait dissoudre m = 513 g de sulfate daluminium Al2(SO4)3 (c |
| Devoir surveillé n°2 |
| Devoir surveillé n°6 (sujet A) |
| Chapitre 5 : Cohésion et mélange despèces chimiques |
| Physique-chimie Concentration/ Problème de spécialité En cas de |
Quelles sont les 3 etapes de la dissolution ?
Quel est l équation de dissolution ?
Comment écrire l'équation de dissolution dans l'eau ?
. En divisant par V : n(Fe3+(aq)) / V = n(FeCl3, 6 H2O) / V.
Comment se fait la dissolution des substances ?
. Lorsqu'on mélange un soluté et un solvant, les molécules de soluté se déplacent jusqu'à ce qu'elles soient réparties de manière uniforme dans l'eau.
Comment représenter la dissolution d'un solide ionique ?
- L'équation de dissolution. La dissolution d'un solide ionique peut être représentée par une équation de réaction dans laquelle figure le solide de départ et les ions formés. La gauche de l'équation comporte la formule du solide suivi entre parenthèses du signe (s) qui indique le composé est encore sous forme de solide cohérent.
Qu'est-ce que l'équation de dissolution d'un solide ?
- L'équation de dissolution d'un solide est le bilan de ces trois étapes. Elle fait apparaître, à l'état initial, la formule du solide ionique, qui est alors le soluté, et à l'état final, les formules des ions obtenus. Le nom ou la formule du solvant peuvent être indiqués au-dessus de la flèche, mais ce n'est pas obligatoire.
Comment calculer l’équation de dissolution ?
- L’équation de dissolution est donc de la forme suivante: Espèce chimique (s, l ou g) → espèce chimique (aq) Exemples d’équation de dissolution: Du glucose: C 6 H 12 O 6 (s) → C 6 H 12 O 6 (aq) Du dioxygène: O 2 (g) → O 2 (aq) De l’éthanol: C 2 H 6 O(l) → C 2 H 6 O(aq) Équation de dissolution d’un composé ionique
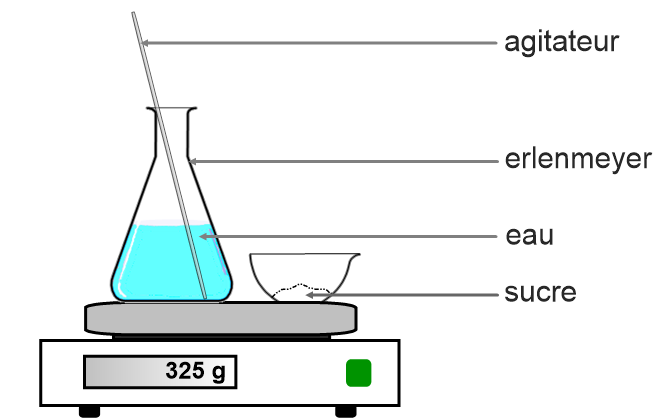
Comment réaliser des dissolutions ?
- Il faut donc faire le tableau d’avancement de l’équation et trouver les relations. Voyons maintenant le protocole expérimental pour réaliser de telles dissolutions. 1ère étape : peser la masse de soluté. Il faut d’abord calculer la masse de soluté que l’on va dissoudre.
|
LA DISSOLUTION DUN SOLIDE IONIQUE DANS LEAU - Free
Un solvant polaire est un solvant constitué de molécules présentant un moment dipolaire, telles que l'eau sciences physiques et chimiques – Première S |
|
EXERCICES - Physicus
1e Spécialité Physique Chimie 2 Dissolution des solides ioniques Le potassium est dans la première co- Le sulfure d'aluminium est un composé io- |
|
SPÉCIALITÉ PHYSIQUE CHIMIE - Physicus
pliant les coefficients de la première équation par b et ceux de la deuxième par Table 5 3 – Exemple de tableau d'avancement d'une réaction de dissolution Le savon est une partie d'une molécule qui est composée d'un atome ou d'un |
|
FICHE PROTOCOLE PREPARATION DUNE SOLUTION PAR
PHYSIQUE A HERRIOT Première S PREPARATION D'UNE SOLUTION Préparer une solution par dissolution d'un solide dans l'eau, de façon à obtenir |
|
Devoir surveillé n°6 (sujet A)
25 fév 2016 · Rappel de cours : indiquer les 3 états physiques de la matière et le nom des 6 changements d'état 2 Quel composé parmi les deux cités |
|
Fiche dexercices 12 : Solides ioniques et moléculaires - Physique et
Physique – Chimie Première S obligatoire - Année scolaire 2016/2017 PHYSIQUE ET MATHS – Soutien scolaire et Cours particuliers |
|
Physique-chimie - mediaeduscoleducationfr
Le programme de physique-chimie de la classe de première s'inscrit dans la courantes au laboratoire de chimie : dissolution d'un composé solide ionique ou |
|
PHYSIQUE CHIMIE - Lycée dAdultes
Notions de première indispensables présents dans une molécule de ce composé, mais cette formule brute ne Dissolution d'un composé moléculaire |
|
Ch 10 - La dissolution
Est-il judicieux d'utiliser un tel solvant pour dissoudre du chlorure de fer II (FeCl2) ? II Dissolution et concentrations II 1 Composés moléculaires Exercice : On |