La pile daniell 3ème Chimie
|
B) Fonctionnement de la pile Daniell : c) Réaction aux électrodes
On peut réaliser des piles identiques à la pile Daniell En général une pile est constituée : -D'une plaque d'un métal M plongé dans une solution contenant |
|
Chapitre 2 : Les piles électrochimiques
DANIELL invente la première pile électrochimique à offrir une source d'énergie durable Comment fonctionne une pile électrochimique ? Prenons l'exemple de la |
|
Chapitre 3 :Oxydoréduction
1) Pile Daniell Lorsque l'interrupteur est ouvert on mesure une différence de potentiel de U = 110V Lorsque l'interrupteur est ouvert on observe un |
|
Chimie des solutions
Exemple : Pile Daniell : Une pile est constituée de deux compartiments séparés physiquement Chaque compartiment appelé 1/2 piles contient les 2 membres |
|
Lélectrochimie
Ce type de pile électrochimique avec des électrodes de Cu et de Zn est maintenant appelée la pile Daniell Dans le diagramme les deux demi-piles sont reliées |
|
Tp : comprendre et modeliser le fonctionnement dune pile
Une pile Daniell est constituée de deux demi-piles La demi-pile de gauche est constituée d'un volume V1 = 50 mL d'une solution de sulfate de zinc (II) de |
|
TP N°10-PROF : LES PILES ELECTROCHIMIQUES
Chimie Prof 1 TP N°10-PROF : LES PILES ELECTROCHIMIQUES Objectifs : ➢ Montrer qu'une transformation chimique spontanée impliquant un échange d'électrons |
Comment fonctionne la pile de Daniell ?
Lorsque les électrons se déplacent d'une cathode vers une anode, les électrons « libres » de la cathode tombent sur les emplacements vides d'électrons (les « étagères ») dans l'anode.
Les électrons vont alors occuper volontiers ces vides dans l'anode, ce qui permet au courant de se déplacer plus loin.Quels sont les 3 éléments essentiels qui constituent une pile ?
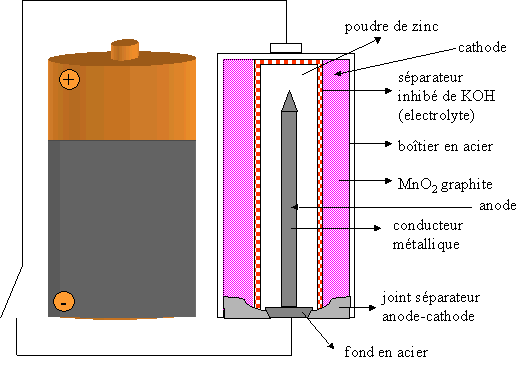
Elles sont constituées d'acier (godet), de zinc et de manganèse avec un électrolyte basique (majoritairement de la soude ou de la potasse).
Quels sont les 3 rôles du pont salin ?
→Le pont salin joue deux rôles : -fermer le circuit afin assurer le passage du courant électrique dans la pile. -assurer la neutralité électrique des solutions.
II/ Modélisation électrique d'une pile.
Notion de force électromotrice.- nmax(e–), la quantité maximale d'électrons que peut faire circuler la pile durant toute sa durée de vie, en mole (mol) e la charge électrique élémentaire : e = 1,60 × 10–19 C.
NA la constante d'Avogadro : NA = 6,02 × 1023 mol.
|
Chapitre 1
Chimie – Partie C – Chapitre 8 : Les piles. – Page 1 sur 3. Nous avons vu au chapitre 7 Transferts spontanés d'électrons – Exemple de la pile Daniell. |
|
Enthalpie libre évolution et équilibre
Rq : elle se calcule à l'aide des potentiels chimiques ? (sera vu en 3ème année). 2. Variation élémentaire d'enthalpie libre Exemple : pile Daniell. |
|
Chapitre 2 - Évolution spontanée dun système chimique
2 NH3. Poisson Florian. Spécialité Physique-Chimie Terminale présenté en suivant l'exemple de la pile Daniell schématisée sur la figure 2.1. |
|
Filière Sciences de la Matière Chimie Cours Chimie des Solutions
Piles électrochimiques - Pile DANIELL. 5.1. Déscription. 5.2. Calcul de la f.e.m de la pile. CHAPITRE IV : REACTIONS DE DISSOLUTION-PRECIPITATION. |
|
TP N°10-PROF : LES PILES ELECTROCHIMIQUES
Chimie. Prof. 1. TP N°10-PROF : LES PILES ELECTROCHIMIQUES. Objectifs : Dans une troisième expérience (qui peut être collective) simuler l'évolution du ... |
|
Chapitre 2 : Les piles électrochimiques I. Quels sont les deux types
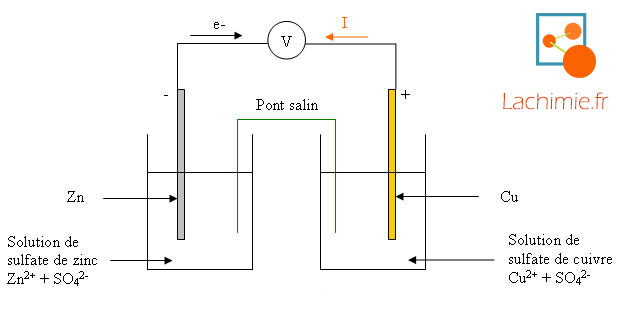
Comment fonctionne une pile électrochimique ? Prenons l'exemple de la pile Daniell (Zinc – Cuivre). Pont salin. (s). |
|
Chapitre 3 :Oxydoréduction
1) Pile Daniell. Lorsque l'interrupteur est ouvert on mesure une différence de potentiel de. U = 1 |
|
Cours de chimie en solution Les acides et les bases
Dans une Pile. OxydAtion. Electrode. Anode. réduCtion. Cathode. Figure III.1 : Pile Daniell. Le pont salin c'est une solution gélifié de KCl les ions K+ et |
|
SCHÉMAS ÉLECTROCHIMIE
Une pile Daniell est constituée d'une électrode de cuivre plongeant dans une solution le montage du 2.1.1 mais en y ajoutant une troisième électrode :. |
|
Electrochimie Exercice n° 1 :
Chimie analytique. Electrochimie. Exercice n° 1 : On réalise la pile Daniell en utilisant : - un bécher renfermant 100cm3 d'une solution molaire de sulfate |
| TP N°10-PROF : LES PILES ELECTROCHIMIQUES - Physagreg |
| Thème : Piles et électrolyses Fiche 4 - Studyrama |
| Niveau 3 - Pierron |
| CH56 PILE et SYNTHÈSE – Correction - sujet A |
| SCHÉMAS ÉLECTROCHIMIE |
| Exercice 1 (6 points) La fabrication du verre |
| Les Piles |
| Chapitre 3 :Oxydoréduction - Melusine |
| Sentraîner : Piles et oxydoréduction Exercice - Lycée Ismael Dauphin |
| Les piles - Chapitre 1 |
| Pile Daniell — Wikipédia |
Comment fonctionne une pile Daniell ?
. Remarque: Le pont salin permet le passage des ions pour conserver l'électroneutralité.
Quels sont les 3 éléments essentiels qui constituent une pile ?
Quelle est l'équation de la caractéristique d'une pile ?
. C'est l'expression de la loi d'Ohm pour le générateur.
. La constante E exprimée en volt (v) est appelée force électromotrice (f.
Comment fonctionne une pile chimie ?
. Elles sont reliées au circuit électrique, par lesquelles entre ou sort le courant électrique.
. L'électrolyte est une solution aqueuse conductrice qui permet la circulation des ions.
Comment fonctionne la pile électrique Daniell ?
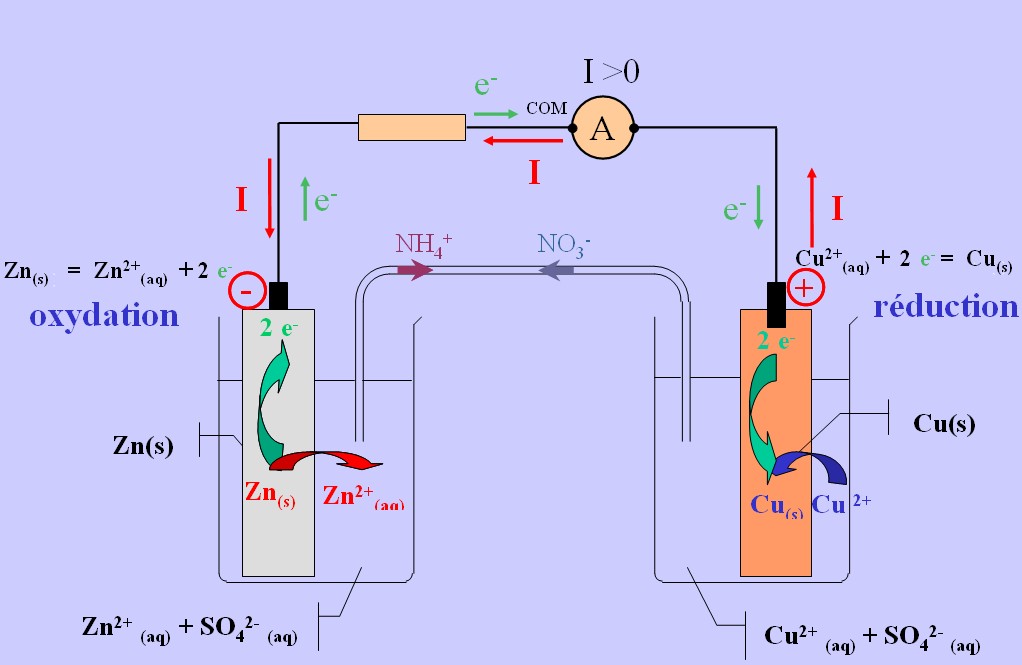
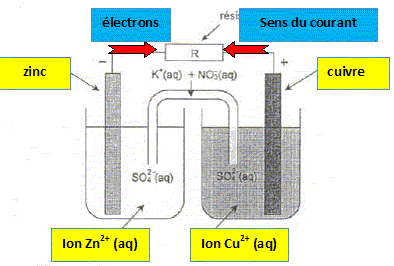
- La pile électrique Daniell est constituée d'une anode (lame de zinc plongée dans une solution contenant du sulfate de zinc) et d'une cathode (lame de cuivre plongée dans une solution contenant du sulfate de cuivre). Les deux solutions sont reliées par un pont salin (solution de chlorure de potassium ou de nitrate de potassium
Quel est le rôle de la pile Daniell ?
- Pile Daniell. Les deux solutions sont reliées par un pont salin (solution de chlorure de potassium ou de nitrate de potassium ) qui sert à équilibrer les charges.
Quelle est la résistance interne d’une pile Daniell ?
- Pour une pile Daniell avec , et à 25 °C, E est en théorie proche de 1,1 V. r est la résistance interne de la pile (en Ohm). Elle est liée à la mobilité des ions, notamment au niveau du pont salin. En travaux pratiques, les valeurs sont de l’ordre de centaines d’Ohms, ou même de .
Comment fonctionnent les piles ?
- Durant le fonctionnement de la pile, la solution de sulfate de zinc s’enrichit en ions zinc ; les ions nitrate vont donc migrer vers cette solution. En parallèle, les ions ammonium vont dans le bac de sulfate de cuivre, afin de compenser le déficit en ions +, du fait de la consommation des ions cuivre. 3. Description générale d'une pile a.
|
Chap4 Pile électrochimique et énergie chimique
On utilisera donc des plaques de cuivre et de zinc, pour réaliser 3 piles avec les 3 citrons, reliées en série avec des fils de cuivre N B Un petit buzzer fonctionne |
|
ECE : Les piles électrochimiques - Académie dOrléans-Tours
John Daniell, professeur de chimie au King's College de Londres invente en 1836 la pile qui porte aujourd'hui son nom Il s'agit d'un élément impolarisable |
|
La pile Daniell
Concours régional des olympiades de la chimie en Franche-Comté - 11 mars 2015 Page 1 sur 4 (voir dans la 3e partie pour les valeurs en cas de dosage |
|
TP N°10-PROF : LES PILES ELECTROCHIMIQUES - Physagreg
Chimie Prof 1 TP N°10-PROF : LES PILES ELECTROCHIMIQUES Objectifs : Dans une troisième expérience (qui peut être collective), simuler l'évolution du |
|
10-Les piles électrochimiques - Physagreg
Chimie 2 2) Exemple : la pile Daniell : Voir TPχn°10 Expérience 2 3) Constitution d'une pile : ➢ Chaque pile électrochimique est constituée de deux demi-piles |
|
Fiche pédagogique enseignant CHIMIE Les piles électrochimiques
CHIMIE Jean-Paul Bel, Institut universitaire de formation des maîtres, Université Montpellier II Dans une troisième expérience, on construit plusieurs piles et on étudie les facteurs qui influencent la valeur c'est la fém de la pile Daniell |
|
Chapitre 2 : Les piles électrochimiques I Quels sont les - Eklablog
c) des fils et une résistance III Comment fonctionne une pile électrochimique ? Prenons l'exemple de la pile Daniell (Zinc – Cuivre) Pont salin (s) Cu (s) Zn 2 |
|
Les Piles
pour l'établissement des lois de l'électricité et de la chimie Dans la pile de Daniell, le système oxydo-réducteur sur l'électrode de cuivre est I GILLET, La pile à combustion électrochimique : une ouverture sur le 3ème millénaire, Bull |
|
FCUP - DAEU B - Chimie
CHIMIE COURS PILES CLAIRE Y – Juin 2002 1/17 Formation Continue Université de La pile Daniell comporte deux compartiments correspondants aux deux couples utilisés * dans un Anode : Al + 3e - ----> Al x 2 - Cathode : O 2- |
|
C4 Activité 3 - Les piles
En prenant exemple sur les schémas des piles salines et alcalines, la plaque de zinc dans la pile Daniell est- elle l'anode ou la cathode ? Et la plaque de cuivre |