LA PILE ELECTROCHIMIQUE 3ème Physique
|
3ème 21/02/2013
21 fév 2013 · Epreuves communes de Sciences-Physiques Physiques Physiques Collège Laurent veut réaliser une pile électrochimique Parmi les schémas qu |
|
Chapitre 3 :Oxydoréduction
II Piles électrochimiques œ potentiel redox A) Pile électrochimique On considère une réaction d'oxydoréduction qui se produit dans une cellule constituée de |
|
Séquence 7 : piles électrochimiques
Séquence 7 – piles électrochimiques Collège des Tilleuls – Annecy Page 1 sur 5 Physique - Chimie Séquence 7 : piles électrochimiques Cours niveau troisième |
C'est quoi une pile électrochimique ?
Une pile électrochimique est le siège d'une réaction d'oxydoréduction spontanée (c'est à dire naturelle) entre deux couples redox.
Elle permet la conversion de l'énergie chimique en une autre forme d'énergie.Comment fonctionne une pile électrochimique ?
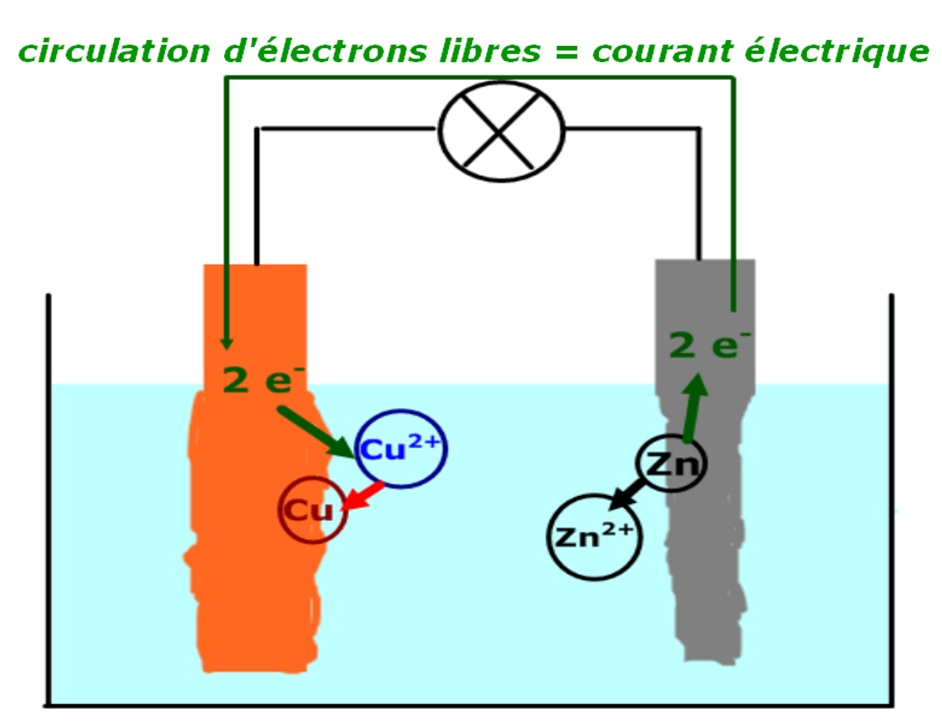
Le fonctionnement d'un générateur électrochimique se base sur le transfert spontané et indirect d'électrons (charges électriques) issus de deux réactions d'oxydoréduction se produisant dans deux compartiments séparés.
Quel est le schéma de la pile ?
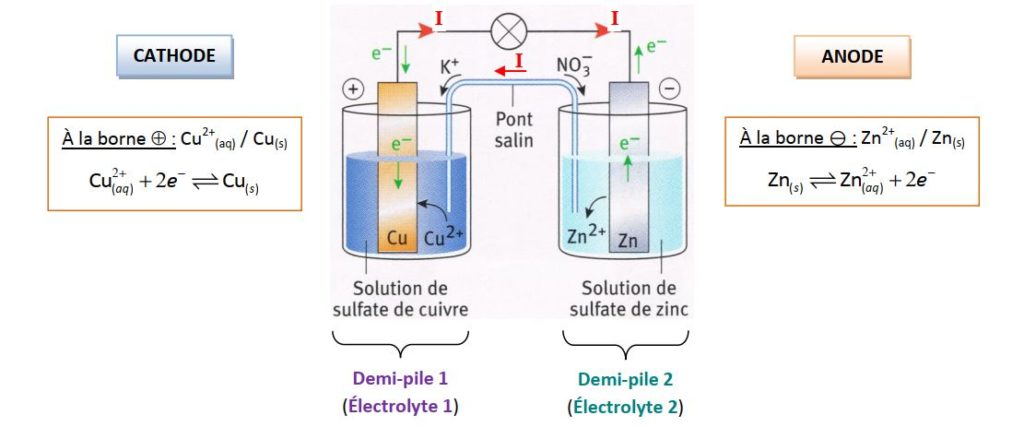
Le courant électrique circule en sens inverse des électrons, c'est-à-dire du pôle (+) (cathode) vers le pôle (–) (anode).
L'écriture symbolique d'une pile est : (–) Réd1/Ox1//Ox2/Réd2 (+).- La pile est composée de deux électrodes – un pôle positif (ou cathode) et un pôle négatif (ou anode) – plongées dans une solution faisant office de conducteur.
Lorsque ces électrodes sont reliées par un fil conducteur à un consommateur électrique, une ampoule par exemple, cela ferme le circuit.
| TP N°10-PROF : LES PILES ELECTROCHIMIQUES - Physagreg |
| 3 3C3D1I13CH14 Notions Pile électrochimique et énergie |
| Séquence 7 : piles électrochimiques |
| Niveau 3 - Pierron |
| Etude et réalisation dune pile électrochimiquepdf |
| 3ème 21/02/2013 - Collège Les Hautes Rayes |
| Physique-Chimie |
| Les piles électriques et lénergie chimique - Blogpeda |
| Chapitre 3 :Oxydoréduction - Melusine |
| Sentraîner : Piles et oxydoréduction Exercice - Lycée Ismael Dauphin |
Qu'est-ce qu'une pile électrochimique ?
. Les cellules électrochimiques fournissent les moyens de contrôler les réactions d'oxydoréduction.
Comment fonctionne une pile electrolytique ?
. Elles sont reliées au circuit électrique, par lesquelles entre ou sort le courant électrique.
. L'électrolyte est une solution aqueuse conductrice qui permet la circulation des ions.
Quels sont les 3 éléments essentiels qui constituent une pile ?
Quel est le principe de fonctionnement de la pile ?
. Il se produit dans une pile une réaction d'oxydation-réduction.
. Pour que cette réaction se produise dans votre pile, il faut qu'elle dispose de deux matériaux.
. Ces deux matériaux vont générer un flux d'électrons.
Comment fabriquer une pile électrochimique?
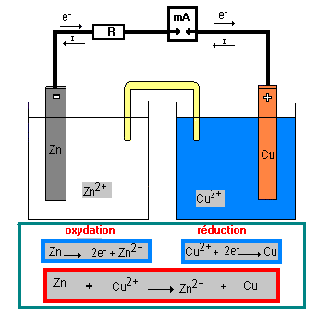
- On réalise une pile électrochimique à l'aide d'une solution de sulfate de Cuivre, d'une plaque de Zinc et d'une plaque de Cuivre et un voltmètre pour observer la tension électrique de la pile. Le voltmètre indique une tension entre les deux lames métalliques donc on a fabriqué une pile électrochimique. Si l'on branche une lampe, elle brille.
Qu'est-ce que l'énergie de la pile électrochimique?
- Cette énergie provient de la transformation de l'énergie chimique contenue dans les réactifs de la pile électrochimique. Quand un des réactifs de la pile est entièrement consommé, la tension entre les deux lames devient nulle.
Quelle est l’équation de la réaction de fonctionnement d’une pile?
- Les électrons venant du circuit extérieur sont captés par l’oxydant. L’équation de la réaction de fonctionnement de la pile correspond à la combinaison des deux réactions électrochimiques. La capacité électrique d’une pile est égale à la charge électrique maximale que la pile peut fournir durant toute sa durée de fonctionnement. 1.
Qu'est-ce que la capacité d'une pile ?
- La capacité d’une pile est la charge électrique totale qu’elle est capable de délivrer au cours de sa vie, de durée de fonctionnement . s’exprime en Coulomb, ou en Ampèreheure (Ah). Par définition, un ampèreheure est la charge électrique qui a transité dans un circuit alimenté pendant 1 heure avec un courant de 1 Ampère. En conséquence, .
|
Chap4 Pile électrochimique et énergie chimique
On utilisera donc des plaques de cuivre et de zinc, pour réaliser 3 piles avec les 3 citrons, reliées en série avec des fils de cuivre N B Un petit buzzer fonctionne |
|
ECE : Les piles électrochimiques - Académie dOrléans-Tours
Royale de Physique à Londres, le 20 mars 1800, Alessandro Volta (1745 – 1827 ) relate les expériences qui lui ont permis de réaliser la pile qui porte son nom : |
|
Les piles électrochimiques - MMorin
Énergie électrique Page 3 2) Pourquoi une pile s'use t-elle ? Voir diaporama Expérience de cours : Observations : Que devient la plaque de zinc ? La plaque de |
|
EXERCICE DE REMÉDIATION - CHIMIE - Physique Chimie Dijon
D1 I1 3 CH14 Notions Pile électrochimique et énergie chimique Capacité Extraire des informations d'un ensemble de documents Pré-requis / connaissances |
|
TP N°10-PROF : LES PILES ELECTROCHIMIQUES - Physagreg
Montrer qu'une pile délivre un courant en circuit fermé Utiliser Dans une troisième expérience (qui peut être collective), simuler l'évolution du comportement |
|
Sequence 7 - piles électrochimiques - élève
Physique - Chimie Séquence 7 : piles électrochimiques Cours niveau troisième Objectifs : - Savoir qu'une pile est un réservoir d'énergie chimique |
|
Piles électrochimiques et énergie chimique - Chapitre 1 : Le circuit
Eric Fourel, certifié de sciences physiques 2008 Chapitre 5 : Piles électrochimiques et énergie chimique Les métaux sont victimes de réactions chimiques |
|
Différentes piles électrochimiques pour différents usages - Région
La qualité de la rédaction sera également prise en compte Page 1 Test académique 3 ème de Physique-Chimie 2015-2016 – |
|
Ressources pour la classe de troisième - Espace pédagogique
A1 5 Pile électrochimique et énergie chimique A1 5 1 Principe l'enseignement des sciences physiques et chimiques fondamentales et appliquées |
|
LA RÉALISATION DUNE PILE ÉLECTROCHIMIQUE - Free
Réaliser une pile électrochimique et modéliser son fonctionnement Situation de départ et non des piles sciences physiques et chimiques – Première S |