cinétique chimique exercices corrigés terminale s
Quels sont les 3 principaux facteurs cinétiques ?
En conséquence, un facteur cinétique modifie la durée d'évolution d'un système chimique.
Plusieurs facteurs cinétiques peuvent être envisagés comme la température, la pression et la concentration des réactifs.Comment comprendre la cinétique chimique ?
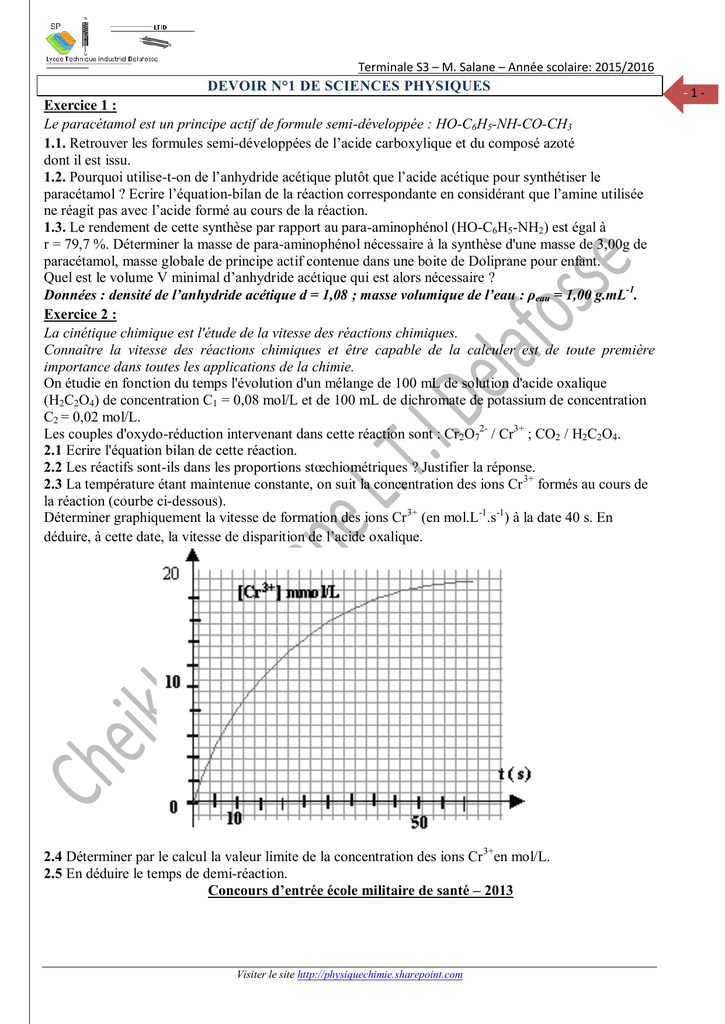
La cinétique chimique est l'étude de la vitesse des réactions chimiques.
Une réaction est dite rapide lorsque l'évolution du système est si rapide qu'à nos yeux.
La réaction semble achevée à l'instant où les réactifs entre en contact.Comment savoir si une réaction est d'ordre 0 1 ou 2 ?
Si on double la concentration d'un réactif, la réaction est : - d'ordre 0 si on n'observe aucun effet sur la vitesse - d'ordre 1 si la vitesse double - d'ordre 2 si la vitesse quadruple.
Lorsqu'on connaît l'ordre de réaction de chacun des réactifs, il devient possible de calculer la constante de vitesse k.L'unité de la constante de vitesse k peut être déterminée par une analyse dimensionnelle (la dimension d'une grandeur se note entre crochets).
Ainsi, [k] = T-1 (T : symbole dimensionnel d'un temps).
Nous pouvons en déduire que, pour une réaction d'ordre global n = 1, l'unité usuelle de k est : s-1.
|
Fiche dexercices 10 : Cinétique chimique
1/6. Fiche d'exercices 10 : Cinétique chimique. Physique – Chimie terminale S obligatoire - Année scolaire 2017/2018. Fiche d'exercices 10 : Cinétique |
|
Thème : Cinétique chimique Fiche 5 : Vitesse de réaction
LE TALENT C'EST D'AVOIR ENVIE. CHIMIE. Série S. Nº : 37005. Fiche Corrigés. Thème : Cinétique chimique. Fiche 5 : Vitesse de réaction. ? Exercice n°1. |
|
Exercices de révisions : Physique-chimie
Exercice n°3 : Quantité de matière et tableau d'avancement. Il s'agit de la réaction de combustion du 11-diméthylhydrazine avec pour comburant |
|
Cinétique Chimique
2°/ Etablir l'expression donnant la variation de la concentration en fonction du temps. 3°/ Calculer la constante de vitesse k. Page 45. Correction Ex2:. |
|
Lycée Kounoune Classe Tle S Série dexercices de chimie 2015
Lycée Kounoune Classe Tle S Série d'exercices de chimie 2015/2016 prof : M.DIAGNE. C4 : CINETIQUE CHIMIQUE. Lycée de Kounoune C4 : CINETIQUE CHIMIQUE prof |
|
Exercices: CINÉTIQUE CHIMIQUE CORRECTION
EXERCICE 10 p.94: TEMPERATURE COMME FACTEUR CINETIQUE. 1. Il s'agit d'une réaction d'oxydoréduction. On écrit les deux demi équations associées à chacun des. |
|
HATIER prof
Chapitre 4 • Cinétique chimique Exercices 1 à 21 corrigés à la fin du manuel de l'élève. ... vA(I2)(5 min) = 46 × 10–6 mol·L–1·min–1. Exercice 26 ... |
|
Thème : Cinétique chimique Fiche 5 : Vitesse de réaction
CHIMIE. Série S. Nº : 37005. Fiche Exercices. ? Exercice n°1. Une transformation chimique est étudiée dans deux conditions différentes et on obtient le |
|
Exo-PC-Terminale-S.pdf
ET CHIMIE DE. LA CLASSE DE TERMINALE S ... PREMIERE PARTIE : EXERCICES CORRIGES DE CHIMIE. ... Donner quelques applications de la cinétique chimique. |
|
Chimie (problèmes et exercices) Indice 540.76 Nombres de Titres
chimiques : rappels de cours exercices corrigés. Gruia |
|
Thème : Cinétique chimique Fiche 5 : Vitesse de - Studyrama
Série S Nº : 37005 Fiche Corrigés Thème : Cinétique chimique Fiche 5 Exercice n°1 |
|
Terminale S - Cinétique chimique - Fiche de cours
e 1 1/6 Cinétique chimique - Exercices Physique – Chimie terminale S obligatoire - Année |
|
Exercices : cinétique macroscopique corrigés
e 3 : loi d'Arrhénius Svante Arrhénius La constante de vitesse de la réaction 2 N2O5(g) → 4 |
|
Exercices – Cinétique chimique
→ Quel est l'ordre de cette réaction ? 2) Calculer la concentration initiale en CrO2+ 2 ? 3) Déterminer le |
|
TERMINALE S Cinétique chimique
LE S CHAP 2 TP SPECTROPHOTOMETRIE CORRECTION manipulation 1 : courbe d' |
|
Cinétique chimique_exercices - Chimie - PCSI
QUE CHIMIQUE EXERCICES Chapitre 1 1 LOI D'ARRHENIUS L' expérience montre que, à la |
|
Exercices corrigés - TuniSchool
es corrigés : La vitesse d'une réaction chimique Page 1 sur 3 WWW TUNISCHOOL COM |
|
Cinétique chimique - UNF3S
?tique chimique étudie la vitesse avec laquelle s'effectuent les Exprimées en mol s-1 (ou mol min-1, mol h-1) td nd )t( C Cf 7,28 103 s • Exercice 4 : 1 ordre par rapport à Br |
|
EXERCICES – SÉRIE 10 Cinétique chimique 101 La - EPFL
loi de vitesse de la réaction 2 A → B est d'ordre 2, avec k = 1,24· ml· mol– 1· s–1 Calculer le temps |