oxydant fort
|
PRECAUTIONARY STATEMENTS PERASAN MP-2 (ANTIMICROBIAL SOLUTION
Agent oxydant fort Corrosif Mélanger seulement avec de l'eau Le produit doit être dilué selon les directives de l'étiquette avant son utilisation Ce produit n'est pas combustible Par contre à des températures supérieures à 69 °C une décomposition se produit libérant de l'oxygène |
|
PRECAUTIONARY STATEMENTS PERASAN® MP-2C OXIDIZER!
Agent oxydant fort Corrosif Mélanger seulement avec de l'eau Le produit doit être dilué selon les directives de l'étiquette avant son utilisation Ce produit n'est pas combustible Par contre à des températures supérieures à 69 °C une décomposition se produit libérant de l'oxygène |

OXYDANT et RÉDUCTEUR ✔️ Vocabulaire 1ère spé Physique Chimie

Oxydoréduction

LES ANTIOXYDANTS ET LE STRESS OXYDANT CEST QUOI ?
|
CLASSE 5 LES SUBSTANCES OXYDANTES
Un oxydant puissant sera le plus souvent un comburant. Par conséquent en présence d'un combustible même très peu dangereux |
|
Dangers des oxydants forts
Le permanganate de sodium est un oxydant fort et la substance projetée L'usine où se produisit l'incident manipulait à la fois des agents oxydants (tel. |
| ANNEXE POTENTIEL ET POUVOIR OXYDANT ECHELLE DE |
|
Oxydo-réduction - 1°) Couple oxydant- réducteur 1.1)Réaction entre
l'oxydant et le réducteur. Ces différentes réactions sont spontanées et font passer des partenaires forts aux partenaires faibles. Bernaud J. |
|
Chimie - Chapitre 9 : Réactions doxydoréduction Ce quil faut retenir…
Un oxydant est un élément capable de capter un ou plusieurs électrons. Un oxydant est d'autant plus fort que son E° est grand. |
|
Chapitre 4 Oxydo-réduction
Couple oxydant / réducteur et demi-équation électronique Un oxydant est d'autant plus fort qu'il capte facilement des électrons et que le potentiel ... |
|
6 Répartition des métabolismes dans la biosphère actuelle 6.1.Lien
les oxydants les plus forts (ceux des couples présentant les plus fort p?). Cela implique aussi que la séquence des réactions d'oxydation est contrôlée par |
|
Les oxydations
Le réactif de Jones H2CrO4 est un oxydant fort obtenu en milieu très acide. Ces conditions ne sont pas forcément compatibles avec toutes les molécules. De. |
|
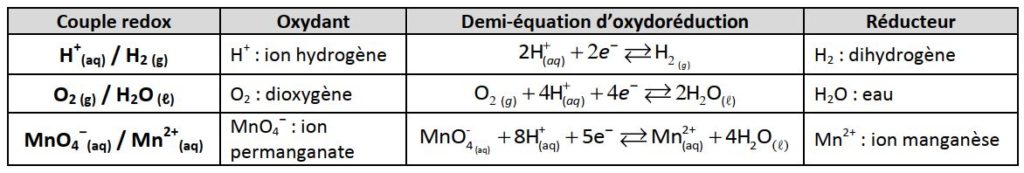
Oxydant Réducteur E0 (Volt)
Table des potentiels standard Ox+ne-?Red à 25°C et à p=101kPa. Oxydant. Réducteur E0 (Volt). F2+ 2 H+ +2 e-. 2HF. 3.05. F2+2 e-. 2F-. 2.87. |
|
LES RÉACTIONS DOXYDORÉDUCTION
Le réducteur fort lui est oxydé et devient un oxydant plus faible. Equation bilan : Rd1 + Ox2 ? Rd2 + Ox1. Les couples Ox1/Rd1 et Ox2/Rd2 forment |
|
Searches related to oxydant fort PDF
Authors: Ranvir Suvartan Gautam Mayur Thul and Navan Sampath Kumar Page 4 of 8 Version 1 0 Since we update this document frequently we request you to download a fresh copy each time |
Quels sont Les Agents Oxydants?
Dans la demi-réaction d'oxydation, l'agent oxydant est réduit car, lors de la réception d'électrons de l'agent réducteur, une diminution de la valeur de charge ou du nombre d'oxydation de l'un des atomes de l'agent oxydant est induite. Cela peut s'expliquer par l'équation suivante: 2Mg (s) + O2(g) ? 2MgO (s) On peut voir que le magnésium (Mg) réagi...
Quels Facteurs définissent La Force d'un Agent Oxydant?
Ces espèces se distinguent par leur "force". C'est-à-dire que les plus faibles sont ceux qui ont une capacité inférieure à soustraire des électrons d'autres substances. En revanche, les plus forts ont plus de facilité ou de capacité à "arracher" ces électrons. Pour sa différenciation, les propriétés suivantes sont considérées:
Les Oxydants Les Plus Forts
Compte tenu de ces paramètres des éléments chimiques, il est possible de déterminer quelles sont les caractéristiques que doivent avoir les meilleurs agents oxydants: une électronégativité élevée, un rayon atomique faible et une énergie d’ionisation élevée. Cela dit, il est considéré que les meilleurs agents oxydants sont les formes élémentaires de...
Exemples de Réactions avec Des Agents Oxydants
Dans certaines réactions redox il est plus facile de visualiser le transfert d'électrons dans l'autre. Ci-dessous, nous vous expliquerons certains des exemples les plus représentatifs:
Quels sont les agents oxydants forts?
Ce produit est stable. Ce produit est incompatible avec ces substances: Les agents oxydants forts: perchlorates, les peroxydes, les hypochlorites, les nitrates (ag, hg), l'acide nitrique, l'acide chromique. Pentafluorure de brome, le chlorure d'acetyle, les oxydes de chlore.
Qu'est-ce que l'agent oxydant?
Agent oxydant - le réactif qui gagne des électrons. L'agent oxydant contient l'élément qui est réduit (gagne des électrons). Si une substance gagne facilement des électrons, on dit qu'elle est un agent oxydant fort. Notez que le nombre d'oxydation de C va de +2 à gauche à +4 à droite.
Qu'est-ce que le stress oxydant ?
Le stress oxydant se définit comme l'incapacité de l'organisme de se défendre contre les espèces réactives de l'oxygène (ERO) en raison de la perturbation d'équilibre endogène entre ces derniers et les agents oxydants (AO). Ce déséquilibre conduit potentiellement à des dégâts structuraux et fonctionnels.
Quels sont les différents types d'agents oxydants ?
Dans ces réactions, deux substances interagissent: l'agent réducteur et l'agent oxydant. Certains des agents oxydants que l'on peut observer plus fréquemment sont notamment l'oxygène, l'hydrogène, l'ozone, le nitrate de potassium, le perborate de sodium, les peroxydes, les halogènes et les composés à base de permanganate.
| Experimental research on inactivation of bacteria and fungi |
| Chapitre 4 : LES REACTIONS D’OXYDO-REDUCTION |
| Acide nitrique - CF Industries |
| Aldon Corporation |
|
Dangers des oxydants forts - AIChE
Le permanganate de sodium est un oxydant fort et la substance projetée L' usine où se produisit l'incident manipulait à la fois des agents oxydants (tel |
|
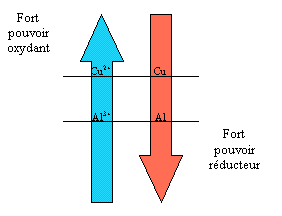
ANNEXE POTENTIEL ET POUVOIR OXYDANT ECHELLE DE
Tous les couples d'oxydant-réducteur s'écrivent sous la forme Ox/Red Ils sont classés de l'oxydant le plus fort au plus faible, ou du réducteur le plus faible au plus |
|
Classification qualitative des couples oxydant réducteur - Fastef
Le dihydrogène est un réducteur plus faible que le fer et le zinc mais plus fort que le cuivre Dans la classification électrochimique, le couple H+/H2 est donc situé |
|
REACTIONS DOXYDATION ET DE REDUCTION
Les conventions suivantes ont été utilisée: Description de la réaction du couple : OXydant + n e- REDucteur E° = [ V] Signe de E° : Plus l'oxydant est fort, |
|
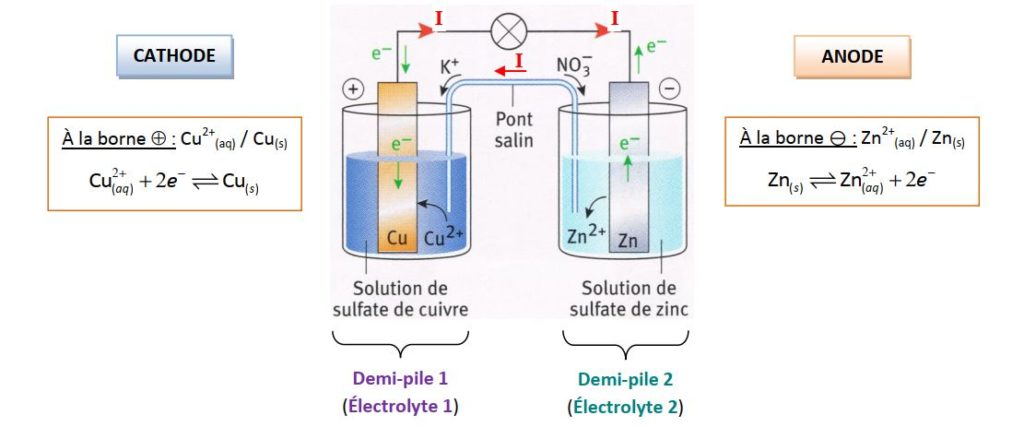
1°) Couple oxydant- réducteur 11)Réaction entre union métallique
Ce sont les ions Cu2+ qui provoque l'oxydation du Zinc, ils sont dit oxydants Oxydant le plus fort des 2 couples et Réducteur le plus fort des 2 couples |
|
Les peroxydes et leur utilisation - INRS
qu'elle contient environ 3 en poids de peroxyde d'hydrogène PROPRIÉTÉS CHIMIQUES H2O2 est un oxydant fort et il se décompose sous l'action de la |
|
Chapitre 3 :Oxydoréduction
L'oxydant est d'autant plus fort que E augmente ; le réducteur est d'autant plus fort que E diminue Réaction Ox1 + Red2 Ox2 + Red1 quantitative De façon |
|
Oxydoreduction - Lycée Ismael Dauphin
Dans une réaction d'oxydoréduction, l'espèce chimique oxydante est réduite Exercice 2 Parmi ces couples, quel est l'oxydant le plus fort ? le réducteur le |
|
Chimie - Chapitre 9 : Réactions doxydoréduction Ce quil faut retenir
La réaction se fait toujours entre l'oxydant du couple ayant le potentiel initial le plus fort et le réducteur du couple ayant le potentiel initial le plus faible (Sens du |