enthalpie de dissolution formule
|
6 Propriétés des solutions
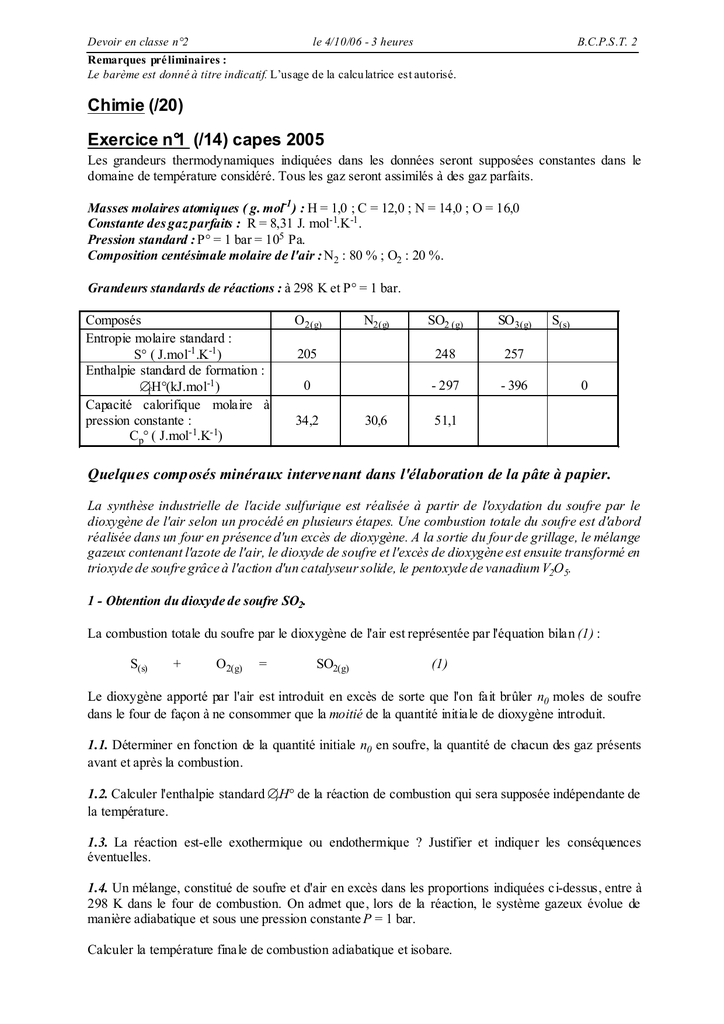
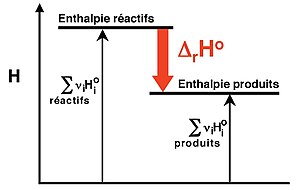
Enthalpie de dissolution La chaleur libérée ou absorbée par mole lorsqu’une substance se dissout à P = cste pour former une solution très diluée est appelée enthalpie de dissolution et est notée dans les conditions standard ΔH0sol Le phénomène de dissolution peut être vu comme la succession de deux étapes |
|
Solvatation
calcul d'enthalpies standard de dissolution de sels ioniques Exemples de TP : Détermination de l'enthalpie standard de dissolution du nitrate d'ammonium par calorimétrie; Détermination de l'enthalpie standard de dissolution de l'acide benzoïque dans l'eau par titrage colorimétrique blanc Introduction |
|
TP N°1 : Détermination expérimentale des Enthalpies de réaction
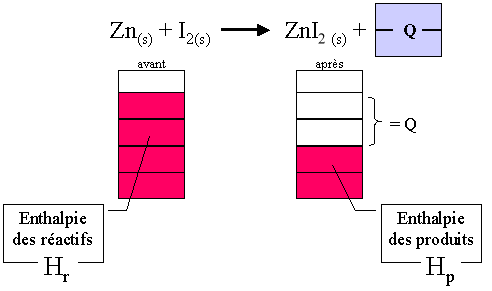
On appelle une enthalpie de dissolution la chaleur qui accompagne la dissolution d’une mole d’une substance présente dans une quantité déterminée d’un solvant ∆Hd= n Q Remarque Si un système dégage de la chaleur son enthalpie diminue (∆H0 |
|
TP: 2 L’ENERGIE DE DISSOLUTION
TP: 2 L’ENERGIE DE DISSOLUTION 5 *Déterminer l’enthalpie de dissolution de H2SO4 : Q 1 = c 1 m 1 (Teq - T1) Q cal = c cal m cal (Teq - T1) c cal m cal = C cal Donc : Q cal = C (Teq - T1) Et on a : ΔHd+ Q eau+ Q cal = 0 ΔHd + c m 1 (Teq - T1) + C cal (Teq – T1) = 0 |
Qu'est-ce que l'enthalpie de dissolution ?
La chaleur libérée ou absorbée par mole lorsqu’une substance se dissout à P = cste pour former une solution très diluée est appelée enthalpie de dissolution, et est notée dans les conditions standard ΔH0sol .
Comment calculer l’enthalpie d’hydratation d’un sel ?
ΔHF = - ΔHd × M / m 4/Détermination de l’enthalpie d’hydratation d’un sel : Premièrement, on prend 100 ml d’eau à l’aide de l’éprouvette graduée, puis mettre l’eau dans le calorimètre, on obtient la température initiale (T1) de l’eau et du calorimètre (T1 = 21°C = 294 k°)
Comment calculer l’enthalpie ?
Enthalpie, fonction d’état, notée H, intervenant dans le premier principe de la thermodynamique. L’enthalpie est définie par l’expression : H = U + PV où U correspond à l’énergie interne du système, P à la pression et V au volume du système. On utilise aussi fréquemment l’expression de l’enthalpie sous sa forme différentielle : dH = dU + PdV + VdP.
Quelle est l’enthalpie de dissolution de NaCl ?
Le tableau de la page précédente montre que la dissolution de NaCl, par exemple, est un processus endothermique. De même, dans le cas du nitrate de potassium KNO3, un sel pourtant très soluble, l’enthalpie de dissolution est de ΔH0sol = + 35 kJ⋅mol–1.

Enthalpies of Formation

Enthalpie formules et démonstrations

TP 1: Enthalpie de Dissolution dun sel (KCl)
|
6. Propriétés des solutions
ΔSsol > 0 permet donc de compenser une enthalpie de dissolution ΔHsol positive en aboutissant à une enthalpie libre ΔGsol < 0 tiennent pas et l'équation de ... |
|
TP N°1 : Détermination expérimentale des Enthalpies de réaction
Cette équation d'échange est appelée équation calorimétrique. I On appelle une enthalpie de dissolution la chaleur qui accompagne la dissolution d'une mole. |
|
[CH1] Détermination dune enthalpie dhydratation par calorimétrie
Définir hydratation (+ processus physico-chimique associés + formule de CaCl2 2H2O) Écart enthalpie dissolution ? Approximation d'Ellingham |
|
Thermodynamique de la solvatation dacides protoniques et des
Enthalpie de dissolution et enthalpie de transfert des espkces. Toutes les nous ont fait prtftrer le calcul par la formule [7]. Ce calcul nous permet ... |
|
La chaleur de dissolution dun sel dans leau Exercice résolu
1) Équation de dissolution du sel dans l'eau. NaNO3 (s). → eau. Na+. (aq). + NO3. -. (aq). ∆H= ? (kJ/mol). 2) La dissolution du sel dans l'eau occasionne une |
|
Bilans thermiques
L'enthalpie de dissolution molaire de. Na2SO4 10 H2O à 10 °C est de 78 |
|
Les dosages acido-basiques
Enthalpie de dissolution (en kJ.mol-1) dans l'eau en excès à 298.15 K. Nom. Formule. Etat physique. 0. H. ∆. A. HClO4 (l). -888 acide perchlorique. HClO4 |
|
Étude de la solubilité de lacide benzoïque dans leau en fonction de
On remarque que l'enthalpie de dissolution ne dépend pratiquement pas de la présence de sel dans la solution. Variation de la solubilité avec la présence de sel. |
|
Enthalpie et énergie de liaison
Mais cela suppose connaître la formule éclatée des molécules (Lewis). Page 4 L'enthalpie de dissolution sera donc très faible. La dissolution de NaCl ... |
|
N°/version 1.1 Nom du minéral : Gibbsite Mécanisme : Précipitation
16 janv. 2012 dissolution (k utilisée dans l'équation 1) est égale à : ... Dans le cas d'une dissolution les vitesses sont indépendantes de l'enthalpie libre ... |
|
Oxydo-réduction et pile : commentaires scientifiques décrivant les
DETERMINATION DE L'ENTHALPIE DE DISSOLUTION. ENDOTHERMIQUE DE NH4NO3(s). Données expérimentales. Lors de la dissolution du NH4NO3(s) dans. |
|
Thermodynamique de la solvatation dacides protoniques et des
Nous avons mesurk i 25°C les enthalpies de dissolution des acides acktique benzoi'que et nous ont fait prtftrer le calcul par la formule [7]. Ce calcul. |
|
Bilans thermiques
d'eau à 20 °C sachant que l'enthalpie de dissolution de NaOH est de – 425 La glycine possède la formule suivante : H2N-CH2-CO2H (M = 75 g.mol–1). |
|
Les dosages acido-basiques
Enthalpie de dissolution (en kJ.mol-1) dans l'eau en excès à 298.15 K. Nom. Formule Formule. Etat physique. 0. H. ? chlorure d'étain (II). SnCl2 (s). |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
CHAPITRE IV : REACTIONS DE DISSOLUTION-PRECIPITATION ?rHT est l'enthalpie de réaction à la température T par unité d'avancement (pour ? =1mol). IV.5.3. |
|
Détermination de lenthalpie standard de formation de lion
Calorimétrie adiabatique ion tétrahydroxoaluminate (III) |
|
Exemples denthalpies standard
Notée ?fHo ; elle correspond à l'enthalpie standard de formation d'un corps composé par la réaction de formation de ce corps à partir des éléments pris |
|
Dissolution du dioxyde de carbone dans des solutions aqueuses d
Cette thèse porte sur l'étude de l'enthalpie de dissolution du dioxyde de termes de composition du flux de CO2 injecté seront formulées de manière à ... |
|
THÈSE PRÉSENTÉE À LUNIVERSITÉ DU QUÉBEC À CHICOUTIMI
11 mai 2015 Bien que l'enthalpie de dissolution de l'alumine ? soit moins ... La MDF est simple à formuler et a un temps de calcul raisonnable. |
|
Étude de la solubilité de lacide benzoïque dans leau en fonction de
que l'on peut dissoudre dans un volume donné de solvant. Par définition : s = [PhCOOH]aqueux et ?rH° : enthalpie standard de la réaction de dissolution. |
|
6 Propriétés des solutions - EPFL
Enthalpie de dissolution La chaleur libérée ou absorbée par mole lorsqu’une substance se dissout à P = cste pour former une solution très diluée est appelée enthalpie de dissolution et est notée dans les conditions standard ?H0sol Le phénomène de dissolution peut être vu comme la succession de deux étapes |
|
TP N°1 : Détermination expérimentale des Enthalpies de réaction
On appelle une enthalpie de dissolution la chaleur qui accompagne la dissolution d’une mole d’une substance présente dans une quantité déterminée d’un solvant ?Hd= n Q Remarque Si un système dégage de la chaleur son enthalpie diminue (?H0 |
|
Exemples d’enthalpies standard - Le Mans University
On peut calculer une grandeur de réaction en connaissant les grandeurs standard de formation des produits et des réactifs Exemple : • combustion de l’acide éthanoïque ; calcul de la variation d’enthalpie de la réaction : CH3COOH (l) + 2 O2(g) ? 2 CO2(g) + 2 H2O(l) ?rH o= 2 ? |
|
EXERCICES DE CHIMIE GÉNÉRALE Série 11 - Université de Genève
Utilisez la valeur obtenue pour déterminer l’enthalpie d’hydratation de Rb+ sachant que l’enthalpie de dissolution de RbBr est de +22 kJ/mol et que son enthalpie réticulaire est 651 kJ/mol Exercice 2 On dissout 1 05 g d’un composé inconnu dans 100g de CCl4 Le point d’ébullition normale de la solution est de 61 51°C ; le point |
|
Searches related to enthalpie de dissolution formule PDF
L’enthalpie H d’un système est définie par : H = U + PV PV terme correspondant à l’énergie d’expansion ou de compression du système H toujours supérieur à U |
Qu'est-ce que l'enthalpie de dissolution?
Enthalpie de dissolution La chaleur libérée ou absorbée par mole lorsqu’une substance se dissout à P = cste pour former une solution très diluée est appelée enthalpie de dissolution, et est notée dans les conditions standard ?H0sol.
Comment calculer l’enthalpie standard d’une réaction ?
Si une réaction peut être écrite sous la forme d’une combinaison linéaire de plusieurs équations-bilans de réactions, l’enthalpie standard de cette réaction à une température T s’obtient à partir des enthalpies standard des différentes réactions à la même température par une combinaison linéaire faisant intervenir les mêmes coefficients.
Qu'est-ce que le phénomène de dissolution?
Le phénomène de dissolution peut être vu comme la succession de deux étapes virtuelles : Dans la première, les ions ou les molécules du solide doivent vaincre leur attraction réciproque et rompre la cohésion du solide pour se séparer.
Comment calculer l’enthalpie de formation ?
2. Détermination expérimentale: cycle de Born Haber Sur l’exemple de KCl : On construit deux chemins différents menant du même état initial K(s) + 1/2Cl2(g) au même état final KCl(s).Le premier direct correspond à l’enthalpie de formation ; le deuxième indirect correspond à différentes enthalpies mesurables.
| TP N°1 : Détermination expérimentale des Enthalpies de réaction |
| Exemples d’enthalpies standard - Le Mans University |
| SOLUBILITE / PRECIPITATION |
| TP: 2 L’ENERGIE DE DISSOLUTION - archiveorg |
| Université du Maine - Faculté des Sciences Retour ) dans l |
| Détermination de l’enthalpie standard de formation de l’ion |
| Searches related to enthalpie de dissolution formule filetype:pdf |
|
Tp12 - calorimetrie - Université de Genève
8 déc 2010 · Calculer l'enthalpie de dissolution H [J/mol] en utilisant la formule suivante : H = M m Cp, mea + Cp, ×(T − T2) msel masse du sel introduite [g] |
|
TP 12 : Calorimétrie
23 sept 2009 · On peut ensuite écrire les réactions de dissolution et calculer la chaleur de dissolution Calcul de l'enthalpie de réaction selon la formule (2) : |
|
Cours C13 Thermochimie 12 - CGDSMPSI
Il s'agit de mesurer les variations d'enthalpie et d'énergie interne d'un système thermodynamique subissant réaction chimique est la dissolution du carbonate de disodium solide (Na2CO3) dans l'eau On trouve formule Na2CO3,10 H2O |
|
Reaction chimique - Thermodynamique - Cinétique
chaleurs de combustion, de dissolution ou de changement d'états, il est L' énergie interne et l'enthalpie d'une quantité donnée de gaz parfait ne dépendent que de sa C'est le gaz parfait associé (de même formule chimique) pur et sous la |
|
Enthalpie de dissolution
Université du Maine - Faculté des Sciences ⌫ Retour Enthalpie de dissolution ( en kJ mol-1) dans l'eau en excès à 298 15 K Nom Formule Etat physique 0 |
|
£EA~R-5928- DETERMINATION DES ENTHALPIES LIBRES DE
11 4 Calcul de l'enthalpie libre de dissolution des verres dans l'eau 216 formulé plus haut avec un complexe activé purement siliceux et pourrait s'écrire |
|
Enthalpie et énergie de liaison
Cette enthalpie de dissociation est appelée énergie de liaison Mais cela suppose connaître la formule L'enthalpie de dissolution sera donc très faible |