comment savoir si c'est un acide fort ou faible
|
Fiche de révisions sur les acides et les bases
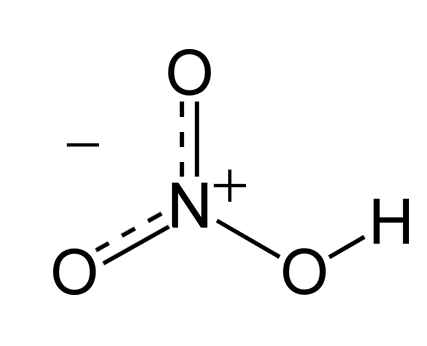
acide faible : c’est un acide dont la réaction sur l’eau n’est pas totale base faible : c’est une base dont la réaction sur l’eau n’est pas totale L’acide éthanoïque ( CH 3 C OOH) est un acide faible : H 3 C OOH ( liq) H 2 O → ← 3 O + aq |
|
D terminer si un acide est fort ou faible
On connait le pH et la concentration de la solution Pour savoir si l’acide est fort ou faible il faut : 1 Déterminer [H 3O +] par la relation [H 3O +]=10-pH ( voir fiche précédente ) 2 Comparer cette valeur à C 3 Conclure S’il y a égalité l’acide est fort S’il y a différence l’acide est faible Exemple Le chlorure d |
Quels sont les conséquences d’un acide fort dissocié ?
Conséquences (pour les concentrations habituelles : << 1 mol.L -1) : un acide fort A est totalement dissocié. Cela veut dire que toutes les molécules de A introduites dans l’eau sont totalement transformées en ions H 3 O + et en sa base conjuguée B . La réaction A + H 2 O ® B + H 3 O + est totale.
Comment savoir si un acide est fort ?
Pour les concentrations en acide habituellement rencontrées c’est à dire pour des concentrations nettement inférieures à 1 mol.L -1, on peut montrer alors que la réaction est quasi totale. Un acide A appartenant à un couple acide-base de pKa négatif sera donc totalement transformé en ions H3O+ : on dit qu’il s’agit alors d’un acide fort.
Quels sont les acides faibles ?
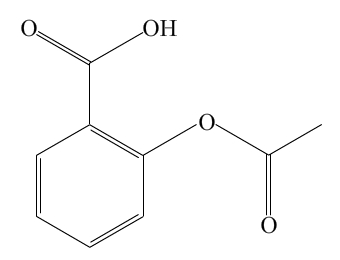
Exemple de bases faibles : les ions carboxylates (fonction ), c'est-à-dire les bases conjuguées des acides carboxyliques. • Un acide fort est un acide réagissant totalement avec l’eau. Si sa concentration est c, alors . • Un acide faible AH réagit avec l’eau selon une réaction limitée .

Quest-ce quun acide fort ? Comment le reconnaître ?

Acide FORT ou acide FAIBLE ? 🎯 Exercice BAC Chimie Chimie Terminale spécialité

Déterminer si un acide est fort ou faible
|
Déterminer si un acide est fort ou faible
|
|
Déterminer si une base est fort ou faible
|
|
Révisions sur les acides et les bases - Nicole Cortial
rev- PDF |
|
PH et pKa - Eli Zysman-Colman
|
|
Chapitre 1 Acides et bases
~vpelassaPDF |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université
docsPDF |
|
C1 : Acides & bases
|
|
VIEtude sommaire des mélanges
PDFPDF |