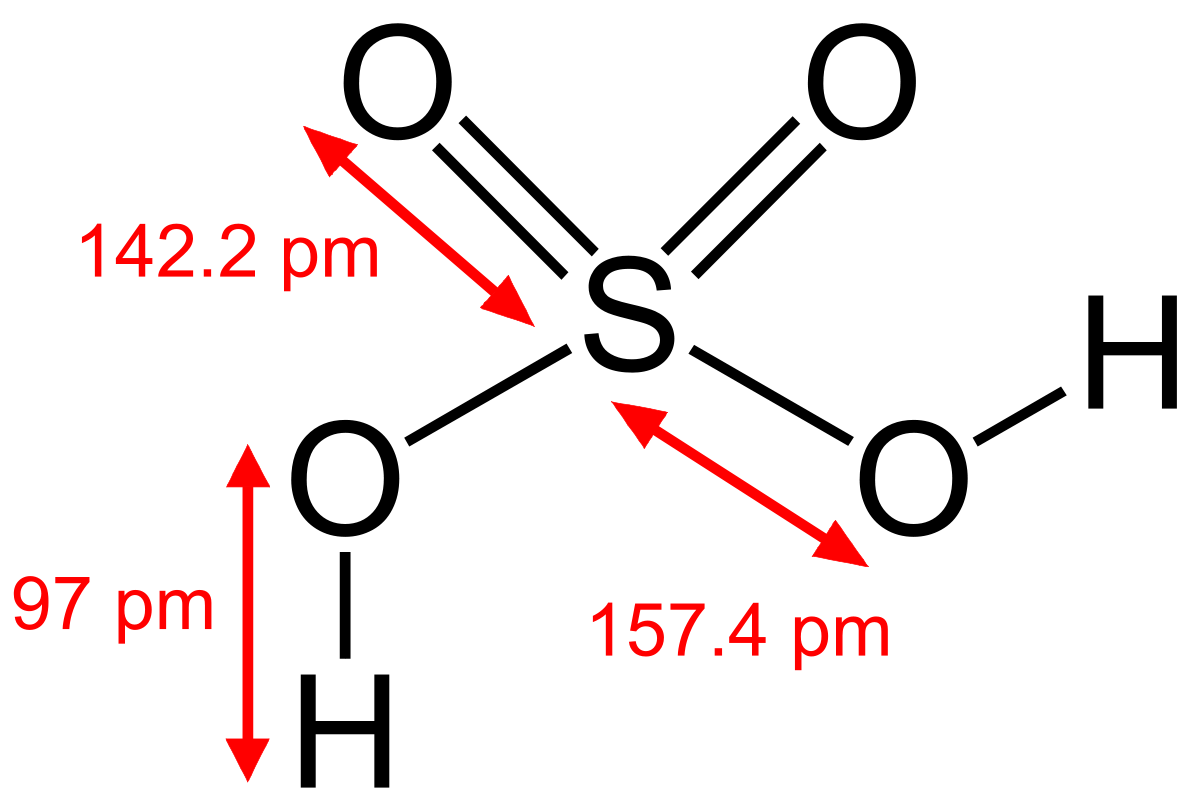
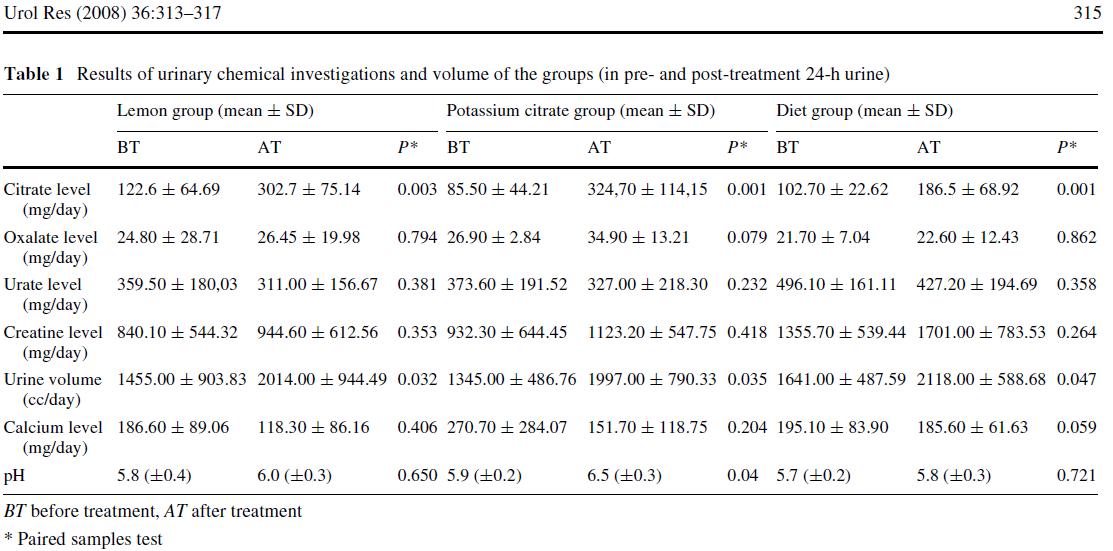
comment savoir si un acide est fort ou faible pka
Formule de calcul de pH
Formule de calcul de pH
1Pour un acide fort : pH = - log C.
2) Pour une base forte: pH = 14 + log C.
Ces formules sont valables pour les concentrations supérieures à 10-7 mol/L.
3) Pour un acide faible : pH = 1/2 pKa - 1/2log C.
4) Pour une base faible : pH = 7 + 1/2 pKa + 1/2log C. 5pH = 1/2( pKa1 + pKa2)
Comment reconnaître l'acide le plus fort ?
Ainsi, pour déterminer quel acide est le plus fort, nous devons identifier quel acide possède la plus grande valeur de �� ��.
Parmi les acides fournis, l'acide qui a la plus grande constante d'acidité est l'acide nitreux.
Par conséquent, l'acide le plus fort est l'acide nitreux, HNO2.
Comment savoir si c'est un acide fort ou faible ?
Un acide A appartenant à un couple acide-base de pKa négatif sera donc totalement transformé en ions H3O+ : on dit qu'il s'agit alors d'un acide fort.
Un acide A appartenant à un couple acide-base de pKa positif ne sera que partiellement transformé en ions H3O+ : on dit qu'il s'agit alors d'un acide faible.
|
Déterminer si un acide est fort ou faible
On connait le pH et la concentration de la solution. Pour savoir si l'acide est fort ou faible il faut : 1. Déterminer [H3O+] par la relation [H3O+]=10- |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0. Dans le cas d'un acide fort totalement dissocié dans l'eau |
|
PH et pKa
[H2O] est très grand et ~constant. Constante d'acidité. pKa = -log Ka. Plus la valeur de pKa est faible plus le Ka est grand |
|
Fiche de synthèse n°2 : réactions acido-basiques en solution aqueuse
? est une grandeur comprise entre 0 et 1. ? = 1 correspond à un acide totalement dissocié donc fort. Exemple : Pour un acide faible de pKa = 5 et C0 = 10- |
|
TD1b : Acides et bases suite
Le pKa du couple acide/base de l'éthanamine vaut 107 : pKa < pKe il s'agit donc d'une b) Pour savoir si l'acide butanoïque est un acide fort ou faible |
|
Déterminer si une base est fort ou faible
Pour savoir si la base est forte ou faible il faut : acide. Concentration ( mol.L-1 ). pH. [HO-] ( mol.L-1 ). Faible ou fort. |
|
Exercice 1 Du lait au yaourt (6pts)
L'acide lactique est-il un acide fort ou faible ? Indiquer comment faire si on veut réaliser 2000 mL de solution. 16. Le pH de la solution sera-t-il ... |
|
Dosage acide faible – base forte
devant négligé est. A. ? . Ceci implique que l'acide ne soit pas trop fort ou trop dilué pour que sa dissociation ne soit pas trop importante : 2 clog. pKa. |
|
§ 7 (suite) Titrages acide-base
La solution initiale est constitué d'une base faible. Si celle-ci n'est que faiblement protonée on aura: pH ? 7 + 1/2 { pKa + log (ca / |
|
Déterminer si un acide est fort ou faible - archimede
On connait le pH et la concentration de la solution Pour savoir si l'acide est fort ou faible, il faut : 1 Déterminer [H3O+] par la relation [H3O+]=10- |
|
Chapitre 1 Acides et bases
acide si son pH est inférieur à 7, i e [H3O+]> 10−7 mol L−1 (à faible ssi la dissociation est une réaction équilibrée ssi pKa > 0 Dans le cas La base conjuguée d'un acide fort est dite “indifférente dans l'eau”, i e cette espèce ne le cas de solutions concentrées on peut donc avoir des projections lors de la réaction, |
|
Révisions sur les acides et les bases - Nicole Cortial
acide fort : c'est un acide qui réagit entièrement avec l'eau base forte : c'est une base qui réagit totalement avec l'eau acide faible : c'est un acide dont la |
|
Les acides et bases en solution aqueuse - Groupe Transition
Echelle et table des constantes d'acidité Ka (pKa) 4 5 Coefficient d'ionisation ( de dissociation) d'un acide ou d'une base faible Pourcentage Un acide est une substance qui, en solution aqueuse, libère des ions H + ″ eau ex HCl(g) si l'acide est fort, la valeur de Ka est grande et la base conjuguée A - du couple est |
|
PH - UNF3S
Quelle est la masse de NaOH (base forte, M = 40 g mol-1) qu'il faut dissoudre pour Calculer le pH d'une solution d'un acide faible (pKa= 4,75) de concentration 1 : L'acide éthanoïque CH3COOH (pKA = 4,8) est un acide plus fort que l'ion |
|
Dosage acide faible – base forte
est A − Ceci implique que l'acide ne soit pas trop fort ou trop dilué pour que sa 1 0 x=0 5 pH=pKa AH A- dosage d'un acide faible (pKa=5, ca=0 01 mol L -1 ) L'acide est totalement neutralisé si il n'est pas trop faible La solution à |
|
Cours 5 - Equilibres Acido-basiques
Savoir calculer le pH d'une solution acide faible: un acide est fort si sa réaction d'ionisation peut être considérée Acides négligeables Echelle de pKa : pH 0 14 Bases fortes Bases faibles Si l'acide est suffisamment faible donc peu |