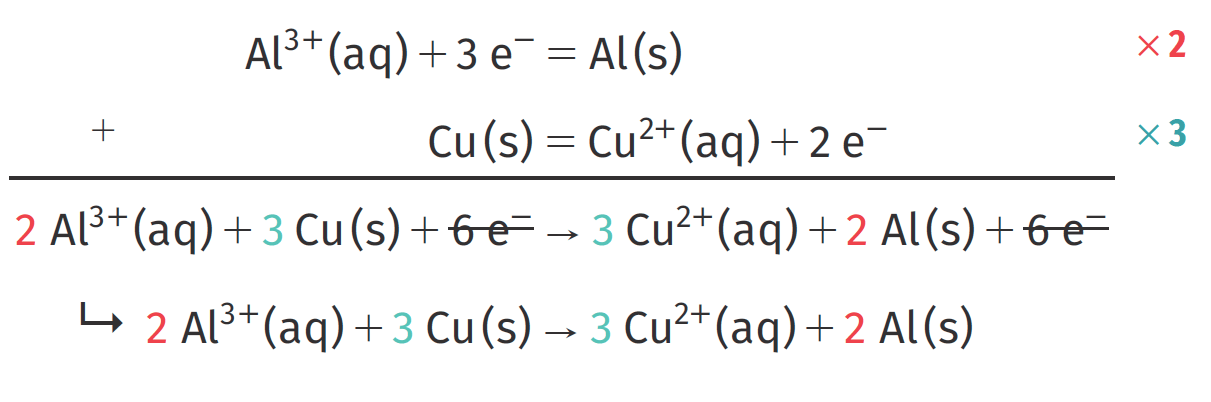oxydant reducteur cours
|
Chapitre IV
Un oxydant ( Réducteur ) est une espèce chimique qui fixe ( cède ) des électrons Lorsqu’un oxydant fixe des électrons il est réduit Inversement lorsqu’un réducteur cède des électrons il est oxydé Exemples: Oxydation: Zn ↔↔↔↔ Zn 2+ + 2e - : Perte d’électrons Réducteur Oxydant |
|
Chapitre 4 Oxydo-réduction
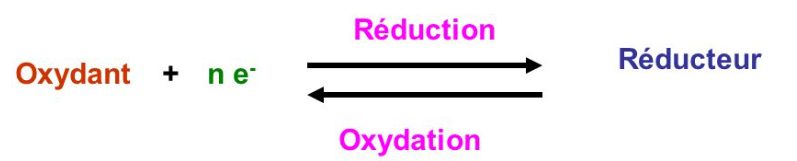
1 2 Couple oxydant / réducteur et demi-équation électronique À tout oxydant est associé un réducteur reliés par la demi-équation électronique: Ox + n e– ⇄ Red n orrespond au nom re d’életrons éhangés L’oxydant et le réduteur reliés par ette demi -équation électronique forment alors un couple oxydant / |
|
OXYDANT et REDUCTEUR réduction oxydation
« incandescents » entre deux éléments chimiques |
|
Oxydo-réduction – Fiche de cours
Vocabulaire Oxydant Un oxydant est une espèce chimique pouvant gagner des électrons Oxydation Une oxydation est une transformation chimique qui s’accompagne d’une perte d’électrons Réducteur Un réducteur est une espèce chimique pouvant perdre des électrons Réduction |
|
Chapitre 1 : Oxydoréduction
Oxydant = capteur d’électrons On appelle réducteur une entité (atome molécule ou ion) capable de céder au moins un électron au cours d’une réaction chimique : Réducteur = donneur d’électrons Un oxydant et un réducteur sont dits conjuguées et forment un couple redox (noté Oxydant/Réducteur) si on peut les relier par une |
|
Chapitre 6 : Les réactions d’oxydoréduction
Comme pour les acides et les bases un oxydant réagit forcément avec un réducteur Définition : Une réaction d’oxydoréduction consiste en un transfert d’électrons entre un oxydant d’un couple et un réducteur d’un autre couple Méthode d’écriture des demi-équations électroniques : a Oxydant + e- = réducteur b |
Comment calculer le couple oxydant-réducteur ?
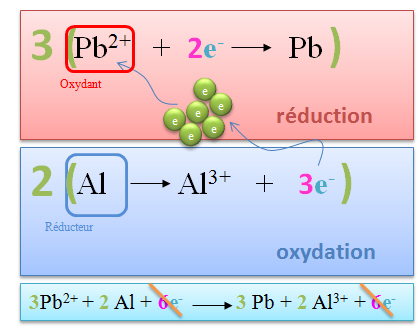
Au cours de cette oxydation, le réducteur se transforme en sa forme conjuguée qui est un oxydant : β Red = α Ox + ne−. Réduction : gain d’électron(s) par un oxydant. Au cours de cette réduction, l’oxydant se transforme en sa forme conjuguée qui est un réducteur : α Ox + ne− = β Red. On parle alors de couple oxydant/réducteur noté Ox/Red.
Quelle est la différence entre un oxydant et un réducteur ?
I-1- Définitions 1-a. Oxydant et Réducteur Un oxydant (Réducteur ) est une espèce chimique qui fixe (cède) des électrons. Lorsqu’un oxydant fixe des électrons il est réduit. Inversement lorsqu’un réducteur cède des électrons, il est oxydé.
Quelle est la différence entre oxydation et réduction ?
Oxydation : perte d’électron(s) par un réducteur. Au cours de cette oxydation, le réducteur se transforme en sa forme conjuguée qui est un oxydant : β Red = α Ox + ne−. Réduction : gain d’électron(s) par un oxydant. Au cours de cette réduction, l’oxydant se transforme en sa forme conjuguée qui est un réducteur : α Ox + ne− = β Red.
Comment calculer le pouvoir oxydant ?
Le pouvoir oxydant diminue si l’oxydant participe à une réaction parallèle. Considérons des ions Ag+ en milieu chlorure Cl−. On pourra donc retrouver l’argent au degré d’oxydation +I sous la forme d’ion Ag+ ou de précipité AgCl(s) Question 23 : Ecrire les deux demi-équations redox Ag+I/Ag0.
Echanges électroniques
ORA : Oxydoréduction en phase aqueuse
(ions solvatés, métaux immergés, gaz dissous et déga gements gazeux) bts-sciencesphysiques.org
2 Cu
aq : pour avoir un échange parfait d’électrons entre’oxydant l et le réducteur. bts-sciencesphysiques.org
Expérience 3 : entre le cuivre et l’ion nitrate
NO- : oxydant, il capte ? électrons, en subissant une réduction bts-sciencesphysiques.org
1B1 intérêt et utilisation du couple
Le couple est un « outil » pour équilibrer les équations bilan d’oxydoréduc tion. Equation bilan de la demie équation associée au couple : forme oxydée écrite à gauche - forme réduite écri te à droite. on ajoute le nombre d’électrons adéquat du côtée dla forme oxydée à gauche. bts-sciencesphysiques.org
2A1 la première pile en 1792
Alessandro professeur à Pavi Une « excitation » des nerfs de grenouille est provoquée par contact avec le cuivre et le zinc d’un empilement de pièces de monnaies en bronze (alliage à base de cuivre) et de zinc, séparés par des feutres imbibés de vinaigre. Cet empilement constitue un générateur (pile). bts-sciencesphysiques.org
2C Potentiel (standard) d’oxydoréduction du couple re dox
Il est donné par la lecture de la différence de pot entiel E+ - E-, sur le voltmètre. bts-sciencesphysiques.org
Réactions d’une grande variété et d’une grande importance
(les électrons sont échangés lors du choc entre les réactifs, ils ne se propagent pas dans l’air) combustion des carburants corrosion des métaux action des acides sur les métaux métallurgie (production* et affinage des métaux) électrochimie (piles, accumulateurs, électrolyses
4A Caractéristiques
Elles ne nécessitent aucun apport extérieur d’énergie . Elles sont plus ou moins rapides, voire parfois très lentes. bts-sciencesphysiques.org
4C3 oxydation par voie sèche
Les échanges électroniques ne sont pas évidents àisualiser v dans les équations d’oxydoréduction : combustions, oxydation par le dioxygène de l’air
(On ne parle plus de couples redox)
Retenons, alors, que le transfert de l’élément oxyg ène d’une espèce chimique vers une autre traduit une oxydation. bts-sciencesphysiques.org
4D1 principe
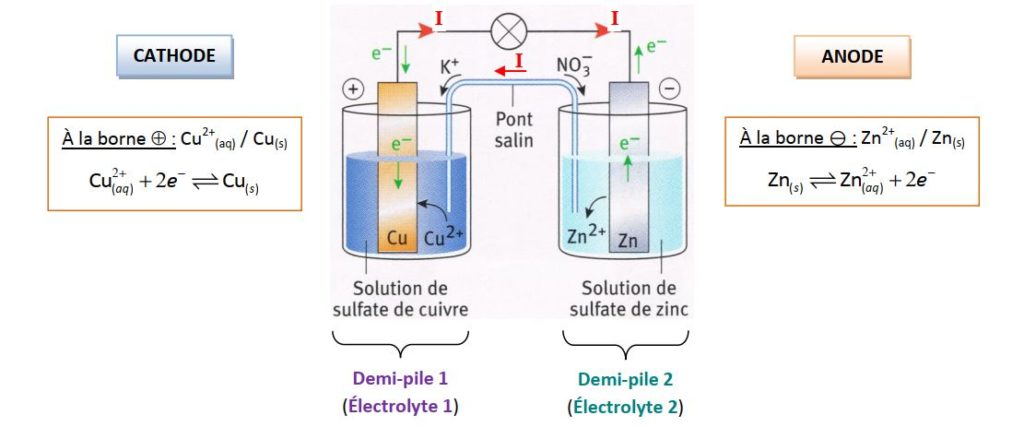
On réalise deux compartiments reliés par un pont salin qui assure la conductivité électrique entre les deux solutions et maintient la neutralité électriq ue des solutions. Les électrons circulent dans les métaux (électrodes : anode et athode, c et fils de connexion). Dans les solutions aqueuses, ce sont les ions qui permettent le passage du courant
h- remarque
Dans la pile, l’énergie libérée est cédée sous forme électrique à tout appareil lui étant connecté. Dans le cas de la lame de zinc plongeant dans la solution de sulfate de cuivre, l’énergie libérée par la réaction chimique échauffe la solution. bts-sciencesphysiques.org
5A Caractéristiques - Exemples
Elles nécessitent l’apport extérieur d’énergie . Une tension est imposée par un générateur . C’est le cas des électrolyseurs et des accumulateurs (batteries rechargeables, contrairement aux piles). bts-sciencesphysiques.org
5B1 principe
Alimenter deux électrodes plongeant dans un électrolyte liquide (aqueux ou non) par un générateur extérieur. Elle permet de réaliser une réaction d’oxydoréducti on inverse des réactions spontanées de l’énergie électrique au système chimique. (la réaction est « provoquée ») bts-sciencesphysiques.org

Oxydoréduction

OXYDANT et RÉDUCTEUR ✔️ Vocabulaire 1ère spé Physique Chimie

Oxydoréduction ✔️ Exercice complet 1ère Chimie
|
Chapitre 3 :Oxydoréduction
• Oxydation : réaction au cours de laquelle une espèce perd un ou plusieurs A) Couple oxydant/réducteur en phase aqueuse (cas simple). Exemple : Fe3+ ... |
|
Les réactions doxydo-réduction
➔ Le réducteur d'un couple (noté 1) peut participer à une réaction chimique avec l'oxydant d'un autre couple. (noté 2). ➔ Au cours de cette réaction le |
|
Chapitre 4 Oxydo-réduction
Dans une réaction d'oxydoréduction les réactifs sont un oxydant et un réducteur de deux couples oxydant. / Au cours de cette réaction |
|
Fiche de synthèse n°3.b Oxydants et réducteurs
Oxydant et réducteur : Un oxydant est une espèce chimique (atomes ions |
|
PHYSIQUE-CHIMIE THEME : OXYDOREDUCTION TITRE DE LA
oxydant-réducteurs est celle entre l'oxydant le plus ... Après le cours de chimie sur la classification quantitative des couples oxydant/réduceurs ton groupe. |
|
Leçon 11 : RÉDUCTION DES OXYDES
-Une réaction d'oxydoréduction est une réaction chimique au cours de laquelle l'oxydation et la - L'eau est réducteur/oxydant. Exercice 4. Le père de Kourouma ... |
|
Ch 6
Une oxydation est une réaction chimique au cours de laquelle une espèce chimique un réducteur perd Une réduction transforme un oxydant en son réducteur ... |
|
Chapitre 4 Oxydo-réduction
Dans une réaction d'oxydoréduction les réactifs sont un oxydant et un réducteur de deux couples oxydant. / Au cours de cette réaction |
|
CHAPITRE 3 : Réactions doxydo-réduction
Au cours de cette oxydation le réducteur se transforme en sa forme Définition : Couple oxydant/réducteur |
|
école numérique - thème : oxydoréduction titre de la leçon : couples
est un oxydant et ils forment le couple oxydant/réducteur ou couple redox Donne les couples oxydant / réducteur présents dans la solution au cours du dosage. |
|
Chapitre 3 :Oxydoréduction
Oxydation : réaction au cours de laquelle une espèce perd un ou plusieurs L'oxydant est un accepteur d'électrons le réducteur un donneur d'électrons. |
|
Les réactions doxydo-réduction
Chaque couple oxydant-réducteur représente un transfert d'électron(s) réalisable Au cours de cette réaction le réducteur 1 va libérer 1 ou plusieurs ... |
|
CHAPITRE 2 : LES REACTIONS DOXYDO-REDUCTION
2.2 Equation de demi-réaction d'un couple oxydant/réducteur Une réaction d'oxydo-réduction est une transformation chimique au cours de laquelle il y a ... |
|
1 NOTION DE COUPLE OXYDANT-REDUCTEUR
Notion de couple oxydant réducteur 1S1 AAMMAA LSIRL 2019.2020 Une réaction chimique au cours de laquelle une espèce chimique perd un ou des électrons ... |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
Titrage d'un acide faible par une base forte. CHAPITRE III : REACTIONS D'OXYDO-REDUCTION. 1. Généralités. 1.1. Oxydant réducteur |
|
Filière Sciences de la Matière Chimie Cours Chimie des Solutions
Oxydant réducteur |
|
Chapitre SA-PC&PSI. Seconde période Plan du cours
26 mars 2017 Oxydant et réducteur. 1.1. Défini on : le couple Ox/Red et la demi-équa on électronique. Un oxydant Ox est une espèce chimique qui peut ... |
|
Chapitre 4 Oxydo-réduction
Couple oxydant / réducteur et demi-équation électronique Au cours de cette réaction l'aldéhyde est oxydé en ion carboxylate R-COO–(aq) et les ions ... |
|
LES GLUCIDES
Ce sont donc des réducteurs qui vont subir une oxydation au cours de leur réaction. Oxydation de la fonction aldéhyde en fonction acide carboxylique. |
|
Chapitre CO-PC1. Seconde période Plan du cours Oxydoréduction
24 mai 2016 Une oxydation en chimie organique se traduit par une augmentation du nombre d'oxydation moyen des atomes de carbone. Une réduction en chimie ... |
Comment savoir qui est l'oxydant et le réducteur ?
. L'écriture s'effectue en juxtaposant les abréviations de l'oxydant et du réducteur séparés par un /.
C'est quoi un couple oxydant réducteur ?
. Fe(s) est le réducteur et Fe2+(aq) est l'oxydant du couple.
. La demi-équation d'oxydoréduction de ce couple est : Fe2+(aq) + 2 e– = Fe(s).
Comment faire une équation oxydant réducteur ?
. De nombreuses transformations chimiques impliquent le transfert d'un ou de plusieurs électrons d'un atome à un autre.
|
Chapitre 3 :Oxydoréduction
Oxydation : réaction au cours de laquelle une espèce perd un ou plusieurs électrons Couple redox/oxydant réducteur : Ox/Red Notation : Red e Ox réduction |
|
Chapitre 6 : Les réactions doxydoréduction - Physagreg
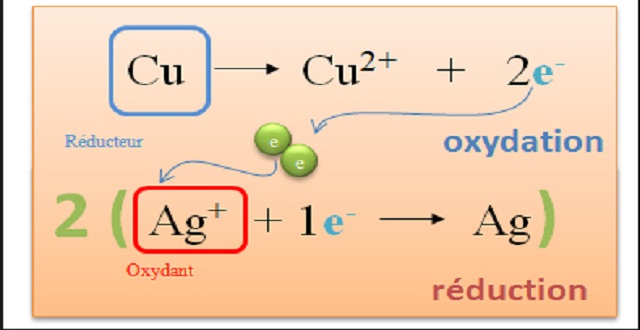
On dit que l'ion cuivre (II) est l'oxydant conjugué du cuivre ou que le cuivre est le réducteur conjugué de l'ion cuivre (II) Exercices n°7,12 et 13 p92 Page 3 |
|
Chapitre SA-PC&PSI Seconde période Plan du cours
26 mar 2017 · Oxydant et réducteur 1 1 Défini on : le couple Ox/Red et la demi-équa on électronique Un oxydant Ox est une espèce chimique qui peut |
|
Classification qualitative des couples oxydant réducteur - Fastef
classification quantitative des couples oxydants-réducteurs (réactions redox, propriétés D) L'oxydant est une substance oxydée au cours de la réaction |
|
E Q U I L I B R E D O X Y D O R E D U C T I O N
Beaucoup de ces réactions mettent en jeu le dioxygène (cf cours de chimie de Un réducteur cède un électron si un oxydant est présent pour pouvoir le capter |
|
Solutions aqueuses 2 : réactions doxydo-réduction - UNF3S
Ils forment un couple d'oxydo-réduction Ox/Red dit couple redox I 1) Définitions Ox + n e- = Red réduction oxydation Une oxydation est une perte d'électrons |
|
Chapitre V : REACTIONS DOXYDO-REDUCTION - WIMS
L'oxydant et le réducteur forment un couple conjugué, encore appelé couple Au cours de la réaction, l'étude de la variation du n o permet de déterminer si |
|
OXYDANT et REDUCTEUR réduction et oxydation - BTS - Sciences
il se fait oxyder Ces deux types de réaction font intervenir un même couple redox : Couple oxydant / réducteur Couple Cu 2+ aq / Cus 1A2 autres couples Zn |
|
REACTIONS DOXYDATION ET DE REDUCTION
celle-ci CHIMIE – 2e OS - 2014/2015 : Cours et exercices -24- Ecrivez l' équation de cette réaction, et identifiez l'oxydant et le réducteur 2 Le cuivre |
|
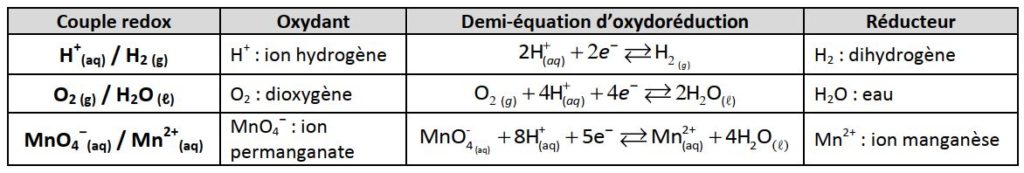
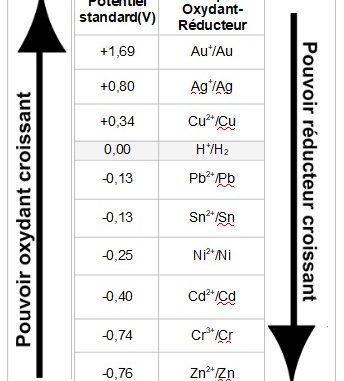
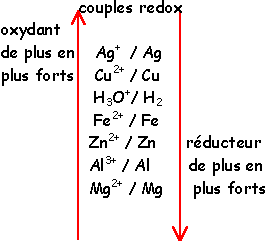
On obtient un couple oxydant / réducteur: H+ / H2 - Free
Des couples à connaitre : Page 2 ChiMie L'oxydo-réduction Le cours |