test de reconnaissance des ions chlorure
|
CH4 IDENTIFICATION D’IONS évaluation
qu’il y a des ions fer II dans la solution testée ; ce sera donc la solution de chlorure de fer II Il est inutile de réaliser le test au nitrate d’argent puisque dans les deux solutions il y a des ions chlorure ; dans les deux cas il se formera un précipité blanc qui ne nous permettra pas de différencier les deux solutions |
|
Chapitre 3 : Test de reconnaissance d’ions
1) Définitions Définitions : • Une transformation chimique est une transformation où des substances (molécules ou ions) disparaissent et d’autres apparaissent • Les substances qui disparaissent sont appelées réactifs réagissent entre eux • Les substances qui apparaissent sont appelées produits |
|
Chapitre 4 : L’identification des ions I TEST DE
On obtient un précipité blanc de chlorure d’argent qui noircit à la lumière : • La soude (hydroxyde de sodium : (Na + HO-)) est le réactif qui permet d’identifier les ions cuivre Cu 2+ les ions fer (II) Fe 2+ et les ions fer (III) Fe 3+ en solution On obtient un précipité caractéristique de l’ion testé |
|
Chapitre CHIMIE – Comment identifier les IONS présents dans
1) Une solution Ionique contient toujours des IONS POSITIFS et des IONS NEGATIFS 2) Par exemple dans une solution Ionique de Chlorure de Sodium (eau salée) il y a des Ions CHLORURES et des Ions SODIUM 3) La formule des Ions Chlorures est : Cl - 4) La |
|
FICHE RESSOURCE : Comment identifier des ions en solutions
ion chlorure-Cl ion argent Ag+ nitrate d'argent précipité BLANC de chlorure d'argent ion calcium Ca2+ Ion oxalate oxalate d'ammonium précipité BLANC d'oxalate de calcium ion cuivre II Cu2+ ion hydroxyde OH-hydroxyde de sodium précipité BLEU d'hydroxyde de cuivre ion fer -II Fe2+ ion hydroxyde OH hydroxyde de sodium précipité VERT d |
Qu'est-ce que le test de chlorure ?
Quand utiliser ce test ? Quand utiliser ce test ? Il permet de vérifier si une solution aqueuse contient des ions chlorure (de formule Cl – ). Les ions chlorure ne colorent pas les solutions aqueuses dans lesquelles ils sont dissous, leur présence ou leur absence ne peut donc être devinée à la couleur d’une solution.
Qu'est-ce que les ions chlorures ?
Les ions chlorures sont des halogénures qui, comme les ions bromure et les ions iodure, sont mis en évidence par du nitrate d’argent (NO 3– + Ag +) car ils précipitent en présence d’ ion argent Ag +.
Quelle est la formule des ions chlorures et sodium ?
Par exemple dans une solution Ionique de Chlorure de Sodium (eau salée) , il y a des Ions .CHLORURES... et des Ions ......SODIUM........ La formule des Ions Chlorures est : ......Cl -........................................... La formule des Ions Sodium est : ......Na +..................................................
Quel est le précipité caractéristique de l’ion testé ?
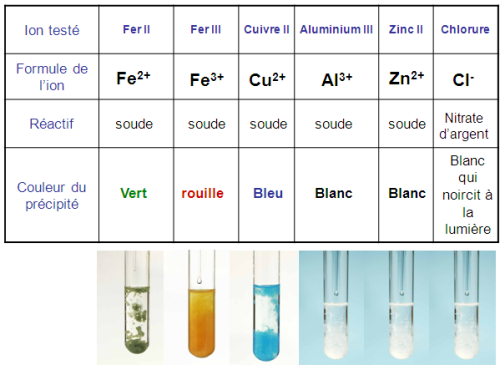
On obtient un précipité caractéristique de l’ion testé. (voir le tableau récapitulatif). • Tableau récapitulatif : Ion à identifier Réactif Couleur du précipité Chlorure : Cl-Solution de nitrate d’argent (contient l’ion argent : Ag+) Blanc (noircit à la lumière) Cuivre : Cu2+Bleu Fer (II) : Fe2+Vert Fer (III) : Fe3+
Les Ions Chlorure en Solution Aqueuse
Les ions chlorure ne colorent pas les solutions aqueusesdans lesquelles ils sont dissous, leur présence ou leur absence ne peut donc être devinée à la couleur d’une solution. webphysique.fr
Le Réactif
Les ions chlorures sont des halogénures qui, comme les ions bromure et les ions iodure, sont mis en évidence par du nitrate d’argent (NO3– + Ag+) car ils précipitent en présence d’ion argent Ag+. webphysique.fr
Le précipité
Le précipité est d’une couleur blanche laiteuse (on le qualifie en général de blanc cailleboté), il se forme par réaction entre les ions chlorure et les ions argent et il est constitué de chlorure d’argent (formule AgCl). Ce précipité a comme caractéristique de noircir lorsqu’il est laissé à l’air libre et exposé à la lumière, cette réaction chimiq
La Réaction de Précipitation
Si l’on ne fait pas figurer les ions spectateur alors la réaction de précipitationpeut s’écrire: ion chlorure + ionargent -> chlorure d’argent L’équation de réactioncorrespondante s’écrit alors: Cl–(aq) + Ag+(aq) -> AgCl(s) Cette équation indique que les proportions sont les suivantes: – La réaction de précipitationconsomme autant de chlorure que d
La Réalisation Pratique Du Test Des Ions Chlorure
Prélever un échantillon de solution à tester limité à quelques millilitreTransvaser cet échantillon dans un tube à essaiAjouter quelques gouttes (2 ou 3) de nitrate d’argent (utilisé comme réactif)Observer le résultat et vérifier s’il se forme un précipité webphysique.fr
Interprétation Des Résultats Du Test
S’il se forme un précipitéblanc alors le test est positif et confirme la détection d’ions chloure en solution.Si aucun précipité n’est visible alors le test est négatif: cela signifie qu’il n’y a pas d’ions chlorure en solution ou que leur concentration est si faible qu’ils ne peuvent être détectés (soit l

Tests didentification des ions

Test de reconnaissance des ions en solution.

Tests didentification des ions métalliques et chlorure
|
Chap 4 Tests de reconnaissance de quelques ions Ion cuivre Cu2+
I). Identification des ions chlorure Cl- : L'eau salée est une solution de chlorure de sodium. Elle contient des ions sodium Na+ et les ions chlorure. Cl- . On |
|
QUELQUES TESTS DIDENTIFICATION DES IONS
Si des ions chlorures sont présents alors il se forme un précipité blanc qui noircit à la lumière. Identification de l'ion sulfate : SO4. |
|
Chapitre CHIMIE – Comment identifier les IONS présents dans une
Comment utiliser des test de reconnaissance pour 2) Par exemple dans une solution Ionique de Chlorure de Sodium (eau salée) il y a des Ions . |
|
Reconnaître la présence dions en solution
la solution inconnue contient des ions fer (II) : c'est le test de reconnaissance des ions fer (II) Fe2+. Figure 4. Ion testé. Ion chlorure. Ion cuivre. |
|
Fiche Méthode N°6 : Tests de reconnaissance
Précipité bleu. Précipité blanc. Tests de présence des ions : chlorures métalliques et sulfate. Test de reconnaissance de l'eau. Tests de présence des gaz. |
|
Tests de reconnaissance de quelques ions _Doc. professeur
Identifier certains ions présents dans une solution aqueuse ;. • Respecter des consignes expérimentales. ACTIVITÉ 1 : Test de l'ion chlorure. 1. Dans une |
|
IDENTIFICATION DIONS
Les ions chlorure peuvent être mis en évidence grâce au nitrate d'argent ou plus précisément grâce aux ions argent. 1.2 Test par l'oxalate d'ammonium : 2. + C2. |
|
Tests didentification de quelques ions - AlloSchool
Test d'identification des ions chlorure. 1. Expérience : On verse quelques gouttes de nitrate d'argent de formule chimique. (. + ) dans des tubes à essai. |
|
Tests didentification de certaines espèces chimiques
Tests d'identification de certaines espèces chimiques. Nom espèce chimique for- mule appar ence. Protocole du test. Observation si le test est positif. |
|
CHP 5 : Réaction entre le fer et lacide chlorhydrique
1) Test des ions présents dans l'acide chlorhydrique Test de reconnaissance des ions : Nom : Ion chlorure. Formule :. |
|
Tests didentification de quelques ions - AlloSchool
Test d'identification des ions chlorure 1 Expérience : On verse quelques gouttes de nitrate d'argent de formule chimique ( + ) dans des tubes à essai |
|
Tests didentification de quelques ions - AlloSchool
Test d'identification de l'ion chlorure Cl- Interprétation En présence d'ions argent Ag+ les ions chlorure Cl- forment un précipité blanc qui noircit à |
|
QUELQUES TESTS DIDENTIFICATION DES IONS
Si des ions chlorures sont présents alors il se forme un précipité blanc qui noircit à la lumière Identification de l'ion sulfate : SO4 |
|
Chap 4 Tests de reconnaissance de quelques ions
I) Identification des ions chlorure Cl- : L'eau salée est une solution de chlorure de sodium Elle contient des ions sodium Na+ et les ions chlorure Cl- On |
|
Test Identification des ions - Physique Chimie
Télecharger la fiche au format PDF : Identification des ions (329 13 Ko) Test de reconnaissance des ions Chlorure Cl-: Réactif utilisé le Nitrate |
|
Tests de reconnaissance de quelques ions _Doc professeur - Pierron
Identifier certains ions présents dans une solution aqueuse ; • Respecter des consignes expérimentales ACTIVITÉ 1 : Test de l'ion chlorure 1 Dans une |
|
Tests de reconnaissance des ions I Les solutions ioniques
Ex : le chlorure d'aluminium Ions : Cl - Al3+ On crée la formule de la manière suivante : (Formule du cation + formule de l'anion) |
|
Activité 1 : Tests didentification de quelques ions
Observation Il se forme un précipité III/ Identification de l'ion chlorure Pour identifier les ions chlorures Cl- on utilise le nitrate d'argent |
|
I- Tests didentification des ions chlorure 1
Tests d'identification des ions chlorure L'ion chlorure est un anion qui existe dans plusieurs solutions aqueuses comme : solution de chlorure d'hydrogène |
|
4-1 Test ions Version 1 - Sites ENSFEA
Identification des ions But : j'identifie les ions chlorure cuivrique ferreux (fer II) et ferrique (fer III) dans des produits de la vie courante |
Quel est le test d'identification de l'ion chlorure ?
==> Test de reconnaissance des ions Chlorure Cl-: Réactif utilisé le Nitrate d'argent. En présence de nitrate d'argent, les ions Cl- forment un précipité blanc qui noircit à la lumière. Si la solution à un pH inférieur à 7, c'est-à-dire un pH acide, nous sommes en présence d'ions H+.Comment mettre en évidence les ions de chlorure ?
On ajoute quelques gouttes d'une solution de nitrate d'argent. En présence d'une solution de nitrate d'argent, l'ion chlorure Cl- forme un solide appelé précipité. Ce précipité blanc noircit à la lumière. Ce sont les ions argent et les ions chlorure qui réagissent ensemble pour former le précipité.- Test de reconnaissance des ions Chlorure
Elle mène alors à la formation d'un précipité de Chlorure d'Argent (AgCl). Après ajout du Nitrate d'Argent dans la solution de Chlorure de Sodium, un précipité blanc de Chlorure d'Argent se forme, ce qui confirme la présence d'ions Chlorure dans la solution initiale.
| Chapitre 3 : Test de reconnaissance d’ions - ac-versaillesfr |
| II Principe de reconnaissance des ions - AlloSchool |
| Tests d'identification de Collège quelques ions - AlloSchool |
| II Principe de reconnaissance des ions - AlloSchool |
| Tests de reconnaissance de quelques ions - AlloSchool |
| Searches related to test de reconnaissance des ions chlorure filetype:pdf |
Qu'est-ce que le test de reconnaissance des ions?
- Principe de reconnaissance des ions : Un test de reconnaissance a pour objectif de prouver la présence des ions dans une solution ionique. ?Pour mettre en évidence la présence d’ions dans des solutions, on réalise des réactions de précipitation.
. Un précipité est un solide résultant de la réaction chimique entre un anion et un cation.
|
Chap 4 Tests de reconnaissance de quelques ions
I) Identification des ions chlorure Cl- : L'eau salée est une solution de chlorure de sodium Elle contient des ions sodium Na+ et les ions chlorure Cl- On ajoute |
|
QUELQUES TESTS DIDENTIFICATION DES IONS - Collège Les
Si des ions chlorures sont présents, alors il se forme un précipité blanc qui noircit à la lumière Identification de l'ion sulfate : SO4 2- Manipulation : On verse |
|
Tests de reconnaissance de quelques ions _Doc - Pierron
Mots clefs o Ion o Ion chlorure o Ion cuivre (II) o Ion fer (II) o Ion fer (III) o Nitrate d' argent o Précipité o Solution aqueuse o Soude o Test d'identification Prévoir |
|
12 Identification de lion chlorure Cl 13 Identification de lion sulfate
En présence des ions chlorure, il se forme un précipité blanc qui peu à peu Tests test à la soude test au nitrate d'argent test au chlorure de baryum Couleur |
|
Tests de reconnaissance des ions
ème : A – Test de reconnaissance de l'eau par le sulfate de cuivre anhydre ⇨ Niveau 5 b) Tests de reconnaissance des ions chlorure et des ions métalliques |
|
Reconnaître la présence dions en solution
le test de reconnaissance des ions fer (II) Fe2+ Figure 4 Ion testé Ion chlorure Ion cuivre Ion fer (II) Ion fer (III) Formule chimique Cl - Cu2+ Fe2+ Fe3+ Test |
|
I- Tests didentification des ions chlorure 1- Expérience et
I- Tests d'identification des ions chlorure L'ion chlorure est un anion qui existe dans plusieurs solutions aqueuses comme : solution de chlorure d'hydrogène |
|
TP CHIMIE n°2 : Tests de reconnaissance de quelques ions - MMorin
Objectifs du TP : Mettre en oeuvre les tests caractéristiques qui permettent de déceler la présence des ions suivants : l'ion chlorure (Cl-), l'ion cuivre (Cu2+), l' ion |
|
EXERCICE DE REMÉDIATION - CHIMIE - 3ÈME 3C3D1I41CH9
Le test au nitrate d'argent permet d'identifier l'ion chlorure : il apparaît un précipité blanc Le test à la soude permet d'identifier les ions cuivre II, fer II et fer III : il |