Pile Chimique
|
Les piles dispositifs mettant en jeu des transformations spontanées
1) Définition : Une pile électrochimique est un générateur qui transforme de l'énergie chimique fournie par une réaction d'oxydoréduction spontanée en énergie |
|
Les piles
Lorsque la pile est usée le système chimique est à l'équilibre : Qréq = K et I = 0 Exemple : la pile Daniell Les porteurs de charge assurent le passage du |
|
Oxydo-réduction et Piles électrochimiques SMPC2 fsr 2015
3) Ecrire l'équation de la réaction chimique globale de fonctionnement de la pile et calculer sa constante d'équilibre 4) Faire un schéma de la pile sur lequel |
|
Thème : Piles et électrolyses Fiche 4
Pile : ensemble de deux demi piles reliées par un pont électrolytique l'effet d'une transformation chimique à l'électrode qui constitue cette borne (pile) |
|
Chimie
Chimie – Partie C – Chapitre 8 : Les piles – Page 1 sur 3 Nous avons vu au Une pile est constituée de deux demi-piles reliées par un pont salin Chaque |
|
10pilespdf
Une pile est un système chimique hors équilibre Lorsqu'elle fonctionne elle évolue spontanément vers l'état d'équilibre et la valeur de son quotient tend vers |
|
Tp : comprendre et modeliser le fonctionnement dune pile
Les piles sont omniprésentes Elles sont le siège d'une transformation chimique spontanée Nous allons ici tenter de modéliser le fonctionnement d'une pile (ici |
|
X9: Les piles électrochimiques
Une pile électrochimique est un générateur qui transforme une partie de l'énergie chimique venant d'une réaction d'oxydoréduction spontanée en énergie |
|
On appelle pile électrochimique tout dispositif qui permet dobtenir
a- Préciser le sens de courant électrique et celui de mouvement des électrons dans le circuit extérieur b- Déduire l'équation de la réaction chimique spontanée |
I.
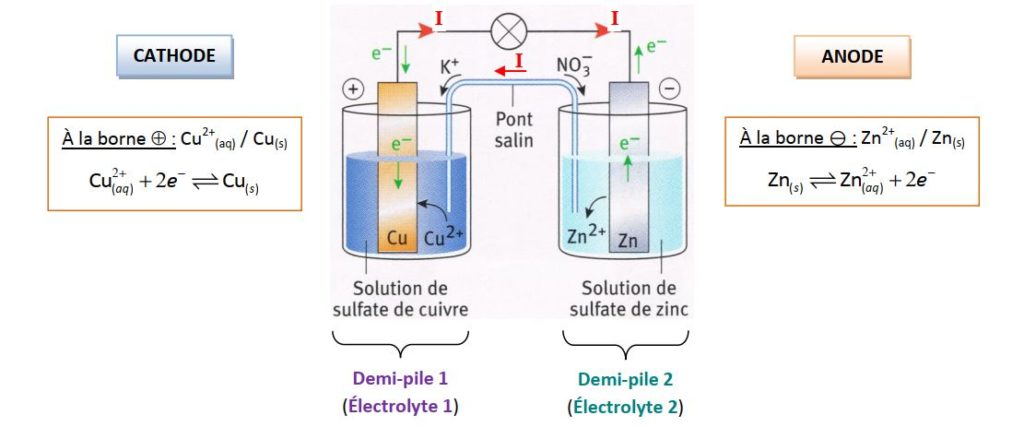
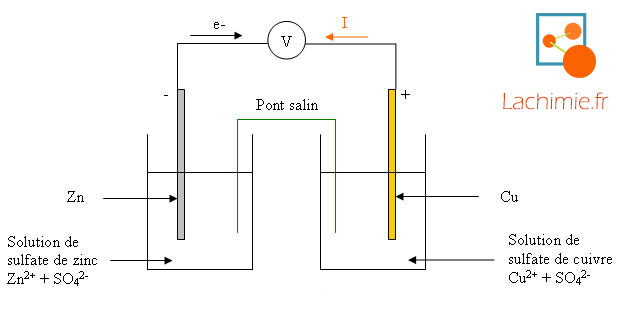
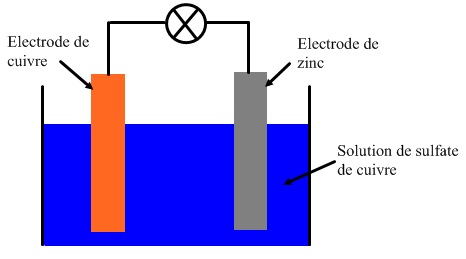
La première demi-pile est constituée d'une lame de Cuivre plongée dans une solution de sulfate de Cuivre composée d'ions sulfate SO42- et des ions Cuivre Cu2+.
La deuxième demi-pile est constituée d'une lame de Zinc qui trempe dans une solution contenant du sulfate de Zinc (SO42- et Zn2+).
Quels sont les principaux composants de la pile Électro-chimique ?
L'électrolyte de la pile est une solution congelée de chlorure d'ammonium N H 4 C l , un sel, d'où le nom de pile saline.
Du carbone en poudre est dispersé dans l'électrolyte pour le rendre plus conducteur.
L'oxydant M n O 2 , du dioxyde de manganèse en poudre, est aussi dispersé dans la solution gelée.
Comment fonctionne une pile chimie ?
Comment ça marche ? La pile est composée de deux électrodes – un pôle positif (ou cathode) et un pôle négatif (ou anode) – plongées dans une solution faisant office de conducteur.
Lorsque ces électrodes sont reliées par un fil conducteur à un consommateur électrique, une ampoule par exemple, cela ferme le circuit.
C'est quoi une pile électrochimique ?
Une pile électrochimique est le siège d'une réaction d'oxydoréduction spontanée (c'est à dire naturelle) entre deux couples redox.
Elle permet la conversion de l'énergie chimique en une autre forme d'énergie.
|
Stabilisation chimique des électrolytes polymères pour pile à
5 sept. 2012 électrolytes polymères utilisés en pile à combustible. ... vecteurs de dégradation chimique induits en pile et de ce fait |
|
Chapitre 2 - Évolution spontanée dun système chimique
Le principe sera présenté en suivant l'exemple de la pile Daniell schématisée sur la figure 2.1. Une pile est constituée de deux demi-piles |
|
Fiche pédagogique sur le mini-jeu de la pile à combustible
Ce puzzle permet de mettre en œuvre le principe de fonctionnement d'une pile à combustible. (programme de physique?chimie niveau lycée) |
|
Evolution spontanée dun système chimique` TP : COMPRENDRE
Une pile Daniell est constituée de deux demi-piles. La demi-pile de gauche est constituée d'un volume V1 = 50 mL d'une solution de sulfate de zinc (II) de |
|
ATELIER PÉDAGOGIQUE 1 CONSTRUCTION OBSERVATION ET
Se sensibiliser aux composants chimiques et métalliques de la pile. 1. OBJECTIF. Matériel et installation : il faut un acide (du citron) deux métaux (zinc |
|
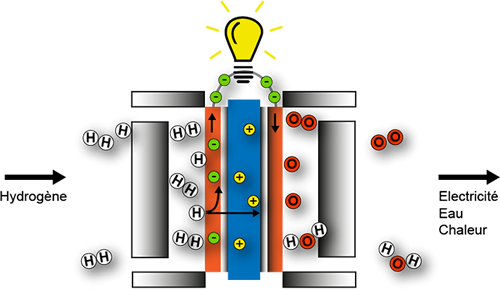
La piLe à hydrogène
Ces liaisons possèdent de l'énergie appelée énergie chimique. b. schéma de la pile à hydrogène (pile à combustible). Anode oxydation du dihydrogène H2. |
|
Lénergie chimique et ses conversions
peut être convertie lors de transformations chimiques en énergie thermique Lorsque la pile fonctionne il se produit une transformation chimique. |
|
La piLe à hydrogène
Ces liaisons possèdent de l'énergie appelée énergie chimique. b. schéma de la pile à hydrogène (pile à combustible). Anode oxydation du dihydrogène H2. |
|
Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
système chimique au travers d'électrodes qui trempent dans le système. CHIMIE. Série S. Nº : 37004. Fiche Cours. ? Une pile est le siège d'une réaction ... |
|
LES PILES A COMBUSTIBLE
Les piles à combustible convertissent directement en électricité l'énergie chimique de combustibles divers (sans combustion) avec de multiples avantages |
Quels sont les différents types de piles ?
Qu'est-ce qu'une pile en chimie ?
. Définition. Une pile électrochimique est un générateur qui transforme une partie de l'énergie chimique venant d'une réaction d'oxydoréduction spontanée en énergie électrique.
C'est quoi une pile électrochimique ?
. Elle permet la conversion de l'énergie chimique en une autre forme d'énergie.
Quel est la composition d'une pile ?
|
Chap4 Pile électrochimique et énergie chimique
Pile sulfate de cuivre-Zinc AE : Pile cuivre-Zinc Expérience n°1: Une transformation chimique peut elle produire de l'énergie |
|
10-Les piles électrochimiques - Physagreg
Une pile électrochimique est un générateur qui transforme de l'énergie chimique fournie par une réaction d'oxydoréduction spontanée en énergie électrique |
|
Les piles électrochimiques Cours I-/ Définition dune - TuniSchool
de la pile Daniell 1-/ Schéma de la pile 2-/ Symbole de la pile Zn Zn 2+ (1 mol L -1 ) Cu 2+ (1 mol L -1 ) Cu 3-/ Équation chimique associée à la pile |
|
Piles et électrolyses - Studyrama
système chimique au travers d'électrodes qui trempent dans le système CHIMIE Série S Nº : 37004 Fiche Cours ☞ Une pile est le siège d'une réaction |
|
Les piles électrochimiques
dans le circuit extérieur de la pile, du potentiel le plus bas mique en énergie électrique ; l'énergie chimique La pile Daniell (ou pile cuivre-zinc) est consti- |
|
ECE : Les piles électrochimiques - Académie dOrléans-Tours
John Daniell, professeur de chimie au King's College de Londres invente en 1836 la pile qui porte aujourd'hui son nom Il s'agit d'un élément impolarisable |
|
Les piles - Chapitre 1
Chimie – Partie C – Chapitre 8 : Les piles – Page 1 sur 3 Nous avons vu au chapitre 7, qu'un système chimique peut évoluer spontanément vers un état |
|
Oxydo-réduction et pile : commentaires scientifiques décrivant les
Le potentiel de la pile est lié aux composants des deux cellules de demi-réaction et dépend des L'équilibre chimique entre les protons et les molécules |
|
STOCKAGE DE LÉNERGIE ÉLECTRIQUE : LES PILES - Mediachimie
Étude expérimentale de la pile Daniell 1re STI2D Thème • Matière et matériaux Partie • Transferts d'électrons lors d'une transformation chimique Capacités |
|
Les piles et loxydo-réduction :
2 - Indiquer le signe des pôles de la pile formée ainsi que le sens de passage du courant Le couple du fer est oxydant vis à vis de celui du cuivre ( Volt 345 0 E |