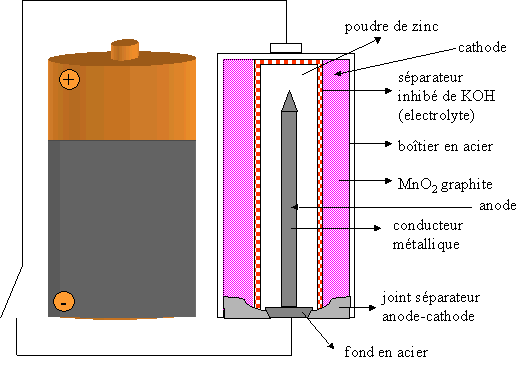
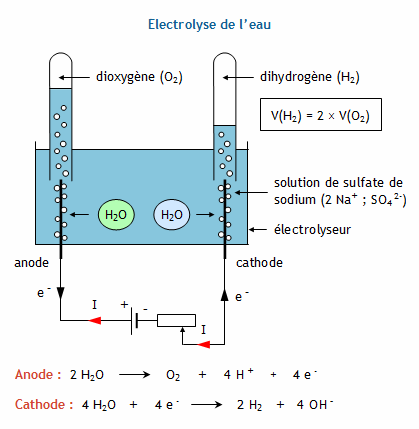
pile cuivre zinc
|
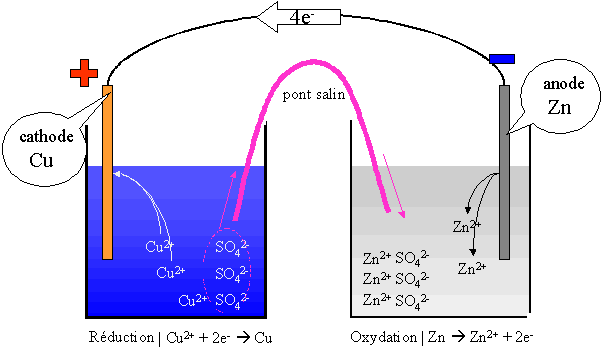
B) Fonctionnement de la pile Daniell : c) Réaction aux électrodes
La plaque de cuivre qui représente le pôle positif de la pile s'appelle: la cathode La plaque de zinc qui représente le pôle négatif de la pile s'appelle l' |
|
Les piles dispositifs mettant en jeu des transformations spontanées
Observations : ➢ Expérience TP : la solution dans laquelle on a ajouté la poudre de cuivre et la poudre de zinc s'est décolorée ➢ Expérience cours : un dépôt |
|
Pile Cuivre-Zinc
L'objectif de la manipulation est de réaliser une pile cuivre-zinc et de déterminer la durée d'autonomie de cette pile lorsqu'elle alimente une LED La |
|
10pilespdf
La pile Daniell ▫ La pile Daniell (ou pile cuivre-zinc) est constituée de deux demi- piles : l'une formée d'une plaque de cuivre plongée dans une solu- |
|
Piles électrochimiques
- Dans un bécher mélanger environ 20 mL d'une solution de sulfate de cuivre 0 1 mol/L et 20 mL de sulfate de zinc 0 1 mol/L - Plonger dans le bécher une lame |
|
ETUDE DUNE PILE CUIVRE-ZINC
A partir de la mesure d'une tension ou de l'intensité d'un courant analyser le fonctionnement d'une pile électrochimique I Constitution Vous disposez d'une |
|
La pile électrique chimique
L'électrode de zinc se couvre d'une couche de cuivre ! En fait la réaction qui s'est produite à cette électrode est directement Cu++ + Zn → Cu + Zn++ Les |
|
Tp : comprendre et modeliser le fonctionnement dune pile
Faire un schéma avec une lame de zinc plongeant dans une solution de sulfate de cuivre Transfert direct d'électrons -Une pile est le siège d'une réaction |
|
Fiche de synthèse n°4 : piles
Une pile correspond à l'association de deux compartiments distincts deux demi-piles reliées par un pont salin ou une membrane poreuse imbibée d'une solution |
Comment fonctionne la pile de Daniel ?
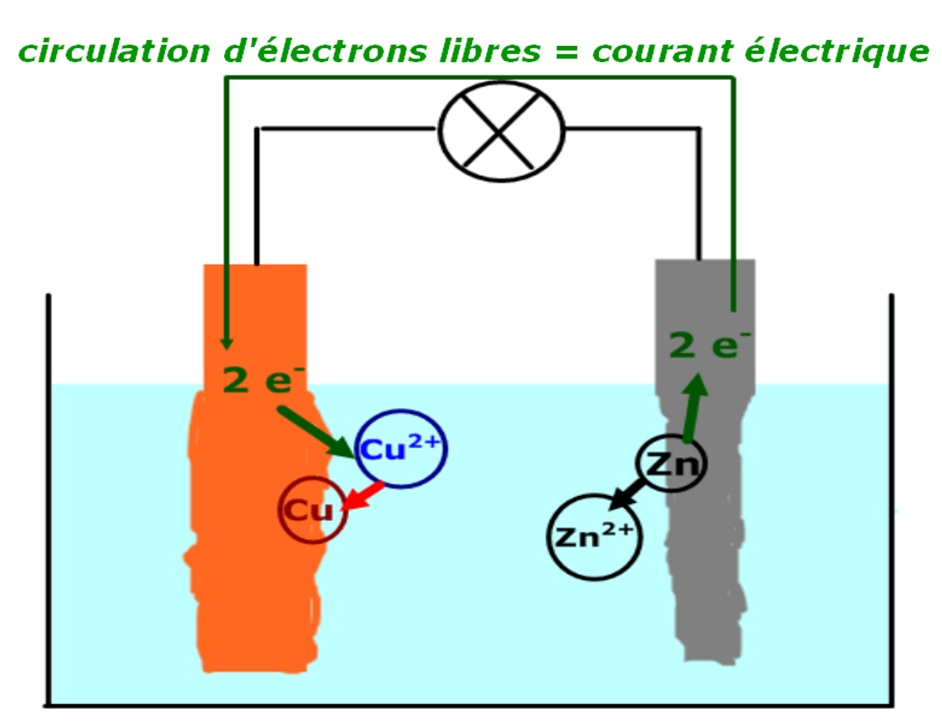
Lorsque les électrons se déplacent d'une cathode vers une anode, les électrons « libres » de la cathode tombent sur les emplacements vides d'électrons (les « étagères ») dans l'anode.
Les électrons vont alors occuper volontiers ces vides dans l'anode, ce qui permet au courant de se déplacer plus loin.Quel est le rôle de chaque électrode ?
l'une est le siège de la réaction de réduction, c'est la cathode (pôle + de la pile) ; l'autre est le siège de la réaction d'oxydation, c'est l'anode (pôle – de la pile).
Quel est le rôle du pont ionique ?
Un pont salin permet le transport des charges d'une demi-pile à l'autre, grâce à la migration des ions.
1799 : La pile Volta - 1836 : La pile Daniel
En 1799, le physicien italien Alessandro Volta a créé la première pile en empilant successivement des couples de disques zinc-cuivre avec des morceaux de tissu imbibés d'eau salée.
|
Oxydo-réduction et pile : commentaires scientifiques décrivant les
Les ions cuivre (II) en solution arrachent ainsi des électrons au zinc métallique et transforment ce dernier en ions zinc aqueux. Dans ce système le zinc |
|
TP 9 chimie : Terminale REALISATION ET ETUDE DE PILES Étude
Montrer qu'une pile délivre un courant en circuit fermé. Utiliser le critère d'évolution Qu'ont échangé le cuivre et le zinc dans cette expérience ? |
|
La pile de daniell – calcul de la force electromotrice
Relions les 2 bornes de la pile au moyen d'un voltmètre. l'électrode de cuivre. ... Le potentiel standard de réduction de l'électrode de zinc. |
|
3B SCIENTIFIC 3B SCIENTIFIC® PHYSICS Pile Daniell 1002898
La pile Daniell appelée d'après John Frederic Daniell |
|
ETUDE DUNE PILE CUIVRE-ZINC
L-1 d'une solution de sulfate de zinc à 10-2 mol.L-1 et d'un pont salin contenant une solution gélifiée de chlorure de potassium pour réaliser une pile cuivre- |
|
B) Fonctionnement de la pile Daniell : c) Réaction aux électrodes: d
Un ampèremètre branché aux bornes de la pile indique le passage du courant électrique de la plaque de cuivre vers la plaque de zinc. |
|
TP N°10-PROF : LES PILES ELECTROCHIMIQUES
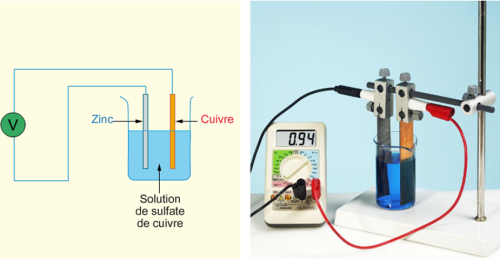
Un multimètre permet de mesurer la tension à vide aux bornes de la pile. La simulation faite avec la pile cuivre-zinc ne conduit pas à des résultats |
|
Observations : Identification des réactifs : Identification des produits
On admet que des ions Zn2+ (incolores) sont apparus dans le bécher. CH.5. COMMENT FONCTIONNE UNE PILE ? CORRECTION. Lame de zinc. (Zn). Sulfate de cuivre :. |
|
Niveau 3
APPROCHE DE L'ENERGIE CHIMIQUE : Comment une pile électrochimique peut-elle être une o Le cuivre est un métal rouge orangé le zinc est un métal gris. |
|
T.4.1 T.P. N°1 Comment fabriquer une pile ?
II) Matériel : Deux béchers étiquetés « Cu ». Un bécher étiqueté « Zn ». Une lame de zinc deux lames de cuivre. Une solution de sulfate de zinc (1 mol/L). |
Comment fonctionne la pile de Daniel ?
. En même temps, des particules de zinc avec quelques électrons manquants (ions zinc Zn2+) entrent dans la solution.
Quelle est la borne positive de la pile ?
. La réaction capte des électrons.
. L'électrode de cuivre attire les électrons, qui ne peuvent venir que du circuit électrique. L'électrode de cuivre est la borne positive de la pile.
Quels sont les composants d'une pile ?
Quelle est la polarité de la pile ?
. Le pôle positif est celui qui capte les électrons.
|
Chap4 Pile électrochimique et énergie chimique
Réaliser, décrire et schématiser la réaction entre une solution aqueuse de sulfate de cuivre et de la poudre de zinc en réalisant une pile I Comment fabriquer |
|
TP : LA PILE CUIVRE ZINC - fredpeurierecom
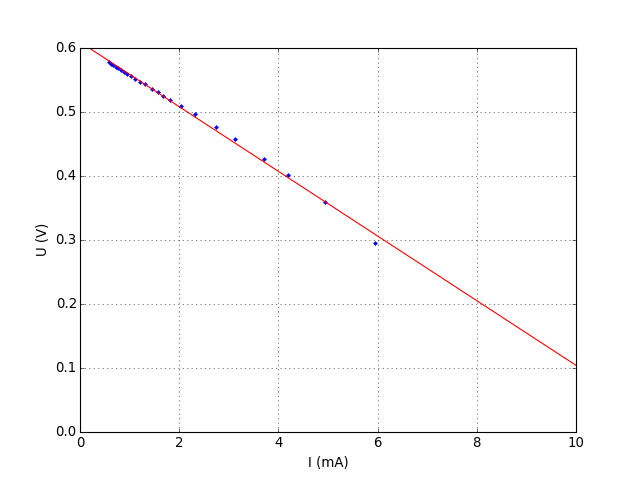
TP : LA PILE CUIVRE ZINC CORRECTION 1 En branchant le multimètre de façon à mesurer une tension (mode voltmètre), il est possible de déterminer |
|
Les piles électrochimiques
faut une centrale électrique (pile, batterie) cons- tituée de 2 dans le circuit extérieur de la pile, du potentiel La pile Daniell (ou pile cuivre-zinc) est consti- |
|
Quelques expériences avec les piles - LFRD
Un peu d'histoire des sciences sur l'invention de la pile : Présentation de la pile Volta devant Napoléon couples de cuivre et de zinc, occupant 54 mètres |
|
TP N°10-PROF : LES PILES ELECTROCHIMIQUES - Physagreg
Montrer qu'une pile délivre un courant en circuit fermé La simulation faite avec la pile cuivre-zinc ne conduit pas à des résultats satisfaisants, il est donc |
|
10-Les piles électrochimiques - Physagreg
Interpréter le fonctionnement d'une pile en disposant d'une information parmi d' électrons direct entre les atomes de zinc de la lame et les ions cuivre II de la |
|
ECE : Les piles électrochimiques - Académie dOrléans-Tours
1 lame métallique de cuivre bien décapée - 1 lame métallique de zinc bien décapée - Pont salin (papier + solution de KCl ou tube rempli de gel de KCl) |
|
STOCKAGE DE LÉNERGIE ÉLECTRIQUE : LES PILES - Mediachimie
Activité expérimentale Fonctionnement de la pile électrique cuivre • zinc Pont salin, pinces crocodiles, conducteur ohmique de 10 Ω, fils, multimètre |
|
Niveau 3 - Pierron
sulfate de cuivre et de la poudre de zinc : - par contact direct - en réalisant une pile Réaction entre les ions cuivre (II) et la poudre de zinc Pistes d'activités |
|
Piles et électrolyses - Studyrama
Exemple : la pile cuivre zinc utilise les deux couples oxydants réducteurs Cu2+ ( aq)/Cu(s) et Zn2+ (aq)/Zn(s) ; dans cette pile, l'anode est le zinc et la cathode |