pile daniell
|
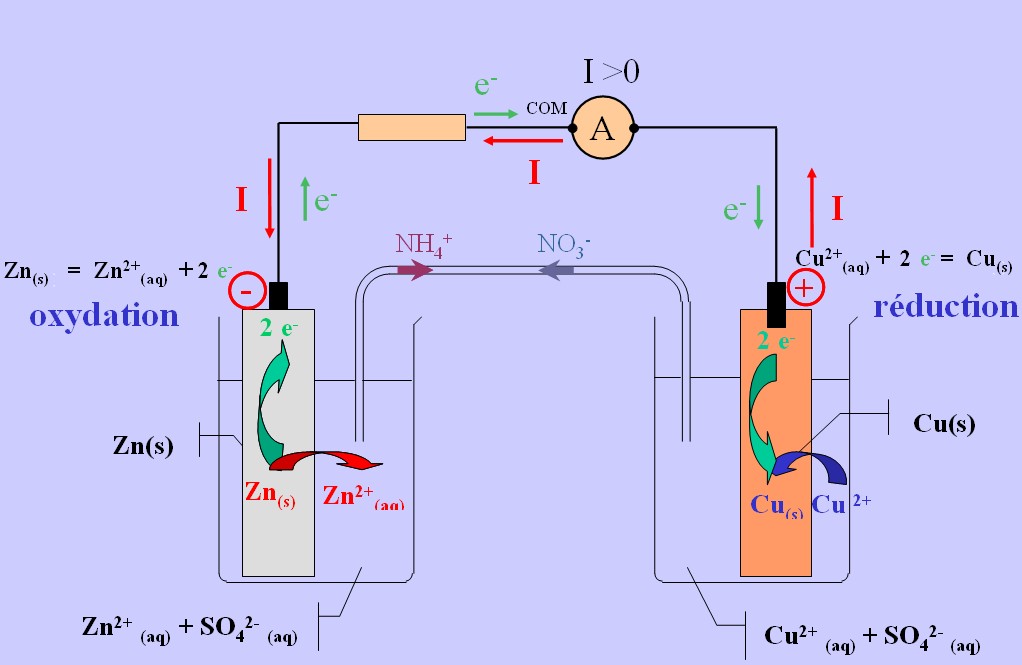
B) Fonctionnement de la pile Daniell : c) Réaction aux électrodes
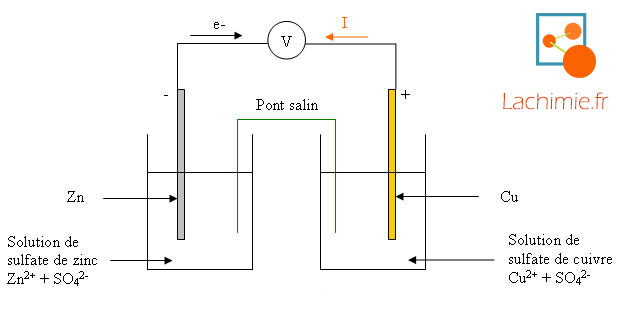
b) Fonctionnement de la pile Daniell : Un ampèremètre branché aux bornes de la pile indique le passage du courant électrique de la plaque de cuivre vers la |
|
Les piles dispositifs mettant en jeu des transformations spontanées
Une pile électrochimique est un générateur qui transforme de l'énergie chimique fournie par une réaction d'oxydoréduction spontanée en énergie électrique Page |
|
Chimie
La pile Daniell a débité une intensité constante égale à 100 mA Quelle a été la durée de fonctionnement de la pile ? Nous cherchons la durée ∆t de |
|
Chapitre-7-ETUDE-DE-LA-PILE-DANIELLpdf
La pile Daniell est un système chimique constituée de deux compartiments contenant l'un le métal cuivre en contact avec une solution aqueuse d'un sel de cuivre |
|
Tp : comprendre et modeliser le fonctionnement dune pile
Nous allons ici tenter de modéliser le fonctionnement d'une pile (ici la pile Daniell) en déterminer les réactions chimiques qui ont lieu au niveau des |
Comment fonctionne la pile de Daniell ?
Lorsque les électrons se déplacent d'une cathode vers une anode, les électrons « libres » de la cathode tombent sur les emplacements vides d'électrons (les « étagères ») dans l'anode.
Les électrons vont alors occuper volontiers ces vides dans l'anode, ce qui permet au courant de se déplacer plus loin.Qui a inventé la pile Daniell ?
1799 : La pile Volta - 1836 : La pile Daniel
En 1799, le physicien italien Alessandro Volta a créé la première pile en empilant successivement des couples de disques zinc-cuivre avec des morceaux de tissu imbibés d'eau salée.Quel est le rôle du pont salin dans la pile Daniell ?
→Le pont salin joue deux rôles : -fermer le circuit afin assurer le passage du courant électrique dans la pile. -assurer la neutralité électrique des solutions.
Comment ça marche ? La pile est composée de deux électrodes – un pôle positif (ou cathode) et un pôle négatif (ou anode) – plongées dans une solution faisant office de conducteur.
Lorsque ces électrodes sont reliées par un fil conducteur à un consommateur électrique, une ampoule par exemple, cela ferme le circuit.
|
3B SCIENTIFIC 3B SCIENTIFIC® PHYSICS Pile Daniell 1002898
La pile Daniell appelée d'après John Frederic Daniell |
|
B) Fonctionnement de la pile Daniell : c) Réaction aux électrodes: d
La pile Daniell est constituée de deux compartiments liés par un pont salin. ? Le premier compartiment se compose d'une plaque de cuivre plongée dans une |
|
Energy on demand: A brief history of the development of the battery
piles to modern lithium ion cells batteries have been powering scientific and techno- Battery |
|
1836 : La pile Daniel En 1799 le physicien italien Alessandro Volta
Pile Volta. La prochaine évolution dans la technologie des piles date de 1836 lorsque le chimiste anglais John Frederick Daniell a inventé la pile Daniell. |
|
Evolution spontanée dun système chimique` TP : COMPRENDRE
Une pile Daniell est constituée de deux demi-piles. La demi-pile de gauche est constituée d'un volume V1 = 50 mL d'une solution de sulfate de zinc (II) de |
|
I- La pile Daniell Cours chimie : Piles électrochimiques
I- La pile Daniell. 1- Transfert indirect d'électrons d'un réducteur à un un oxydant. Dispositif expérimental. Lorsqu'on ferme l'interrupteur k. |
|
Chapitre-7-ETUDE-DE-LA-PILE-DANIELL.pdf
3/ Généraliser le principe de la pile Daniell à d'autres piles du même type. 4/ Prévoir le sens d'évolution spontanée d'un système siège d'une réaction redox d' |
|
La pile de daniell – calcul de la force electromotrice
LA PILE DE DANIELL –. CALCUL DE LA FORCE ELECTROMOTRICE. Relions les 2 bornes de la pile au moyen d'un voltmètre. On y lit une différence de potentiel (ddp) |
|
LA PILE DE DANIELL Mod. CB-IN-81/EV
à la pile Daniell. La pile est formée de deux éléments galvaniques. (demi-cellules) chacun formé d'une lame métallique plongée. |
|
ECE : Les piles électrochimiques
La pile Daniell initiale est constituée d'un cylindre de cuivre contenant une solution de sulfate de cuivre où baigne une corne de bœuf. Celle-ci est remplie d' |
Quel rôle joue le pont salin ?
Quelle est la fonction de la pile ?
. Contrairement aux batteries (ou accumulateurs), la pile est à usage unique et ne peut être rechargée.
Comment savoir qui est l'anode et la cathode ?
. Les ions chargés négativement appelés anions sont attirés vers l'électrode positive, que nous appelons l'anode.
. Donc, sur cette figure, l'anode est à gauche et la cathode est à droite.
Comment identifier les pôles d'une pile ?
. Avec un branchement correct, la borne « com » (négative) du voltmètre est reliée à l'électrode de zinc.
. La borne positive est l'électrode de cuivre.
|
La pile Daniell
11 mar 2015 · La pile Daniell Cahier de laboratoire : éléments de correction Contenu du cahier Colonne réservée à l'évaluateur Première partie : montrer |
|
Les piles électrochimiques Cours I-/ Définition dune - TuniSchool
Cours En Ligne Pour s'inscrire : www tunischool com Page 1 sur 4 Titre Description I-/ Définition d'une pile II-/ Présentation de la pile Daniell 1-/ Schéma de |
|
10-Les piles électrochimiques - Physagreg
Chimie 2 2) Exemple : la pile Daniell : Voir TPχn°10 Expérience 2 3) Constitution d'une pile : ➢ Chaque pile électrochimique est constituée de deux demi-piles |
|
La pile Daniell (mémo)
La pile Daniell est constituée de deux compartiments/béchers appelés demi- piles : - Une demi-pile qui comprend une lame de cuivre plongeant dans une |
|
ÉTUDE DE LA PILE DANIELL - Unisciel
ÉTUDE DE LA PILE DANIELL 1) Montage i, EECS2-EECS1, EZn-EECS1, ECu -EECS2 (l'indice 1 est réservé à la demi pile contenant le zinc et l'indice 2 à |
|
STOCKAGE DE LÉNERGIE ÉLECTRIQUE : LES PILES - Mediachimie
Étude expérimentale de la pile Daniell 1re STI2D Thème • Matière et matériaux Partie • Transferts d'électrons lors d'une transformation chimique Capacités |
|
Pile Daniel - E-monsite
But : Réalisation et fonctionnement de la pile Daniell Matériel et produits : • Deux béchers de 100 ml • Une lame de zinc • Une lame de cuivre • Deux pinces |
|
ECE : Les piles électrochimiques - Académie dOrléans-Tours
John Daniell, professeur de chimie au King's College de Londres invente en 1836 la pile qui porte aujourd'hui son nom Il s'agit d'un élément impolarisable |
|
Les piles - Chapitre 1
Est-il possible lors de cette évolution spontanée de récupérer de l'énergie ? 1 Transferts spontanés d'électrons – Exemple de la pile Daniell 1 1 Transfert entre |
|
Résumé Introduction
2 avr 2007 · Les piles électrochimiques fournissent de l'énergie sur le principe des réactions redox La pile de Daniell utilise du sulfate de cuivre avec une |