Pile électrochimique
|
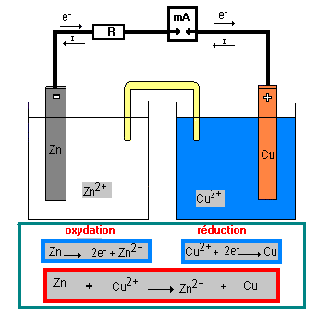
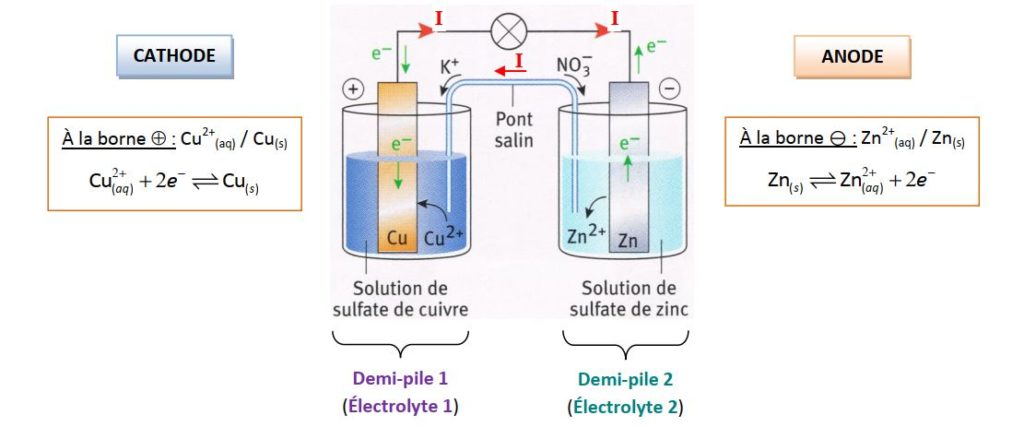
B) Fonctionnement de la pile Daniell : c) Réaction aux électrodes
-D'un pont salin qui relie les deux solutions La pile électrochimique convertit l'énergie chimique (résultant d'un transfert spontané d'électrons entre deux |
|
Oxydo-réduction et Piles électrochimiques SMPC2 fsr 2015
On considère la pile symbolisée par: Cu / Cu2+ (01M) // Fe2+ (01 M) /Fe 1) Calculer le potentiel de chaque électrode 2) Indiquer l'anode la cathode et |
|
10pilespdf
Les piles électrochimiques A : Petite parenthèse hydraulique B : Les piles au laboratoire 1 Descriptif 2 Un transfert spontané d'électrons 3 La pile |
|
Piles électrochimiques
fonctionnement de la pile Page 3 Réaction chimique et énergie électrique : les piles électrochimiques Matériel et Réactifs: - 4 béchers +/- 100 mL + 2 |
|
On appelle pile électrochimique tout dispositif qui permet dobtenir
✍ On appelle pile électrochimique tout dispositif qui permet d'obtenir du courant électrique grâce à une 1) La pile Daniell et les piles électrochimiques de |
|
Constitution dune pile électrochimique
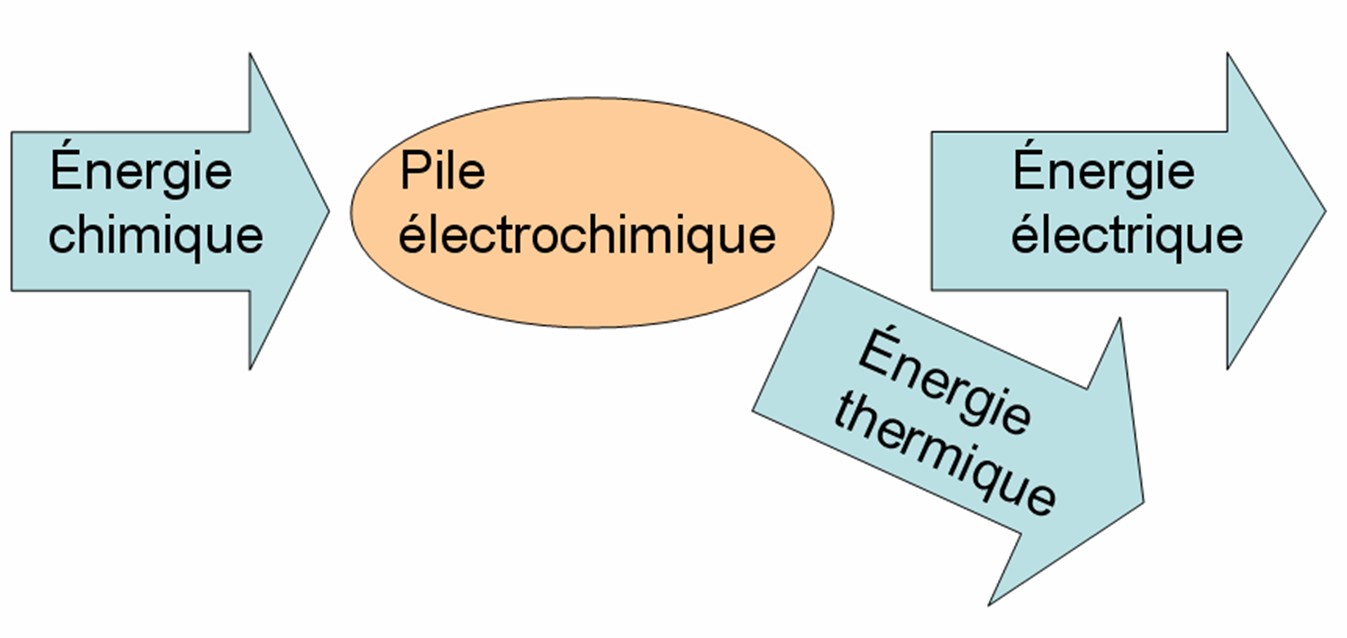
Une pile électrochimique est un générateur qui transforme une partie de l'énergie chimique venant d'une réaction d'oxydoréduction spontanée en énergie |
|
Chapitre 2 : Les piles électrochimiques
Une pile électrochimique est un dispositif qui convertit une énergie chimique en énergie électrique grâce à un transfert spontané indirect d'électrons entre |
Quels sont les 3 éléments essentiels qui constituent une pile ?
Elles sont constituées d'acier (godet), de zinc et de manganèse avec un électrolyte basique (majoritairement de la soude ou de la potasse).
Comment concevoir une pile électrochimique ?
Pour fabriquer une pile électrochimique, il suffit d'immerger deux métaux différents dans des électrolytes contenant leurs propres ions Mn+ , et relier ces deux électrolytes par un pont salin.
|
??????? ???? ??? ???? ??????? ???????? ??????? ??????
Deuxième exercice (7 points). Anode ou cathode ! Pour savoir si un métal est l'anode ou la cathode d'une pile électrochimique on compare sa tendance à perdre |
|
La pile électrochimique : source dénergie?
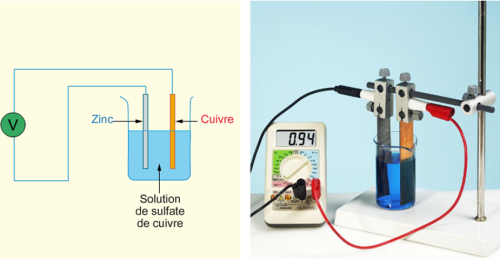
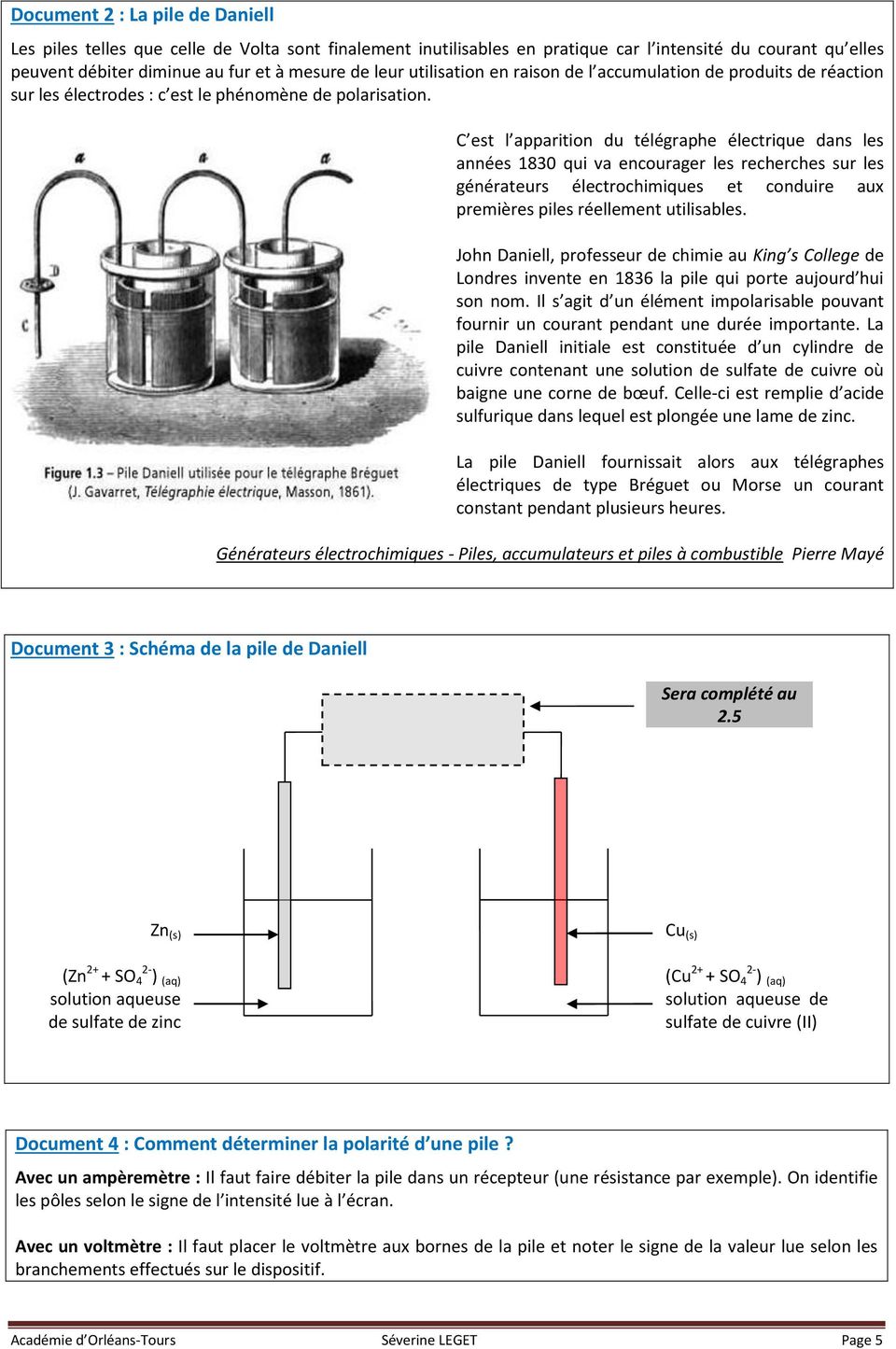
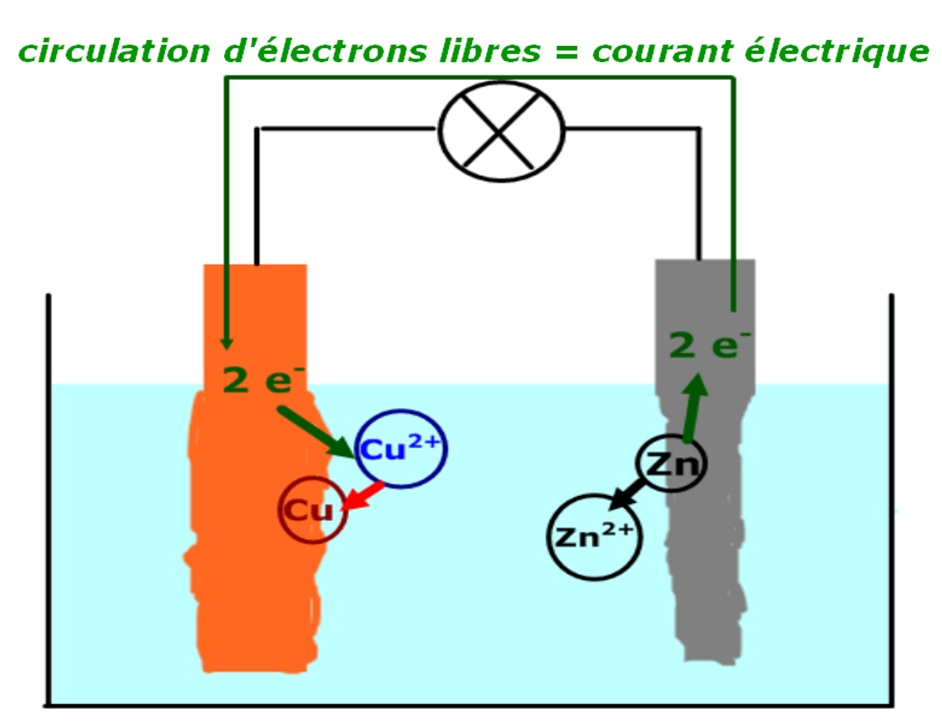
Une lame de zinc et une lame de cuivre plongées dans une solution de sulfate de cuivre constituent une pile électrochimique. Il existe une tension entre ces |
|
Les piles électrochimiques
A : Petite parenthèse hydraulique… B : Les piles au laboratoire. 1. Descriptif. 2. Un transfert spontané d'électrons. 3. La pile Daniell. |
|
I- La pile Daniell Cours chimie : Piles électrochimiques
spontanée est appelé pile électrochimique. Une pile est constituée de deux demi-piles reliées par une jonction électrochimique ou pont salin. |
|
Pile électrochimique
Une pile électrochimique est un dispositif qui convertit l'énergie chimique d'une réaction redox spontanée en électricité. Elle est utilisée comme source |
|
Les piles dispositifs mettant en jeu des transformations spontanées
Une pile électrochimique est un générateur qui transforme de l'énergie chimique fournie par une réaction d'oxydoréduction spontanée en énergie électrique. |
|
Chap 7 la pile électrochimique
Chap 7 La pile électrochimique. Quels sont les ions responsables de la couleur bleue de la solution de sulfate de cuivre? Pourquoi une solution de sulfate |
|
Doù vient lénergie fournie par une pile électrochimique ?
Je découvre. Document 1 : La découverte des piles. Bien que Alessandro Volta soit l'inventeur de la première pile d'autres chercheurs avant lui l'ont. |
|
Ch-8- La pile électrochimique Intro : Quel est le rôle dune pile
Le rôle d'une pile électrochimique est de transférer de l'énergie chimique en énergie électrique. On dispose du matériel suivant : Une plaque de cuivre : Cu(S). |
|
Chapitre 6 - Les piles électrochimiques
d'inventer la première pile électrochimique. II) Une transformation chimique peut-être produire de l'énergie ? 1) Expérience :. |
Comment fonctionne une pile électrochimique ?
. Une pile transforme une partie de l'énergie provenant de cette réaction chimique en énergie électrique.
Pourquoi Parle-t-on de pile électrochimique ?
Quelle est la nature de la réaction se produisant dans une pile électrochimique ?
. Pour que cette réaction se produise dans votre pile, il faut qu'elle dispose de deux matériaux.
. Ces deux matériaux vont générer un flux d'électrons.
. C'est de cette réaction d'oxydation-réduction que l'énergie électrique est produite.
Comment fabriquer une pile électrochimique en général ?
|
Chap4 Pile électrochimique et énergie chimique
Comment fabriquer une pile ? DI : Les calculs citronnés ont la patate Remarque : pour augmenter la tension, il faut associer deux piles en |
|
10-Les piles électrochimiques - Physagreg
Une pile électrochimique est un générateur qui transforme de l'énergie chimique fournie par une réaction d'oxydoréduction spontanée en énergie électrique |
|
Les piles électrochimiques Cours I-/ Définition dune - TuniSchool
Les piles électrochimiques Cours Cours En d'une pile II-/ Présentation de la pile Daniell 1-/ Schéma de la pile 3-/ Équation chimique associée à la pile |
|
Les piles électrochimiques
Les piles électrochimiques Petite parenthèse faut une centrale électrique (pile, batterie) cons- tituée de 2 dans le circuit extérieur de la pile, du potentiel |
|
ECE : Les piles électrochimiques - Académie dOrléans-Tours
Exploiter la transformation chimique considérée grâce à des mesures Compétences évaluées Coefficients respectifs Partie 1 : Sous-ECE «Les piles : de l' |
|
Les piles électrochimiques - MMorin
Il venait d'inventer la première pile électrochimique II) Une transformation chimique peut-être produire de l'énergie ? 1) Expérience : |
|
Filière sciences de la matière Cours délectrochimie SMC Semestre 5
positif en utilisant à ce pôle un système redox de tension plus élevée que celle de l'électrode à hydrogène a Piles impolarisables : Pile Daniell : + Cu / CuSO4 |
|
Piles et électrolyses - Studyrama
Dans la pile, les cations circulent de la demi pile à l'aluminium vers la demi pile au nickel et les anions en sens inverse ▻ Exercice n°2 1) Les électrons circulent |
|
313 Cellules électrochimiques - ESI
utilisées pour convertir l'énergie chimique en énergie électrique ❚ Types de cellules galvaniques d'importance commerciale: ❚ pile Leclanché Zn ❘ MnO 2 et |
|
Lélectrochimie
Chaque pile galvanique devrait comprendre : une anode (zinc), qui sera oxydée (perdra des e-) une cathode (cuivre) qui sera réduite (captera |