pile électrochimique cuivre fer
Quel est le métal qui constitue la borne négative de la pile ?
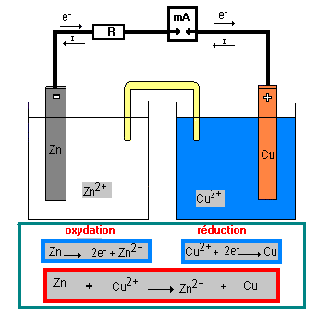
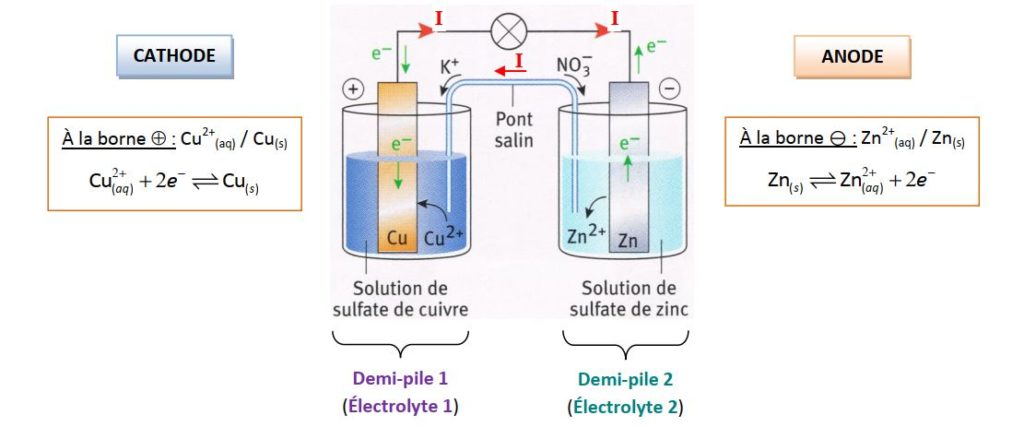
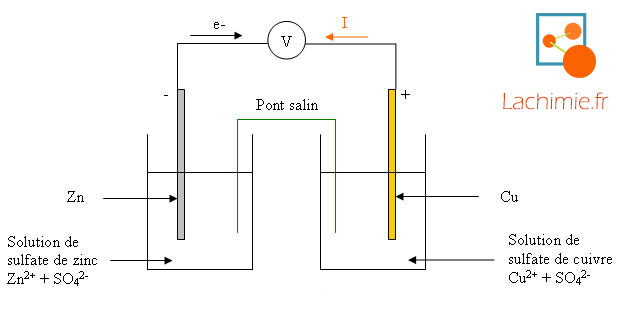
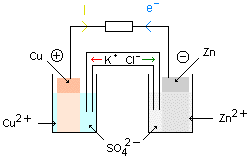
. A la borne négative il se produit une oxydation (perte d'électrons) de Zn en Zn2+.
. La borne positive est constituée par la cuivre.
Quel est le principe d'une pile électrochimique ?
. Une pile transforme une partie de l'énergie provenant de cette réaction chimique en énergie électrique.
Quel est le lien entre pile et corrosion ?
. L'effet pile est augmenté si la surface de métal noble est très supérieure à celle du métal non noble.
Comment fabriquer une pile électrochimique en général ?
|
Chap4 Pile électrochimique et énergie chimique
électrode en fer par de l'asphalte, et un cuivre N B Un petit buzzer fonctionne avec 2 piles (cuivre-zinc-citron) en série, chacune Pile sulfate de cuivre-Zinc |
|
Les piles et loxydo-réduction :
2 - Indiquer le signe des pôles de la pile formée ainsi que le sens de passage du courant Le couple du fer est oxydant vis à vis de celui du cuivre ( Volt 345 0 |
|
10-Les piles électrochimiques - Physagreg
chimique a lieu) : c'est le principe des piles électrochimiques II Constitution d ' une pile Faire le schéma au fur et à mesure de la Les électrons arrivent sur l' électrode de cuivre donc le courant sort de cette électrode il s'agit de la borne |
|
TD1 – Léquilibre rédox - Chamilo
à l'état de sulfate de fer (II) (FeSO4 totalement dissocié en Fe 2+ et SO4 2- Lorsque la pile est à l'équilibre (usée), la réaction redox a atteint l'équilibre De même l'équation électrochimique du couple Ni 2+ /Ni est : Ni 2+ objet en cuivre en l'immergeant dans une solution de chlorure de nickel (II) à 1 mol L -1 en |
|
Les piles électrochimiques
DOC 11 Les piles électrochimiques La pile Daniell (ou pile cuivre-zinc) est consti- tuée de lique plongeant dans une solution d'ions Fer III Fe3+ et d'ions |
|
Classification qualitative des couples oxydant réducteur - Fastef
plus fort que le cuivre Dans la classification électrochimique, le couple H+/H2 est donc situé entre le couple Fe2+/Fe et Cu2+/Cu 2- Pile Danielle : |
|
ECE : Les piles électrochimiques - Académie dOrléans-Tours
Générateurs électrochimiques - Piles, accumulateurs et piles à combustible Pierre Fer III (ferrique) Aluminium Cuivre II (cuivrique) Zinc Chlorure Formule |
|
Oxydo-réduction et corrosion
Les ions cuivre Cu2+ ont oxydé le fer : l'ion Cu2+ est un oxydant Une pile électrochimique est un générateur qui transforme de l'énergie chimique fournie par |
|
Chimie 12e année - Manitoba Education
[R] Chimie en solution aqueuse – l'oxydoréduction – piles électrochimiques [R ] Réaction entre l'acide nitrique concentré et le métal cuivre La galvanisation est un procédé où le fer est recouvert d'une couche de zinc protectrice |
|
Lélectrochimie
Inviter les élèves à construire une pile au citron (voir Chimie 11-12, p 611) OU Le fer métallique est oxydé en Fe2+, le Cu+ est réduit pour devenir du cuivre |