déterminer l'ordre d'une réaction chimique
|
TP 2 Détermination expérimentale de lordre dune réaction I
L'expérimentation comporte une partie : 1- Détermination de l'ordre d'une réaction en utilisant la méthode des vitesses initiales II 2- Matériels et réactifs |
|
9 Cinétique chimique
La détermination expérimentale de l'ordre d'une réaction complexe peut ainsi donner une information sur la molécularité de son étape cinétiquement |
|
Détermination de lordre dune réaction
Détermination de l'ordre d'une réaction La vitesse d'une réaction s'exprime éventuellement en fonction des concentrations : ○ des réactifs ○ des produits |
|
Cours-Cinétique-chimiquepdf
➢ La méthode des vitesses initiales (relatives) permet de déterminer l'ordre de réaction par rapport à chacun des réactifs ➢ Pour ce faire on compare les |
|
Loi de vitesse dune réaction chimique
La méthode des vitesses relatives permet de déterminer l'ordre de réaction par rapport à chacun des réactifs Pour ce faire on compare les vitesses initiales à |
|
Détermination expérimentale de lordre global de réaction
global de réaction L'ordre d'une réaction peut être déterminé à partir : ‐ de la courbe d'évolution temporelle (méthode longue) ‐ de la mesure du temps de |
|
Cinétique Chimique
1°/ Quel est l'ordre de cette réaction ? 2°/ Etablir l'expression donnant la variation de la concentration en fonction du temps 3°/ Calculer la constante |
|
Cinétique chimique
Lorsque l'équilibre chimique est atteint une réaction directe et sa réaction Détermination de l'ordre d'une réaction 2 1 Méthode intégrale pour un seul |
Comment déterminer l'ordre d'une réaction chimique ?
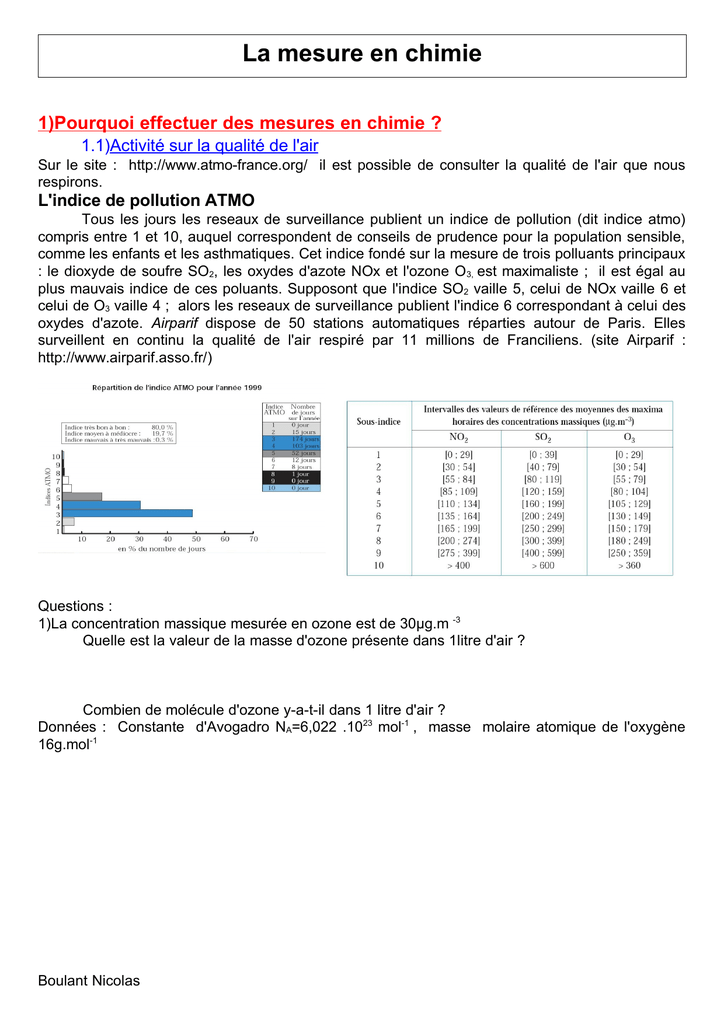
Vérification de l'ordre 2 à partir des temps de demi-vie
On constate immédiatement que le temps de demi-vie varie avec la concentration initiale, la réaction n'est donc pas du premier ordre.
Pour vérifier si elle est du second ordre, calculez le produit t 1 2 × C A , 0 pour chaque expérience.Comment savoir si une réaction est d'ordre 2 ?
Si des réactifs ont disparu lors de la réaction, alors il s'agit d'une transformation chimique.
Si des produits sont apparus lors de la réaction, alors il s'agit d'une transformation chimique.
Si aucun des réactifs n'a disparu et si aucun des produits n'est apparu, alors il ne s'agit pas d'une transformation chimique.Comment déterminer une réaction chimique ?
Soit par exemple une réaction : A + B = P dont la loi de vitesse serait.
C A α .
C B β et l'ordre global n = α + β .
La réaction apparaît donc comme étant d'ordre alors qu'elle est en réalité d'ordre .
|
Loi de vitesse dune réaction chimique
Presque toutes les réactions chimiques se produisent plus rapidement lorsqu'on élève la température. L'équation d'Arrhenius permet de déterminer l'énergie d' |
|
Génie de la Réaction Chimique: les réacteurs homogènes
14 juil. 2022 Déterminer le temps nécessaire pour une conversion de 50% de l'acide acétique. Réacteurs idéaux isothermes. 38. Marie DEBACQ. Page 40. e ... |
|
Reaction chimique - Thermodynamique - Cinétique
Dans l'état initial nA = 0.3 mol |
|
Cinétique chimique
Calculer la concentration initiale des réactifs dans le mélange. 2. Exprimer la vitesse de la réaction si les ordres partiels sont un par rapport à chaque. |
|
Exercices : cinétique macroscopique corrigés
La constante de vitesse de la réaction. 2 N2O5(g) ? 4 NO2(g) + O2(g) double quand on passe de 2250°C à 27 |
|
Cinétique chimique
Détermination de l'ordre d'une réaction. 2.1 Méthode intégrale; 2.2 Méthode du temps de demiréaction. 2.3 Méthode de la vitesse initiale; 2.4 Méthode des |
|
Cinétique enzymatique
La cinétique est l'étude des vitesses des réactions chimiques. La cinétique enzymatique a pour but de déterminer les vitesses des réactions que l'enzyme |
|
La chimie
afin de déterminer l'effet de la concentration d'un réactif sur la vitesse de la réaction dans cet exemple la réaction est d'ordre x en A et d'ordre. |
|
Détermination de lordre dune réaction
On souhaite déterminer les ordres partiels et la constante de vitesse k. Page 2. Cas où v = k.[A]p. Il existe plusieurs |
|
Cinétique chimique - vitesse de réaction
Lors d'une réaction chimique la quantité de matière du constituant A à l'instant t Cette méthode permet de déterminer l'ordre initial mais pas l'ordre ... |
|
Cinétique chimique - UNF3S
Savoir définir et déterminer l'ordre d'une réaction chimique, la dégénérescence de l'ordre – Loi empirique d'Arrhenius, énergie d'activation • Savoir exprimer et |
|
Cinétique chimique - Chimie en PCSI
Calculer la concentration initiale des réactifs dans le mélange 2 Exprimer la vitesse de la réaction si les ordres partiels sont un par rapport à chaque réactif |
|
2007
La vitesse d'une réaction chimique est la variation de concentration d'un produit en Nous avons déterminé l'ordre partiel de la réaction entre I- et S2O8 2- |
|
Comment calculer [A]=f(t) et trouver lordre dune réaction ?
3) En déduire p en fonction du temps t méthode physique Méthodes de suivi d' une cinétique formelle méthode chimique grandeur physique |
|
Cours de chimie g´en´erale Pr´eparation au concours B des ´ecoles
La cinétique chimique est l'étude de la cinétique des réactions chimiques En d' autres termes comment peut-on trouver l'ordre de la réaction ? Le principe de |
|
Cinétique chimique
Avec k: constante de vitesse et p, q ordres partiels par rapport aux réactifs Ai1 et Ai2 La somme p + q = α ordre global de la réaction Remarques : • l'ordre partiel p |
|
Cinétique chimique
1 7 Cinétique de réactions d'ordre 1 proches de l'équilibre 1 8 Expression d'une équation cinétique et d'une loi de vitesse intégrée 2 Détermination de l'ordre |
|
Cinétique chimique - Lycée dAdultes
Suivi expérimental de la vitesse de réaction et temps de demi-réaction • Loi de vitesse d'une réaction d'ordre 1 (Vidéo3) 1 1 Facteurs cinétiques et catalyse |