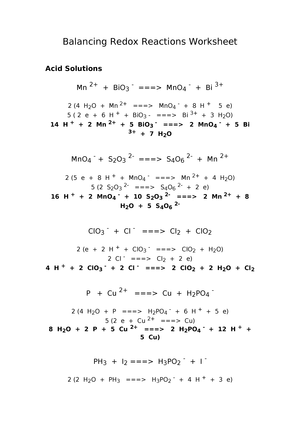s4o6 2- / s2o3 2-
|
Balancing Redox Reactions Worksheet
Balancing Redox Reactions Worksheet 1 Balance each redox reaction in acid solution Mn 2+ + BiO3 - MnO4 + Bi 3+ - Æ MnO4 - + S2O3 2- Æ S4O6 2- + Mn 2+ ClO3 - + Cl - Æ Cl2 + ClO2 P + Cu 2+ Æ Cu + H2PO4 - - - PH3 + I2 Æ H3PO2 + I |
How do you balance the equation S2O3 2 2- + i2 s4o6?
To balance the equation S2O3 {2-} + I2 = S4O6 {2-} + I {-} using the algebraic method step-by-step, you must have experience solving systems of linear equations. The most common methods are substitution/elimination and linear algebra, but any similar method will work.
Is s4o6/s2o3 reversible at inert electrodes?
Here we report protein film electrochemistry that defines the reduction potential of the S4O6 (2-)/S2O3 (2-) couple. The relevant interconversion is not reversible at inert electrodes.
How do you balance MnO4 with oxygen atoms?
The first step in balancing this reaction using step 3 is to add4 H 2 O atoms in order to balance the Oxygen atoms with the 4 on the other side of MnO4- Now that the Oxygen atoms have been balanced you can see that there are 8 H atoms on the right hand side of the equation and none on the left.
|
Exercice 29 p 131 : a) Équation de la réaction : Oxydation de S2O3
Oxydation de S2O3. 2-. (aq) : 2 S2O3. 2-. (aq) = S4O6. 2-. (aq) +2e-. Réduction de I2(aq) : I2(aq) + 2e- = 2I-. (aq). 2 S2O3. 2-. (aq) + I2(aq). S4O6. 2-. (aq) |
|
CHAP 0 : REVISIONS : OXYDO-REDUCTION
(aq) + 2 e- = 2 S2O3. 2-. (aq). 4. Equation d'une réaction d'oxydoréduction. Une (aq) → 5 S4O6. 2-. (aq) + 2 Mn2+. (aq) + 8 H2O. Page 2. 2. |
|
Chapitre 2 28 Concentration en ion thiosulfate dune solution On a
2− (aq) → 2 I– (aq) + S4O6. 2− (aq). La solution de diiode de concentration c1 = 80 × 10–2 mol.L–1 est diluée vingt fois avant. |
|
CH3 TABLEAUX DAVANCEMENT
+ S4O6. 2–. (aq). Remarque : signe égal ou double flèche dans les demi-équations 2 S2O3 2-. + I2. → 2 I-. + S4O62–. État du système Avancement. Quantités de ... |
|
2. t∞
2 I- (aq) + S4O6 2- (aq) ... 1ère méthode: d'après l'équation chimique les proportions stoechiométriques sont de 2mol de. S2O3 2- pour 1mol de I2 donc de 2 ... |
|
Ecrire une Réaction doxydo-réduction Correction
2-. (réducteur du couple : S4O6. 2- / S2O3. 2-. ) ½ équation : H2O2 + 2 H. +. + 2 e- = 2 H2O. ½ équation : 2S2O3. 2- = S4O6. 2-. + 2 e-. Equation (2) : H2O2 + 2 |
|
Potentiels standard de quelques couples oxydoréducteurs
SO2 + 4H+ +6e- <--> S4O62- + 2 H2O. 051. SO4. 2-. / SO2. 0 |
|
1S CHIM CH6 TP8 AVANCEMENT corrige.pub
2– . Ajustez les nombres stœchiométriques. 2 S2O3. 2--. (aq) + I2 (aq) → S4O6. |
|
2- → 2 I + S4O6
I Transformation chimique rapide. Le diiode I2 de couleur marron en solution aqueuse réagit avec une solution aqueuse de thiosulfate de sodium (incolore) |
|
Teneur en dioxygène dissous dans une rivière
2– : 2 S2O3. 2– = S4O6. 2– +2 e–. Bilan : I2 + 2 S2O3. 2– → 2 I– + S4O6. 2– b. Le diiode est le réactif titré l'ion thiosulfate le réactif titrant. L |
|
Exercice 29 p 131 : a) Équation de la réaction : Oxydation de S2O3
2 S2O3. 2-. (aq) + I2(aq). S4O6. 2-. (aq) + 2I-. (aq) b) Il s'agit d'une réaction d'oxydoréduction car il a un échange d'électrons entre deux espèces (I2. |
|
1 S4 Loxydoréduction - Correction Activité H2O2/H2O S4O6 /S2O3
26 avr. 2016 S4. L'oxydoréduction - Correction. Activité. I. Définitions et méthode à mémoriser. II. Pour écrire la demi-équation d'oxydoréduction ... |
|
CHAP 0 : REVISIONS : OXYDO-REDUCTION
2. Couples oxydant/réducteur. Un couple oxydant/réducteur est formé de deux 2 I-. (aq). S4O6. 2-. (aq)/ S2O3. 2-. (aq) S4O6. 2-. (aq) + 2 e- = 2 S2O3. |
|
Oxydant Réducteur E0 (Volt)
F2+2 e-. 2F-. 2.87. O(g) + 2 H+ +2 e-. H2O. 2.43. S2O8. 2- +2H+ +2 e- S4O6. 2-+6 H2O. 0.51. H2SO3+4 H++4 e-. S(s)+3 H2O. 0.50. S2O3. 2-+6 H++4 e-. |
|
Chapitre 2 28 Concentration en ion thiosulfate dune solution On a
L'équation de la transformation est : I2 (aq) + 2 S2O3. 2? (aq) ? 2 I– (aq) + S4O6. 2? (aq). La solution de diiode de concentration c1 = 80 × 10–2 mol. |
|
2. t?
I2 (aq) + 2e- = 2I- (aq). S4O6 2- (aq) + 2e- = 2S2O3 2- (aq). 2. et V2=1mL de solution de thiosulfate de sodium avec [S2O32-]=C2 donc une quantité de ... |
|
The chemistry of thiosulphate ions
I2(s) + 2S2O3. 2–(aq) ? S4O6. 2–(aq) + 2I–(aq). However in this experiment students investigate some of the many interesting reactions of sodium. |
|
TP12 DOSAGE du DIIODE par OXYDORÉDUCTION 1) 2)Les
2- : Ils figurent donc chacun dans le 1er membre de leur demi-équationd'oxydoréduction: I2 /I-. : I2. + 2e- = 2I-. S4O6. 2-/S2O3. 2- : 2S2O3. 2-. = S4O6. |
|
I2 + 2 é 2I- S2O3 S4O6 2- + 2 I
All indirect iodometric titrations are based on the titration of iodine with thiosulfate. Stochiometric reaction equation: S2O3. 2- + I2. S4O6. 2- + 2 I. |
|
1S CHIM CH6 TP8 AVANCEMENT corrige.pub
2– . Ajustez les nombres stœchiométriques. 2 S2O3. 2--. (aq) + I2 (aq) ? S4O6. 2–. (aq) + 2 I–. Les ions sodium n'apparaissent pas dans l'équation car ce |
|
Exercice 29 p 131 : a) Équation de la réaction : Oxydation de S2O3
2 S2O3 2- (aq) = S4O6 2- (aq) +2e- Réduction de I2(aq) : I2(aq) + 2e- = 2I- (aq) 2 S2O3 2- (aq) + I2(aq) S4O6 2- (aq) + 2I- |
|
CHAP 0 : REVISIONS : OXYDO-REDUCTION
(aq) S4O6 2- (aq) + 2 e- = 2 S2O3 2- (aq) 4 Equation d'une réaction d'oxydoréduction Une réaction d'oxydoréduction est un échange d'électrons entre |
|
TP12 DOSAGE du DIIODE par OXYDORÉDUCTION
2- : Ils figurent donc chacun dans le 1er membre de leur demi-équationd'oxydoréduction: I2 /I- : I2 + 2e- = 2I- S4O6 2-/S2O3 2- : 2S2O3 2- = S4O6 |
|
Chapitre 2 28 Concentration en ion thiosulfate dune solution On a
28 Concentration en ion thiosulfate d'une solution On a : I2 (aq) + 2 e– = 2 I– (aq) et 2 S2O3 2? (aq)= S4O6 2? (aq) + 2 e– |
|
2 t? - Scientillula
I2 (aq) + 2e- = 2I- (aq) S4O6 2- (aq) + 2e- = 2S2O3 2- (aq) 2 a La solution est bleu-violet très sombre quasiment noire : le complexe diiode-empois |
|
Réactions doxydo-réduction - A9lame
Il apparaît un précipité vert d'hydroxyde de fer (II) (voir photographie) (aq) ion tétrathionate ion thiosulfate S4O6 2- (aq) + 2e- 2S2O3 2- |
|
CH3 TABLEAUX DAVANCEMENT
sachant qu'il se forme des ions iodure I– et des ions tétrathionates S4O62– Ajustez les nombres stœchiométriques 2 S2O3 2- (aq) +2e- ???? S4O6 2– |
|
1S CHIM CH6 TP8 AVANCEMENT corrigepdf
2– Ajustez les nombres stœchiométriques 2 S2O3 2-- (aq) + I2 (aq) ? S4O6 2– (aq) + 2 I– Les ions sodium n'apparaissent pas dans l'équation car ce |
|
Demi-équation oxydoréduction : S4O62- / S2O32- - YouTube
22 jan 2021 · Comment ajuster la demi-équation du couple S4O62- / S2O32-? ion tetrationate ion thiosulfate Durée : 4:21Postée : 22 jan 2021 |
| PROBLEM SET No 1 - OXIDATION REDUCTION REACTIONS & STOICHIOMETRY |
| Kinetics of Iodine Clock Reaction - Bellevue College |
| Balancing Redox Reactions Worksheet - Mr Miller's Classes |
| Reaction Kinetics: The Iodine Clock Reaction - Bellevue College |
| CHM 115 Lab 14 Kinetics: Concentration Effects - Theochem |
| Searches related to s4o6 2 / s2o3 2 filetype:pdf |
|
A) Équation de la réaction : Oxydation de S2O3 2 S2O3 - MMorin
Exercice 29 p 131 : a) Équation de la réaction : Oxydation de S2O3 2- (aq) : 2 S2O3 2- (aq) = S4O6 2- (aq) +2e- Réduction de I2(aq) : I2(aq) + 2e- = 2I- (aq) |
|
Corrigé de lExamen du 21 janvier 2010 - durée : 2 - lutesupmcfr
Qui joue le rôle de réducteur ? Ecrire l'équation de dosage entre le diiode I2 et l' ion thiosulfate I2 + 2 e- = 2 I- : I2 joue le rôle d'oxydant 2 S2O3 2- = S4O6 |
|
TP12 DOSAGE du DIIODE par OXYDORÉDUCTION 1) 2)Les
4) tableau d'avancementde la réaction de dosage àl'équivalence: Avancement I2 + 2 S2O3 2- → 2 I - + S4O6 2- Etat initial X = 0 C1 V1 C2 (V2)eq 0 0 |
|
La réaction doxydoréduction - Free
2-/S2O3 2-, (ion tétrathionate/ion thiosulfate) établir la demi-équation de ce couple : S4O6 2- (aq)+2e-= 2S2O3 2- (aq) On désire faire réagir le diiode avec |
|
1 S4 Loxydoréduction - Correction Activité H2O2/H2O S4O6 /S2O3
26 avr 2016 · 2) S4O6 2- = 2 S2O3 2- 3) S4O6 2- = 2 S2O3 2- 4) S4O6 2- = 2 S2O3 2- 5) S4O6 2- + 2 e - = 2 S2O3 2- SO2/S2O3 2- 1) SO2 = S2O3 |
|
Le dosage comporte les étapes suivantes : - AC Nancy Metz
Retrouver l'équation correspondant à la réaction (4) sachant que les couples redox mis en jeu sont les couples I2/I- et S4O6 2-/S2O3 2- I2 + 2 e- = 2I- 2 S2O3 |
|
Correction 2x
S4O6 2- + 2 e- 2 S2O3 2- + I2 2I- + S4O6 2- 10 Le point d'équivalence est atteint lorsque les réactifs sont introduits dans les proportions stœchiométriques |