preparation d'une solution en laboratoire
|
Manipulations dans les laboratoires de chimie
laboratoire en terme de : • répartition des surfaces • répartition des matériels et appareillages • utilisation et entretien des systèmes de ventilation • entretien des matériels • règles de fonctionnement • stockage de produits (le stock sera minimum et corres - pondra autant que possible au travail d’une journée) [1] ; |
|
CHAPITRE I PREPARATION DE SOLUTIONS
Solution sursaturée : une solution sursaturée est une solution contenant une plus grande quantité de soluté dissous que celle qui correspond à la limite de saturation d)- La dilution : la dilution d’une solution aqueuse consiste à en diminuer la concentration par ajout de solvant (eau) |
|
TP N°=1 de chimie S1: Préparation des solutions
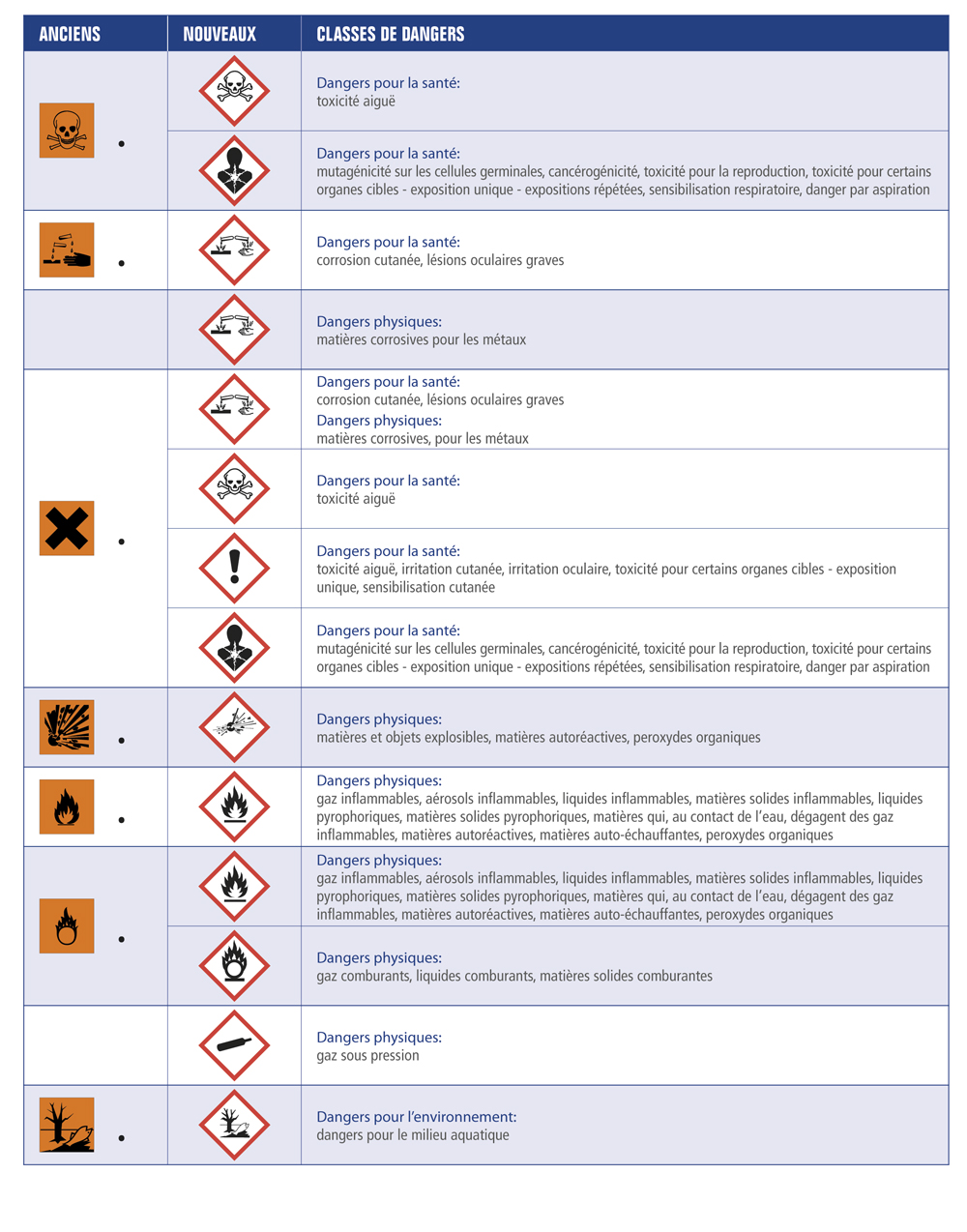
Connaitre les consignes de sécurité à respecter dans un laboratoire de chimie Connaitre les risques des produits chimiques Comprendre les différentes utilisations de la verrerie pour la réalisation d’un TP en chimie Apprendre à préparer des solutions à partir des solides ou des liquides |
|
Lab : préparation d’une solution mère réalisation de dilutions
Objectifs : Préparer une solution mère Réaliser des dilutions d’une solution mère Observer la relation proportionnelle entre la concentration d’une solution et la densité relative Déterminer la concentration d’une solution de NaCl inconnue |
|
TP N° 2 Préparation d’une solution par dissolution ou par
Au laboratoire on peut se retrouver face à 3 types de situations à savoir de devoir préparer une solution : par dissolution d'un solide par dilution d'un liquide plus concentré en connaissant sa concentration |
Quels sont les enjeux de la préparation de solutions en laboratoire ?
La bonne maitrise des techniques de préparation de solutions en laboratoire, revêtent un enjeu capital en chimie. L’expérimentateur doit être à même de préparer des solutions a partir de liquides ou de solides et de pouvoir effectuer cela à différentes concertations tout en diminuant au maximum les erreurs de manipulation.
Comment préparer une solution à partir d'un liquide ?
Pour préparer une solution à partir d’un liquide, la mesure précise des volumes est d'une grande importance au laboratoire. Elle peut être effectuée à l'aide d'une pipette jaugée ou graduée, d'une burette graduée ou d'une fiole jaugée.
l'issu de cet TP, l'étudiant sera capable de :
Connaitre les consignes de sécurité à respecter dans un laboratoire de chimie. Connaitre les risques des produits chimiques. Comprendre les différentes utilisations de la verrerie pour la réalisation d’un TP en chimie. Apprendre à préparer des solutions à partir des solides ou des liquides. staff.univ-batna2.dz
I. Sécurité et verrerie
Consignes de sécurité à respecter en TP de Chimie Porter une blouse en coton boutonnée. Avoir les cheveux attachés s’ils sont longs. Porter des lunettes de protection et des gants lors de la manipulation de produits corrosifs. Laisser les passages libres. Travailler en position stable. Utiliser du matériel propre et en bon état. Se laver
II. Préparation des solutions
Définition d’une solution : est un mélange liquide homogène des molécules d’un liquide (solvant) et d’un solide (soluté), d’un gaz, d’un autre liquide dans les proportions variables et sans qu’il y ait une réaction chimique. Solution = Soluté + Solvant. Un solvant : est une substance liquide qui dissout (absorbe) d’autres substances. C’est le co
La concentration massique Cm
La concentration massique d’une espèce chimique en solution est la masse de soluté présente par litre de solution. Elle s’exprime en g/L. Cm= m (soluté)/V(solution). (m en g et V en L). staff.univ-batna2.dz
La normalité N
La normalité (ou concentration normale) indique la relation entre le nombre d'équivalent-gramme 'ne' de soluté et le volume de la solution. Il existe une relation entre la normalité et la concentration molaire : N= x × C (x est le nombre d'équivalents). staff.univ-batna2.dz
La densité d
La densité relative d'un corps est le rapport de sa masse volumique à la masse volumique d'un corps pris comme référence. Pour les liquides et les solides, le corps de référence est l'eau pure. d= ρcorps/ ρeau La préparation des solutions se fait généralement par : dissolution ou dilution. La dissolution : est le processus physico-chimique par
(solution diluée).
Pour déterminer le volume ou la concentration initiale ou finale de solutions, on peut utiliser la relation suivante : staff.univ-batna2.dz
MH2SO4 = 98 g/mol.
Remarque : Attention, toujours verser l'acide dans l'eau et non l'inverse. staff.univ-batna2.dz
|
CHAPITRE I PREPARATION DE SOLUTIONS
lors de la préparation de solutions au laboratoire : 1)- Masse molaire (M) : La masse molaire est la masse d'une mole d'un composé chimique |
|
Comment préparer une solution de chlore à 005 % (faible
Répétez jusqu'à ce que le seau soit plein. Placez aux stations de lavage des mains. Utilisez une solution de chlore à 005 % (faible concentration) pour laver |
|
TRAVAUX PRATIQUES DE CHIMIE I
Ce manuel reprend les mesures de sécurité qu'il faut respecter dans un laboratoire de chimie les différentes méthodes de préparation de la solution et la |
|
PRÉPARATION DUNE SOLUTION DE TRAVAIL GIEMSA
Certains laboratoires préfèrent colorer les lames une à une même en cas de lots importants |
|
Solutions aqueuses Ce quil faut retenir
La dilution permet de préparer une solution peu concentrée (la solution fille) à partir d'une solution trop concentrée (la laboratoire de chimie :. |
|
Travail dirigé 5 : La concentration dune solution
On désire préparer 250 mL d'une solution de KBr 85 g/L. Quelle masse de KBr solide doit On dispose au laboratoire d'une solution 2 M en soude caustique. |
|
Méthodes de laboratoire en parasitologie intestinale
Donc technique la plus couramment utilisée dans les laboratoires. Note : préparer au moins 500 ml de la solution B et éliminer le reste s'il y a lieu. |
|
Risque chimique dans les laboratoires de biologie moléculaire
Aliquote : une solution aliquote est obtenue par séparation d'une solution en plusieurs parties cléotides de synthèse la préparation de plasmides et la. |
|
Comment préparer une solution de chlore à 05 % (haute
Versez 2 portions d'eau de javel et 3 portions d'eau dans un seau. Répétez jusqu'à ce que le seau soit plein. Mélangez bien pendant 10 secondes. |
| CHAPITRE I PREPARATION DE SOLUTIONS |
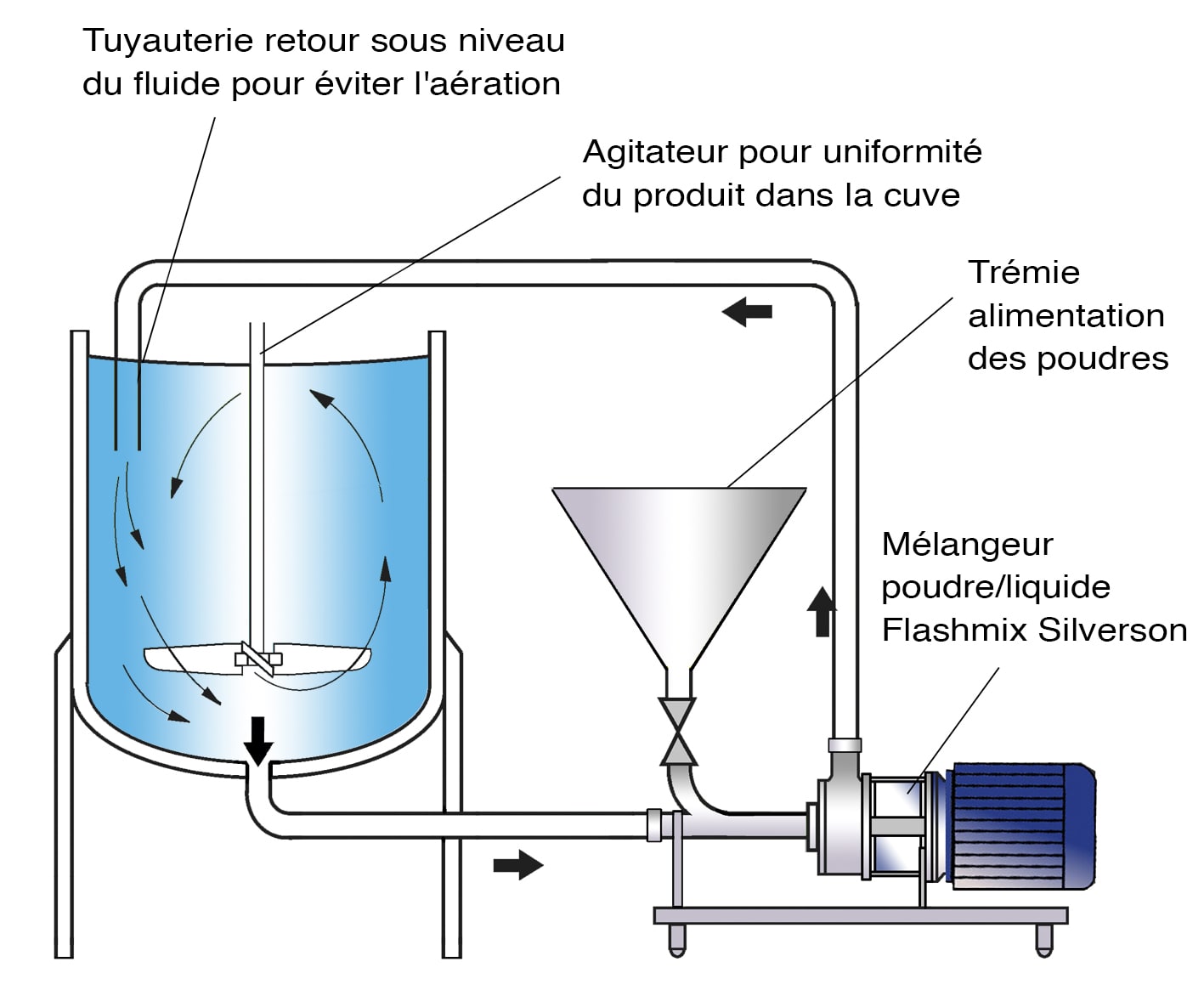
| Le dispositif de préparation d’une solution |
| TRAVAUX PRATIQUES DE CHIMIE I - univ-tiaretdz |
| Lab : préparation d’une solution mère réalisation de dilutions |
| Santé -TP n°7 : Préparation d’une solution Dilution |
| TP N°11 : PREPARATION DE SOLUTIONS - Physagreg |
| Searches related to preparation d une solution en laboratoire filetype:pdf |
|
Introduction à la chimie des solutions et bonnes pratiques de
30 jan 2015 · pratiques de laboratoire Techniciens de laboratoire – 6 personnes maximum Préparation d'une solution par dilution d'une solution de |
|
Préparation de lanalyse - INRS
Traiter les blancs de laboratoire et les blancs de terrain de la même façon Préparer une solution NaOH 0,1N en solubilisant 0,4 g de NaOH pur dans 100 mL |
|
Préparation de lanalyse - INRS
Traiter les blancs de laboratoire et blancs de terrain de la même manière que les échantillons prélevés Toutes les solutions sont filtrées avant dosage |
|
FICHE PROTOCOLE PREPARATION DUNE SOLUTION PAR
Préparer une solution par dissolution d'un solide dans l'eau, de façon à obtenir une concentration molaire en soluté apporté précise MATERIEL NECESSAIRE : - |
|
Protocoles et procédures Table des Matières - Université de Montréal
20 oct 2005 · Procédures expérimentales⎯Laboratoire de chimie analytique Préparation du standard 5 mg/L On verse quelques ml de la solution étalon |
|
Densité dun solide - Préparation dune solution - Dilution ENONCE
Un technicien de laboratoire veut préparer 500 mL d'une solution de sulfate de cuivre (II) de concentration C = 0,10 mol / L Le laboratoire dispose de sulfate de |
|
(Corr de TP n°7préparation solutiondilution)
I La verrerie au laboratoire II- Préparation d'une solution de produit phytosanitaire Préparer les solutions aqueuses de sulfate de cuivre suivantes : Masse à |
|
TRAVAUX PRATIQUES DE CHIMIE I - Université Ibn Khaldoun de
faisant appel à du matériel simple retrouvé aisément dans les laboratoires Préparation de 100 mL d'une solution de NaOH 0,01 N à partir de la solution mère |
|
PRÉPARATION DUNE SOLUTION ÉTALON
Préparer 100,0 ml de solution étalon de 0,200 M de sulfate de cuivre Pendant ce laboratoire, quels éléments devaient rester secs et lesquels auraient pu être |
|
Solutions aqueuses Ce quil faut retenir - Lycée Maurice Ravel
La dilution permet de préparer une solution peu concentrée (la solution fille) à partir d'une solution trop concentrée (la laboratoire de chimie : Bécher, balance |