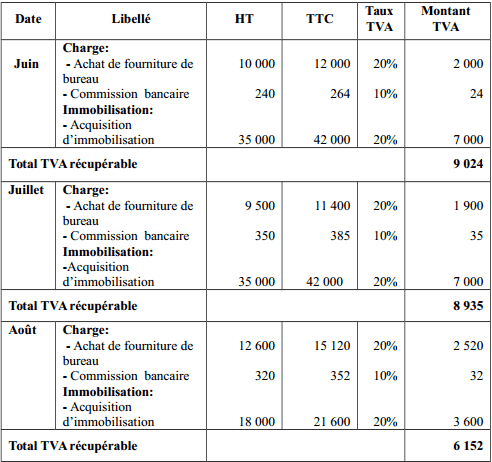
préparation de solution titrée
|
Solutés Une solution titrée Ces relations sont à connaître ou à
Une solution titrée est une solution de concentration connue Quelle relation peut-on écrire entre : ➢ M m et n ? ➢ C n et V ? |
|
TP N° 2 : Préparation dune solution par dissolution ou par dilution
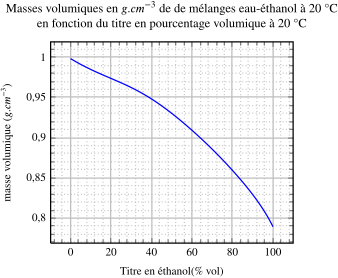
a)- Déterminer le titre massique de la solution 2 sachant que la masse volumique de l'éthanol est μ = 079 g / ml b)- Quelles sont les espèces présentes |
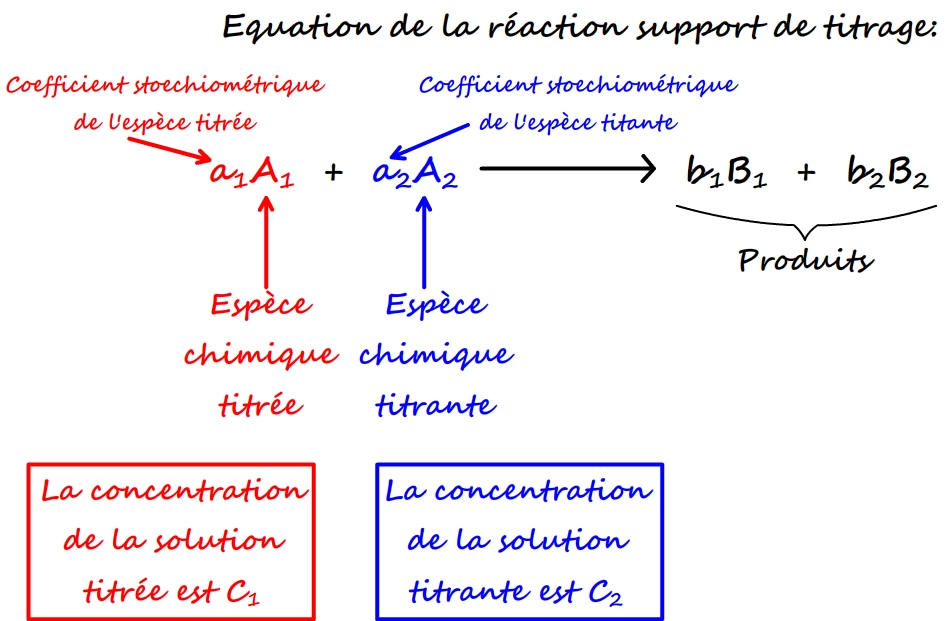
C'est quoi une solution titrée ?
Avant le titrage, les réactifs sont séparés en deux solutions.
Dans l'une des deux se trouve l'espèce dont la concentration est inconnue, il s'agit de la solution titrée.
Dans l'autre se trouve un réactif dont la concentration est parfaitement connue, il s'agit de la solution titrante.Comment calculer le titré de la solution ?
C'est le rapport de la masse de composé X contenu dans un certain volume de solution divisée par ce volume de solution.
|
Solutés. Une solution titrée Ces relations sont à connaître ou à
FICHE 4 : COMMENT PRÉPARER UNE SOLUTION TITRÉE ? Une solution est un mélange homogène formé du solvant en large excès et d'un voire de plusieurs. |
|
Préparation dune solution titrée CA = nA V
Quelle est la concentration d'une solution obtenue par dissolution de 0050 mol de diiode III PREPARATION DUNE SOLUTION TITREE A PARTIR DUN SOLUTE :. |
|
……………………………………….. I) Buts : Préparer une solution
Preparer une solution titrée de chlorure de sodium ( ) de volume = 100 et de concentration molaire = 2 . . ?Déterminer la masse du soluté à dissoudre. |
|
CHAPITRE I PREPARATION DE SOLUTIONS
c)- Solutions aqueuses : Une solution ayant l'eau comme solvant est dite solution aqueuse. Il est possible de mettre en solution : ? Un liquide dans un autre |
|
UNIVERSITE DE LIMOGES l50-Qoefî2^N
PREPARATION DE SOLUTIONS TITREES. Solutions titrées de chlore et solutions -permettant de doser le chlore résiduel. - - Hypochlorite de sodium. |
|
TP N° 2 : Préparation dune solution par dissolution ou par dilution.
On souhaite préparer V=100mL d'une solution de chlorure de sodium NaCl à C=010 mol/L. La masse molaire du chlorure de sodium est MNaCl=58 g/mol. Calculons la |
|
Comment préparer une solution de chlore à 05 % (haute
Versez 2 portions d'eau de javel et 3 portions d'eau dans un seau. Répétez jusqu'à ce que le seau soit plein. Mélangez bien pendant 10 secondes. |
|
FICHE DE PREPARATION BRANCHE: CHIMIE ECOLE : C.S J.M DE
PROF : Fred KAMARA. SUJET DE REVISION : Préparation des solutions titrées. CLASSE : 3e Scientifique. SUJET DE LECON : Préparation par dissolution. |
|
TRAVAUX PRATIQUES DE CHIMIE I
chimie les différentes méthodes de préparation de la solution et la détermination de sa Rincer la burette graduée avec la solution titrante (NaOH). |
|
Labo théorique : Dosage de lacide chlorhydrique par titrage
Déterminer le mode de préparation d'une solution de biphtalate de potassium et la préparer. • Étalonner une solution titrante d'hydroxyde de sodium à l'aide |
| COMMENT PREPARER UNE SOLUTION TITRÉE D'UNE ESPÈCE CHIMIQUE |
| TP verrerie /dissolution / dilution - ac-lyonfr |
| TP1 Préparation d’une solution titrée I SOLUTION AQUEUSE |
| Labo théorique : Dosage de l’acide chlorhydrique par titrage |
| Protocole Réaliser une dilution - Cours de Physique Chimie |
| Searches related to préparation de solution titrée filetype:pdf |
Quels sont les objectifs du TP?
- ?Objectifs du TP : - Utiliser la verrerie à bon escient - Utiliser la balance de précision (10-4) (Distribuer la Fiche technique RN Chimie 1). - savoir préparer une solution de concentration connue par dissolution et par dilution ?Informations présentes sur la verrerie :
Comment limiter la température d’une réaction de dissolution?
- Certaines réactions de dissolution sont exothermiques et il l’eau introduite au départ permet ainsi de limiter les variations de température). ?A l’aide d’un entonnoir à solide (bout tronqué), rincé à l’eau, introduire le solide.
Comment se débarrasser d’une réaction de dissolution?
- Certaines réactions de dissolution sont exothermiques et il l’eau introduite au départ permet ainsi de limiter les variations de température). ?A l’aide d’un entonnoir à solide (bout tronqué), rincé à l’eau, introduire le solide.
. Rincer l’entonnoir dans la fiole. ?Agiter (mouvement circulaire) afin de dissoudre le solide.
|
Préparation simplifiée de solutions éthanoliques de titre - ANSM
PRÉPARATION SIMPLIFIÉE DE SOLUTIONS Volumes d'éthanol de titre X pour cent V/V et d'eau à mélanger, à 20°C, pour obtenir 1000 mL d'éthanol de titre |
|
Les solutions
Ainsi la préparation du combustible nucléaire fait Une solution est un mélange d'un solvant, composé majoritaire, et de solutés qui peuvent (titre molaire), x |
|
Préparation dune solution connaissant la densité de la solution m`ere
On souhaite préparer 250 mL de solution d'acide chlorhydrique de concentration d'une solution commerciale de densité d = 1,17 et de titre de pureté τ = 35 |
|
TRAVAUX PRATIQUES DE CHIMIE I - Université Ibn Khaldoun de
Préparation de 100 mL d'une solution de NaOH 0,01 N à partir de la solution mère A titre d'exemple : R1 Explosif à l'état sec, R45 peut causer le cancer |
|
1 • Préparation dune solution diluée de DesTop© • Mesure du pH
Titrage acido-basique avec suivi pH-métrique • Mesure du titre massique en hydroxyde de sodium du DesTop© et évaluation de son incertitude-type |
|
Comment préparer une solution titrée - Lycée dAdultes
On note généralement : ➢ La quantité de matière n en mole de symbole mol ➢ La masse m en gramme de symbole g (unité normalisée kg) ➢ La masse |
|
JOURNAL OFFICIEL DE LA REPUBLIQUE ALGERIENNE NA 63 14
30 oct 2016 · titre de la protection du consommateur et de la répression des fraudes ; Vu l' arrêté 8 2 2 Préparation de la solution mère : Ajouter une partie |
|
Travaux pratiques de chimie I 1 LMD Année 2019-2020 D Benbezza
TP 1 : Préparation de solution de Chlorure de sodium 08 Préparation d'une solution d'acide chlorhydrique TP4: Titrage le titre du TP 2 ème |
|
Chimie
C'est le processus de la réparation régulière des solvates (hydrates) dans tout le Le titre de la solution (Т) – masse de la substance (х), contenue dans un |