dosage acide fort hcl base forte naoh
|
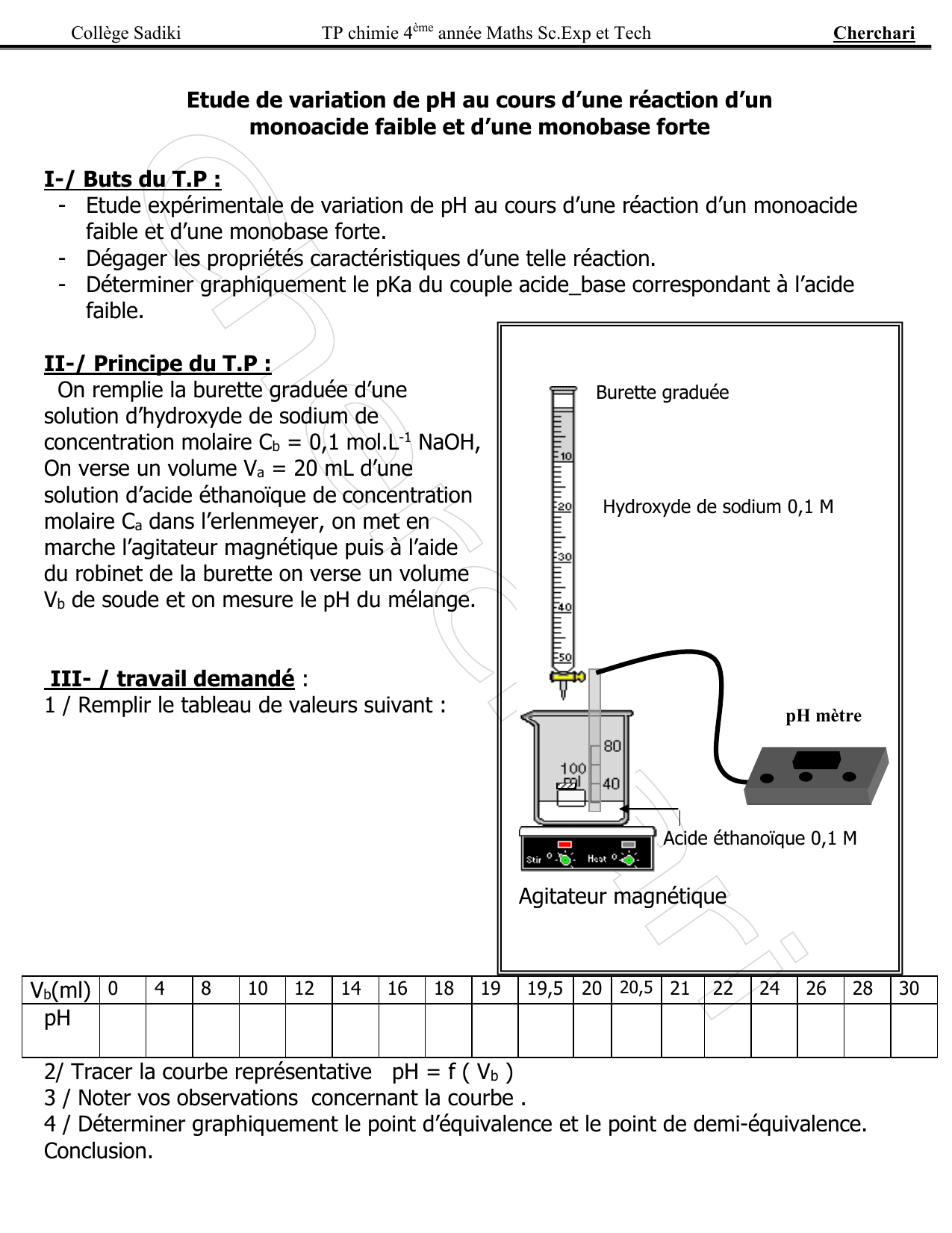
Dosage dune base forte (NaOH) par un acide fort (HCl) 1 Introduction
Le but de ce TP est de vérifier la concentration molaire (inconnue) d'une solution d'hydroxyde de sodium NaOH préparée par dosage acido-basique 4 Mode |
|
TRAVAUX PRATIQUES DE CHIMIE DES SOLUTIONS
Dosage d'un acide faible par une base forte (par exemple acide éthanoïque (acétique) par Na OH) CH3COOH + Na OH ↔ CH3COONa + H2O Le pH du milieu acide faible |
|
Cours-titrage-acide-base-2ème-annnée-pdf
HCl 1M par une solution NaOH 1M a) variation de pH - avant addition de NaOH Puisque HCl est un acide fort et par conséquent un acide totalement dissocié la |
|
§ 7 (suite) Titrages acide-base
Dans le cas particulier du titrage d'une acide fort (HCl par exemple) par une base forte (NaOH par exemple) : – pour 0 < ! < 1 il y a un excès d'acide et |
|
Chapitre 1 Acides et bases
— calculer le pH d'une solution d'acide fort ou de base forte (d'après la concentration apportée) ; — calculer un volume équivalent de dosage pH-métrique; |
|
Dosages acide-base
28 2 Dosage d'un acide fort par une base forte 471 ν1 A1 + ν2 A2 → ν1 A′ 1 28 3 Dosage d'une base forte par un acide fort 473 C'est une réaction totale |
|
Dosages acidobasiques
il y a 7 jours · 1 : Dosage d'un acide fort par une base forte Courbe 1 : ca = cb = 10−3 mol L−1 Va = 20 mL et donc Ve = 20 mL Courbe 2 : ca = cb = 10 |
|
Dosage acide fort
Dosage acide fort – base forte Acide fort HA : titré concentration (à acide fort / base forte (Ca = Cb; Va = 10 mL) Vb (mL) 0 5 10 15 20 pH 0 2 4 |
|
Dosage dune base forte (NaOH) par un acide fort (HCl) 1. Introduction
Le but de ce TP est de vérifier la concentration molaire (inconnue) d'une solution d'hydroxyde de sodium NaOH préparée par dosage acido-basique. 4. Mode |
|
LES TITRAGES ACIDES-BASES
à partir de ce moment le pH est celui de la base forte NaOH. - Après le point d titrage acide fort / base forte. Après le point d'équivalence : il y a un ... |
|
§ 7 (suite) Titrages acide-base
Dans le cas particulier du titrage d'une acide fort (HCl par exemple) par une base forte (NaOH par exemple) : – pour 0 < ! < 1 il y a un excès d'acide et |
|
Les solutions tampons
H. (aq). OH ou. O(l). H. NaCl(aq). HCl(aq). NaOH(aq). 2. 2. -→. -. +. +. -→. -. +. +. -. Page 14. Le titrage acide faible-base forte. • ex.;. • au point d' |
|
Labo théorique : Dosage de lacide chlorhydrique par titrage
Il est important de toujours utiliser pour un titrage acidobasique |
|
Filière Sciences de la Matière Chimie Cours Chimie des Solutions
Calcul du pH de ST. 4. Titrages acide-base. 1.1. Titrage d'un acide fort par une base forte. 1.2. Titrage d'un acide faible par |
|
TP 3 -Titrage dun acide fort et acide faible par une base forte (NaOH)
Le titrage est une technique de dosage utilisée en chimie analytique afin de déterminer la concentration d'une espèce chimique en solution. Généralités. Acides |
|
TP/Methode danalyse électrochimique
Titrages pH-métrique d'un acide fort (HCl) par une base forte (NaOH). 6. Un déterminer la concentration de l'acide chlorhydrique (HCl) par titrage pH-métrique ... |
|
Analyse de laction didactique de sa continuité et de ses
acide fort par une base forte. 3. A : vous allez faire quoi précisément. 4. P1 : c'est un dosage d'un acide fort par une base forte HCl et NaOH avec ... |
|
TP N 03 : Dosage dun acide fort par une base forte
Dans cette partie on souhaite déterminer la concentration inconnue d'une solution d'acide chlorhydrique HCl par de la soude NaOH. |
|
1 TP Nº2 (Semestre 1) : Dosage dune base forte (NaOH) par un
TP Nº2 (Semestre 1) : Dosage d'une base forte (NaOH) par un acide fort (HCl). 1. Introduction : Les réactions acido-basiques résultent du transfert d'un |
|
TP 3 -Titrage dun acide fort et acide faible par une base forte (NaOH)
forte (NaOH) Le titrage est une technique de dosage utilisée en chimie analytique afin de ... Titrage d'un acide fort HCl par une base forte NaOH. |
|
THÈSE
faible par une base forte » « Dosage d'une base faible par un acide fort » avec la Figure 122 : évolution du pH au cours de titrage de HCl par NaOH . |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
Titrage d'un acide faible par une base forte. un gaz (CO2 dans les boissons gazeuses O2 |
|
Filière Sciences de la Matière Chimie Cours Chimie des Solutions
Titrage d'un acide faible par une base forte. un gaz (CO2 dans les boissons gazeuses O2 |
|
Dosage acide faible – base forte
Acide faible HA : constante d'acidité Ka titré concentration (à déterminer) ca volume va. ?. +. ?. ?. +. +. A. OH. OH. HA. 3. 2. Base forte NaOH. |
|
§ 7 (suite) Titrages acide-base
Dans le cas particulier du titrage d'une acide fort (HCl par exemple) par une base forte (NaOH par exemple) : – pour 0 < ! < 1 il y a un excès d'acide et |
|
TP 5 Détermination de la chaleur molaire dune réaction de
La chaleur molaire d'un dosage acide/base est la quantité de chaleur dégagée pour une mole d'acide réagie d'un acide fort (HCl) par une base forte (NaOH). |
|
TP N 03 : Dosage dun acide fort par une base forte
Dans cette partie on souhaite déterminer la concentration inconnue d'une solution d'acide chlorhydrique HCl par de la soude NaOH. |
|
Chapitre 1 Acides et bases
La base conjuguée d'un acide fort est dite “indifférente dans l'eau” de sodium (NaOH |
|
Dosage pH-métrique dun acide fort par une base forte
faible par une base forte » « Dosage d'une base faible par un acide fort » avec la Figure 122 : évolution du pH au cours de titrage de HCl par NaOH |
|
Informatique Titrage acide/base - Cours dinformatique
17 avr 2013 · Dans le cas du titrage d'un acide fort par une base forte, La réaction chimique entre NaOH et HCl peut être notée, en indiquant les ions qui |
|
1) Principes et objectifs 2) Mode opératoire 3) Titrage dun acide fort
3) Titrage d'un acide fort par une base forte On titre une solution d'acide chlorhydrique HCl dans le bécher, par de la soude NaOH à 0 1 mol L-1 |
|
TP 3: Acides et Bases
5 oct 2007 · Préparation d'1L d'hydroxyde de sodium NaOH environ 0 1M par pur ou complété par du HCl ou du NaOH (acide et base forts) à des voir que leur odeur plus ou moins détectable et forte ne dépendait pas de leur pH |
|
TP 3 -Titrage dun acide fort et acide faible par une base forte (NaOH)
Le titrage est une technique de dosage utilisée en chimie analytique afin de déterminer la concentration Titrage d'un acide fort HCl par une base forte NaOH |
|
TRAVAUX PRATIQUES DE CHIMIE DES SOLUTIONS
TP N°1 : DOSAGE ACIDE FORT - BASE FORTE PAR PH-METRIE ET Une solution de base forte de concentration connue (NaOH à 0,1 mol L – 1 ) En utilisant la pipette et la propipette, prélever vb = 10 mL d'HCl de concentration |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
Titrage d'un acide faible par une base forte CHAPITRE III Composé HCl H2SO4 H3PO4 NaOH nombre d'équivalent P P=1 P=2 P=3 P=1 1 5 + Au point équivalent du dosage acide faible - base forte, le milieu est basique |
|
Le pH 5 Le dosage des solutions dacides et des bases forts
Le but du dosage d'une solution d'acide fort par une solution de base forte est 50 ml HCl NaOH 0 1 M 4 2 Etude de la courbe du dosage Sur une courbe de |
|
Le pH 6 Le dosage des solutions dacides et des bases faibles
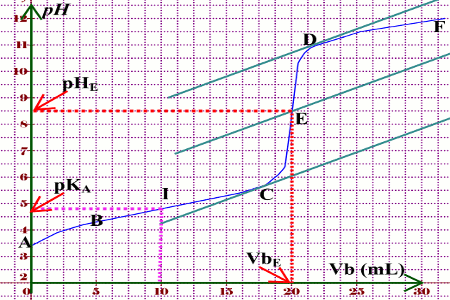
Concentration initiale d'acide fort (utilisée pour doser la base faible) CA Concentration 3 2 Cas du dosage de l'acide acétique par NaOH Pour être acide 0 1 2 3 4 5 6 7 8 9 10 11 12 0 5 10 15 20 25 30 ml HCl pH pH = pKa |
|
Dosage acide faible – base forte
→ OH Na NaOH L'équation bilan de la réaction de dosage s'écrit : OH A OH HA |