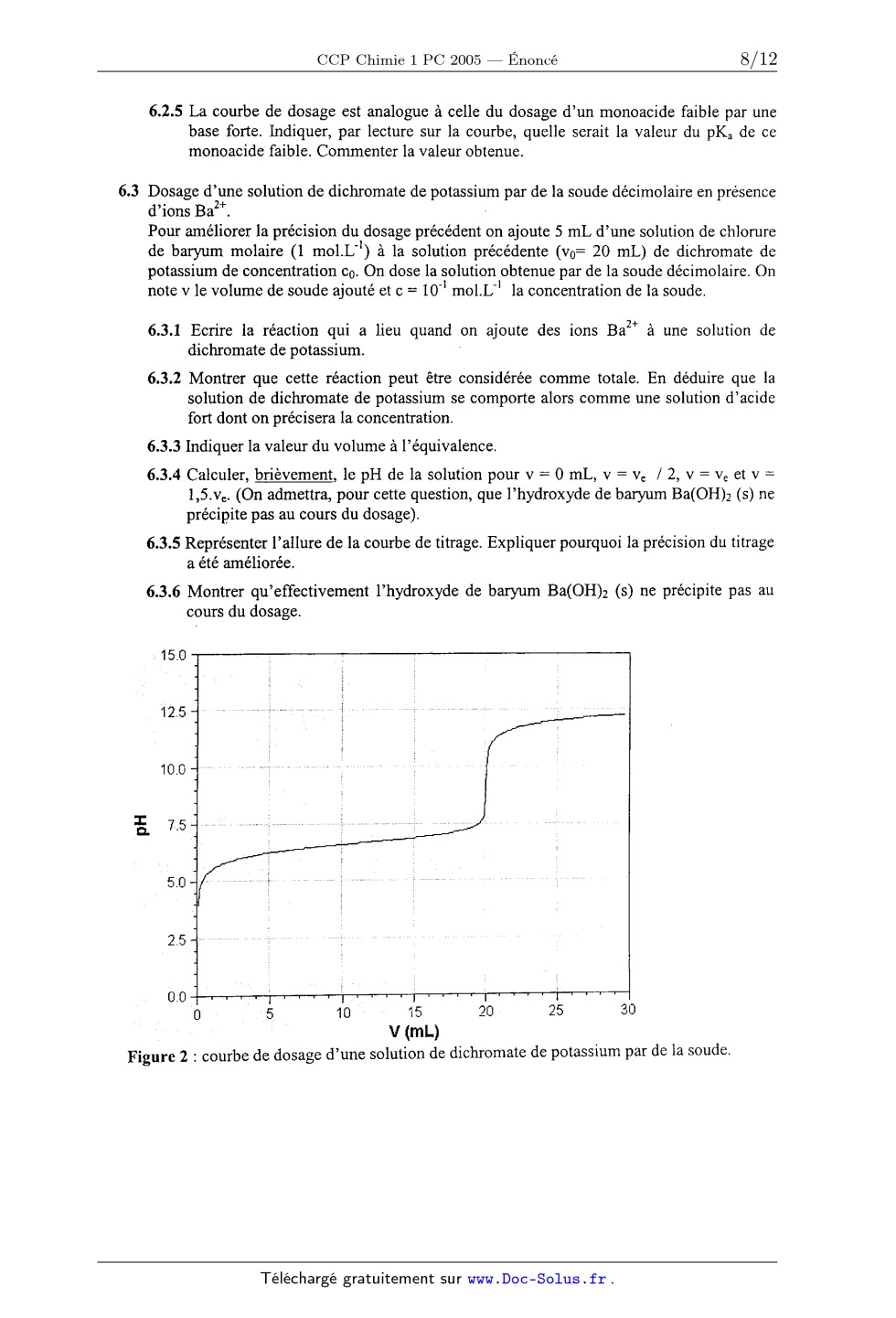
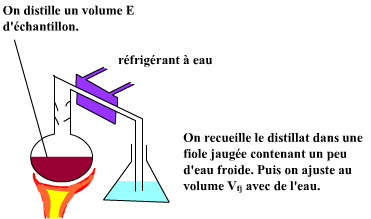
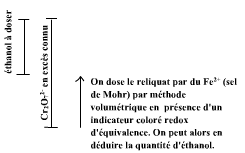
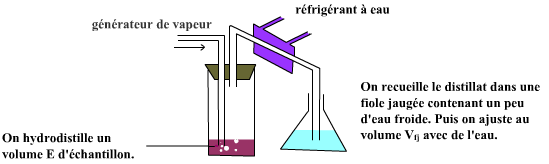
dosage fe2+ par cr2o72-
|
Correction dcopdf
Dosage de l'excès par le Sel de Mohr : Fe2 + On peut écrire pour la totalité des ions dichromate : nT = nMO + nOX D'après la relation de la question 1 4 |
|
éléments de correction 1 Question préparatoire : Fer et dichromate
de la courbe de dosage En effet à l'équivalence les ions Fer II et dichromate ont été introduits en quantités stœchiométriques : n0(Fe2+) 6 = nE(Cr2O7 2 |
|
Transformations chimiques en solution aqueuse
Cela permet de calculer la constante d'équilibre K° de la réaction d'oxydo-réduction Exemple 1 : Oxydation des ions Fe2+ par les ions dichromate Cr2O72- |
|
Exercice V-5 : Dosage du fer (II) par le dichromate Enoncé
plongeant dans la solution lors du dosage Exprimer E = f(V') où V' est le E° (Fe3+ / Fe2+) = 077 V; • E° (Cr2O72- / Cr3+) = 133 V Page 2 Page 2 |
|
Dosage dune solution de sel de Mohr (Fe
- Déterminer la concentration C1 en Fe2+ de la solution de sel de Mohr 3 Dosage de Fe 2+ -- par Cr2O7 2- |
|
Différents types de dosages
L'excès d'ions dichromate est dosé par des ions Fe2+ (5) 1136 BULLETIN DE L Cr2O72 – réagit avec l'éthanol l'excès n2 Cr2O7 2 – est dosé par les ions |
|
Ex 5 Titrage des ions ferreux
On souhaite effectuer le dosage du chlorure de fer (II) par le dichromate de potassium 4(Fe2+/Fe) = −044 V Partie n◦1: Réaction de titrage 1 Quels |
|
TP de potentiométrie : éléments de correction 1 Question
vos graphes de dosage). En effet à l'équivalence |
|
Différents types de dosages Détermination de la concentration dun
L'excès d'ions dichromate est dosé par des ions Fe2+. (5). 1136. BULLETIN DE L Cr2O72 – réagit avec l'éthanol l'excès n2 Cr2O7. 2 – est dosé par les ions. |
|
Exercice V-5 : Dosage du fer (II) par le dichromate Enoncé
plongeant dans la solution lors du dosage. Exprimer E = f(V') où V' est le E° (Fe3+ / Fe2+) = 0 |
|
Méthode : cas du couple Cr2O72-/Cr3 Applications Corrections
Méthode : cas du couple Cr2O72-/Cr3. Etape 1 : Ecrire l'oxydant gauche et le Fe2+ + 2e– = Fe. S4O6. 2–+2e–. = 2S2O3. 2–. I2 + 2e– = 2I–. MnO4. – + 8H+ + 5e ... |
|
Étude dune réaction : titrage des ions fer II par les ions permanganate
dosages. Exemple : Solution de permanganate de potassium. K+(aq) + MnO4. -(aq) ... néq(Fe2+) = ni(Fe2+) – 5 xéq= 0 xéq = ni(Fe2+) / 5 néq(MnO4. -) = nv(MnO4. |
|
Dosage dune solution de sel de Mohr (Fe ) 1. Principe 1
- Déterminer la concentration C1 en Fe2+ de la solution de sel de Mohr. 3. Dosage de Fe. 2+ -- par Cr2O7. 2-. |
|
DETERMINATION DE LA DEMANDE CHIMIQUE EN OXYGENE
on réalise le dosage de 10 mL d'un blanc c'est-à-dire d'un volume On prend la concentration C2 = [Fe2+] trouvée dans la partie B/. Avec C2 = 0 |
|
Dosages du phosphore et de lazote dans un engrais NPK
- Dosage des ions Fe2+. (aq) en excès et résultat final : o Refroidir le masse d'azote (m) contenue dans la solution préparée : n(Cr2O72-) = V3C3 d'où n ... |
|
Oxydoréduction Oxydoréduction
dosage en retour. Dans un bécher on verse V1 = 4 |
|
Untitled
R: Il faut acidifier le milieu (cf équation de la réaction). VIII - Dosage des ions Fe2+ ions Cr2O72- sur les ions Sn²+. R: Cr₂O² + 3 Sn²+ + 14 H+ →. 2 Cr3+ ... |
|
TP de potentiométrie : éléments de correction 1 Question
Fe2+ = Fe3+ + e–. Cr2O7. 2– +6e– + 14 H+ = 2 Cr3+ +7H2O. Et l'équation-bilan de la réaction support du dosage potentiométrique s'écrit : 6 Fe2+ + Cr2O7. |
|
Exercice V-5 : Dosage du fer (II) par le dichromate Enoncé
E° (Fe3+ / Fe2+) = 077 V;. • E° (Cr2O72- / Cr3+) = 1 |
|
Compte rendu du TP de chimie n°9 Les dosages rédox
Vu le résultat du test nous en concluons que la solution inconnue contient des ions fer(II) Fe2+. (aq). Nous allons donc maintenant doser ces ions. |
|
Méthode : cas du couple Cr2O72-/Cr3 Applications Corrections
Méthode : cas du couple Cr2O72-/Cr3. Etape 1 : Ecrire l'oxydant gauche et le réducteur à droite. Cr2O7. 2-= Cr3+ Fe2+/Fe. S4O6. 2–/S2O3. 2–. I2/I–. MnO4. |
|
Exercice 1 : 1. Lion dichromate Cr2O7 2 - de couleur jaune-orangé
c) Choisir alors le couple qui va intervenir entre Fe2+/Fe et Fe3+/Fe2+. L'équation de réaction de dosage est la suivante :. |
|
Untitled
A - Dosage des ions nitrates dans un engrais solide (protocole et manipulation) R: Fe2+. Acide sulfurique. Eau. Faire un schéma avec une légende du. |
|
CORRIGÉ
A l'équilibre il y a unicité des potentiels : E Cr2O72– / Cr3+ = E SO42- / HSO3-. D'où : log K° = 6 x (E° Cr2O72– / Cr3+ - E° SO42- / HSO3-) / 0 |
|
PCSI jeudi 22 juin 2017 CHIMIE Filière PC & PSI DEVOIR
aqueux acide les ions Fe2+ en ions Fe3+ ; C'est un dosage des ions fer(II) dans un produit phytosanitaire qui est proposé ici. |
|
Les dosages doxydoréduction
Une solution de dichromate de potassium de concentration molaire c2 = 0100 mol.L–1 permet d'effectuer le titrage des ions Fe2+ restants. Données : M(N) = 14 |
|
Fer et dichromate
Fe2+ = Fe3+ + e– Cr2O7 2– +6e– + 14 H+ = 2 Cr3+ +7H2O Et l'équation-bilan de la réaction support du dosage potentiométrique s'écrit : 6 Fe2+ + Cr2O7 |
|
Exercice V-5 : Dosage du fer (II) par le dichromate Enoncé - Free
1) Ecrire l'équation-bilan de la réaction de dosage Calculer sa constante E° ( Fe3+ / Fe2+) = 0,77 V; • E° (Cr2O72- / Cr3+) = 1,33 V Fe2 + éq car il faut 6 fois plus d'ions Fe 2+ que d'ions Cr2O 7 2− ; donc Fe 2+ [ ]= 0,144 mol⋅L −1 |
|
Méthode : cas du couple Cr2O72-/Cr3 Applications Corrections
Méthode : cas du couple Cr2O72-/Cr3 Etape 1 : Ecrire Ecrire les demi- équations relatives aux couples Redox suivants : Cu2+/Cu Fe2+/Fe S4O6 2–/ S2O3 |
|
Compte rendu du TP de chimie n°9 Les dosages rédox - MMorin
II) Dosages des ions Fe2+ (aq) contenus la solution : L'ion Fe2+ (aq) a des propriétés d'oxydoréduction et c'est le réducteur du couple Fe3+/Fe2+ Il peut donc |
|
DETERMINATION DE LA DEMANDE CHIMIQUE EN - Eklablog
Dosage de l'excès par le Sel de Mohr : Fe2 + On peut écrire, pour la totalité des ions dichromate : nT = nMO + nOX D'après la relation de la question 1 4 et |
|
Dosage dune solution de sel de Mohr (Fe ) 1 Principe 1
- Déterminer la concentration C1 en Fe2+ de la solution de sel de Mohr 3 Dosage de Fe 2+ -- par Cr2O7 2- |
|
PCSI jeudi 22 juin 2017 CHIMIE Filière PC & PSI - Chimie en PCSI
Il permet, par exemple, d'oxyder, en milieu aqueux acide, les ions Fe2+ en ions Fe3+ ; C'est un dosage des ions fer(II) dans un produit phytosanitaire qui est |
|
Titrage des ions fer II par les ions permanganate
également une pissette d'eau distillée pour rincer le bécher entre les deux dosages violet, et les ions fer II Fe2+ réagissent ensemble pour donner des ions |
|
Semestre 2 – Chapitre 5 : Loxydoréduction Loxydoréduction, qui s
3) Réaction de médiamutation : Fe3+/Fe2+ et Fe2+/Fe Un bécher est rempli par la solution contenant des ions fer (II) Fe2+ à doser (de concentration c0 |
|
Titrage doxydo-réduction par potentiométrie
Les dosages redox après l'équivalence dans le cas du dosage ß par une solution Exemple du dosage d'une solution contenant des ions Fe2+ par une |