Configuration électronique
Comment faire une configuration électronique ?
C'est assez simple.
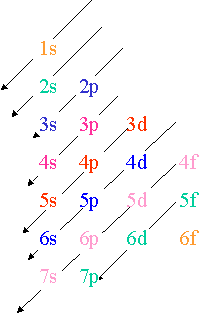
Nous écrivons les noms des sous-couches sur une ligne et utilisons des nombres en exposant pour indiquer le nombre d'électrons qu'elles contiennent.
Dans ce cas, chacune des trois sous-couches mentionnées ne possède que deux électrons : 1 s 2 2 s 2 2 p 2 .Quel atome à pour configuration électronique 1s 2 2s 2 2p 4 ?
Le lithium, avec trois électrons, présente, à l'état fondamental, la configuration 1s2 2s1, tandis que l'oxygène, avec huit électrons, présente, à l'état fondamental, la configuration 1s2 2s2 2p4, et que l'aluminium, avec treize électrons, présente, à l'état fondamental, la configuration 1s2 2s2 2p6 3s2 3p1.
Quels sont les configurations électronique ?
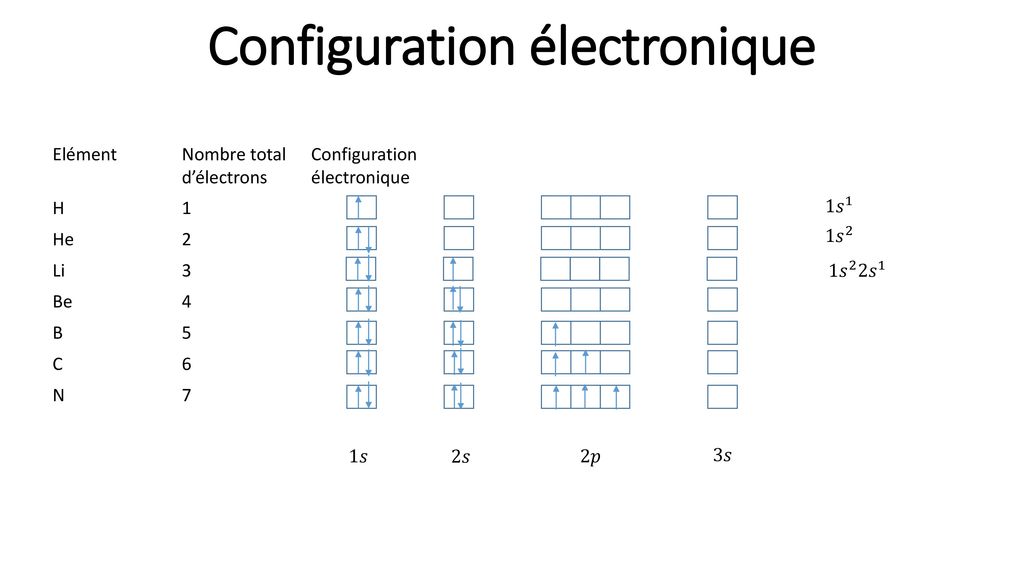
Configuration électronique des éléments chimiques
H Hydrogène : 1s1 1s1 He Hélium : 1s2 1s2 Li Lithium : 1s2 2s1 1s2 2s1 Be Béryllium : 1s2 2s2 1s2 2s2 B Bore : 1s2 2s2 2p1 1s2 2s2 2p1 C Carbone : 1s2 2s2 2p2 1s2 2s2 2p2 N Azote : 1s2 2s2 2p3 1s2 2s2 2p3 O Oxygène : 1s2 2s2 2p4 1s2 2s2 2p4La configuration électronique d'un atome dans son état fondamental indique la répartition des électrons dans les couches et les sous-couches.
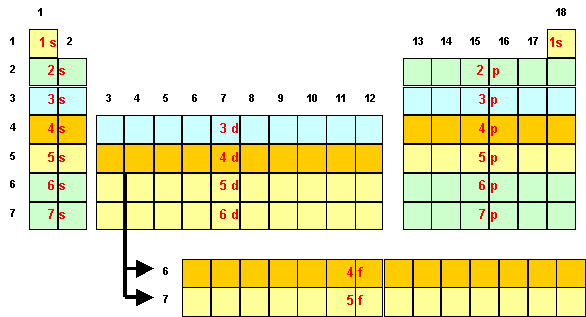
Le numéro de la dernière couche qui contient des électrons indique le numéro de la ligne, appelée période, dans laquelle se trouve d'atome.
|
Règles de remplissage pour les atomes polyélectroniques
On peut alors abréger la notation en indiquant que la configuration des électrons de cœur (électrons d'une couche électronique totalement remplie à l'exception |
|
Chapitre 3 :Structure électronique des atomes
10. −. ∈ n l. : nombre quantique azimutal ou numéro de sous-couche. L'énergie de l'électron dépend (un peu) de l ( ) |
|
Orbitales moléculaires des diatomiques 1 Série 1
Rappelons la configuration électronique des deux esp`eces Be2 et C2 et leur ordre de liaison n: esp`ece configuration nliant nantiliant n. Be2. (1σg)2(1σu)2 |
|
Chapitre 1 - Configuration électronique
Remarque : n nombre quantique principal |
|
Orbitales moléculaires des diatomiques 1 Série 1
Rappelons la configuration électronique des deux esp`eces Be2 et C2 et leur ordre de liaison n: esp`ece configuration nliant nantiliant n. Be2. (1σg)2(1σu)2 |
|
Chapitre 1 - Configuration électronique
Remarque : n nombre quantique principal |
|
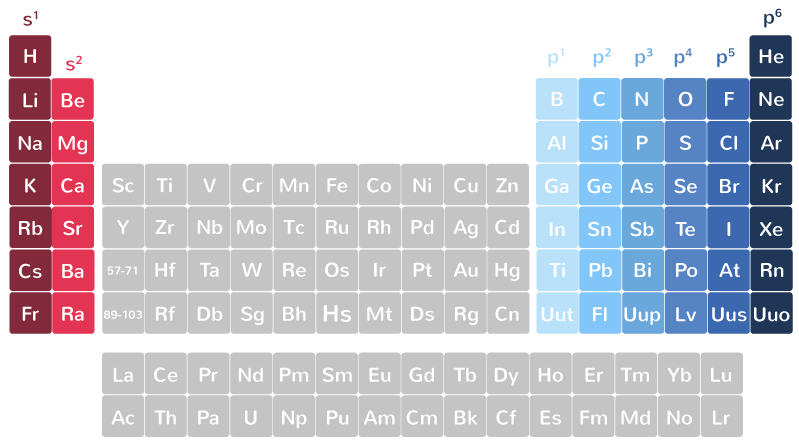
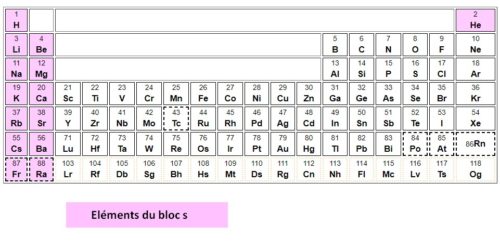
Wikipedia : tableau périodique des éléments
Sous-couche 2p 3 cases quantiques → 6 électrons → 8 éléments sur la 2e période Configuration électronique n° 1. H. Hydrogène. Non-métal. 1s1 n° 2. He. |
|
Lélément Cobalt
II L'atome de cobalt. II-1) Ecrire la configuration électronique d'un atome de cobalt dans son état fondamental. A quel bloc d'éléments appartient-il? |
|
Corrigé
Ecrire la configuration électronique de ces deux ions. Ti a pour numéro atomique Z = 22 et pour configuration externe 4s2 3d2. On peut facilement imaginer |
|
Ch.ci.1:structure de latome et configurations electroniques
Pour obtenir la configuration électronique d'un ion dans son état fondamental il faut d'abord écrire celle de l'atome dont il est issu puis enlever ou |
|
Règles de remplissage pour les atomes polyélectroniques
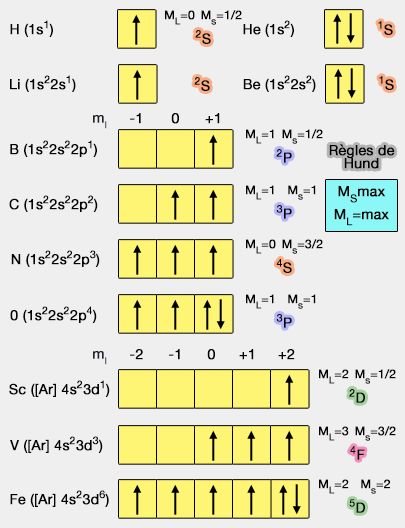
Règle de Hund : pour une sous-couche donnée la configuration électronique de plus basse énergie est obtenue en plaçant un maximum d'électrons de même spin |
|
CORRIGÉ
21 déc. 2017 Dessiner un schéma de Lewis d'une de ces entités. 7 électrons de valence : il leur en manque 1 pour acquérir la configuration électronique du ... |
|
Orbitales moléculaires des diatomiques 1 Série 1
a un ordre de liaison de 2. 2. ´Ecrivons la configuration électronique des quatre esp`eces H+. 2 H2 |
|
Ch.ci.1:structure de latome et configurations electroniques
Pour obtenir la configuration électronique d'un ion dans son état fondamental il faut d'abord écrire celle de l'atome dont. |
|
Chapitre 3 :Structure électronique des atomes
10. ?. ? n l. : nombre quantique azimutal ou numéro de sous-couche. L'énergie de l'électron dépend (un peu) de l ( ) |
|
Corrigé
atomiques pour obtenir la configuration électronique d'un atome. En déduire la configuration électronique du titane. Il faut citer la règle de Klechkowski :. |
|
Lélément Cobalt
II L'atome de cobalt. II-1) Ecrire la configuration électronique d'un atome de cobalt dans son état fondamental. A quel bloc d'éléments appartient-il? |
|
Wikipedia : tableau périodique des éléments
wikipedia : tableau périodique des éléments. Élément chimique. Série chimique. Configuration électronique n° 1. H. Hydrogène. Non-métal. |
|
Chimie - Chapitre 2 : La classification périodique Ce quil faut retenir…
électroniques donné par la règle de Klechkowski : une nouvelle ligne commence chaque fois que la configuration électronique de l'élément. |
|
Règles de remplissage pour les atomes polyélectroniques
Règle de Hund : pour une sous-couche donnée, la configuration électronique de plus basse énergie est obtenue en plaçant un maximum d'électrons de même |
|
Chapitre 3 :Structure électronique des atomes
Chapitre 3 : Structure électronique des atomes Structure de la matière Page 1 sur 5 I Nombres quantiques A) Origine théorique La résolution de l'équation de |
|
CONFIGURATION ÉLECTRONIQUE DES ÉLÉMENTS LA
Principes guidant le remplissage des orbitales électroniques Les principes La configuration électronique d'un Si la configuration de gauche était la bonne, |
|
Corrigé
configuration électronique du titane Il faut citer la règle de Klechkowski : « L' énergie des orbitales atomiques est une fonction croissante de la somme (n+l) A |
|
Configuration électronique et représentation de Lewis - Aix - Marseille
Une couche n peut avoir n sous-couches L'état fondamental d'un atome est celui pour lequel son cortège électronique est de plus bas niveau d'énergie La |
|
LA LIAISON CHIMIQUE 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f
liaisons ioniques comme avec les liaisons covalentes, les atomes ont tendance à acquérir une configuration électronique stable Configuration électronique Il faut |
|
Thème 12 La structure électronique des atomes - DSFM
La configuration électronique • chaque orbitale atomique a trois nombres quantiques: n, l, m • chaque électron a quatre nombres quantiques: n, l, m, s |




































![serie 5 chimie1 15 16[1] par Outhmane - Fichier PDF serie 5 chimie1 15 16[1] par Outhmane - Fichier PDF](https://www.lachimie.net/energie.gif)
