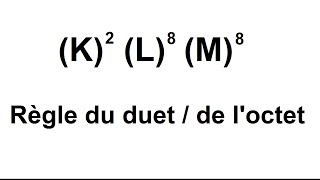Regle d'octet et duet !
|
TD Chapitre 3 : Règles du « duet » et de l’octet / Applications
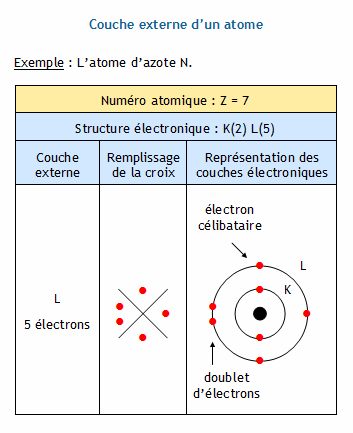
Pour respecter la règle de l’octet il peut gagner 4 électrons en construisant 4 liaisons électroniques avec d’autres atomes Atome d’oxygène O (Z=8) : structure électronique : (K)2(L)6 il a besoin de gagner deux électrons supplémentaires pour respecter la règle de l’octet |
|
I
la règle de l’« octet » Les éléments de numéro atomique (Z≤5) proche de celui de l’hélium adoptent la structure électronique (K)2 Ils ont alors deux électrons sur leur couche externe par formation de molécules (5 |
|
1 Règles de Duet et de lOctet
- La règle de l’«Octet» : Au cours des transformations chimiques les éléments chimiques de numéro atomique (4 < Z ≤18) évoluent de manière à avoir la structure électronique de plus proche gaz rare dans le tableau périodique des éléments (de Néon Ne∶ (K)2(L)8 ou Argon Ar ∶ (K)2(L)8(M) 8 |
|
Règle de loctet
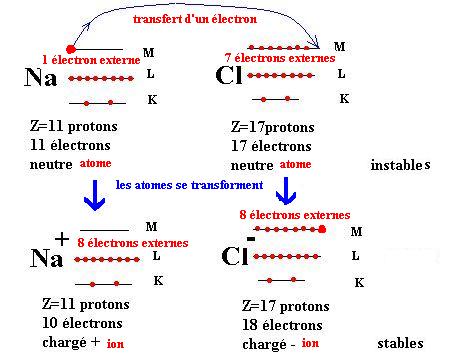
Formation des ions et des molécules Au cours d’une transformation chimique les atomes cherchent à obtenir la structure électronique du gaz rare le plus proche Pour cela ils vont : Perdre ou gagner un ou plusieurs électrons périphériques Perd des électrons Gagne des électrons Ion positif Ion négatif = cation = anion |
Quelle est la règle de l’octet ?
- La règle de l’«Octet» : Au cours des transformations chimiques, les éléments chimiques de numéro atomique (4 < Z ≤18) évoluent de manière à avoir la structure électronique de plus proche gaz rare dans le tableau périodique des éléments (de Néon Ne∶ (K)2(L)8 ou Argon Ar ∶ (K)2(L)8(M)8). Ils portent donc 8 électrons sur leur couche externe. 3.
Quelle est la règle du duet ?
- La règle du «Duet» : Au cours des transformations chimiques, les éléments chimiques de numéro atomique (Z ≤ 4) évoluent de manière à avoir la structure électronique du Hélium He∶ (K)2. Ils ont alors deux électrons sur leur couche externe.
Quels sont les règles de Duet et de l'octet ?
Règles de Duet et de l'Octet : 1. Stabilité des gaz rares : 1. Ecrire la structure électronique des éléments suivantes : L'hélium He (Z=2), le néon Ne (Z=10) et l'argon Ar (Z=18) La structure électronique est : ∶ ( )2 , ∶ ( )2( ) , ∶ ( ) ( ) ( ) . 2. La couche externe de chaque atome est-elle saturée ou non ?
Quelle est la différence entre le Duet et l’octet ?
Règle du duet : un atome ou un ion est stable si la 1ère couche correspond à la couche externe et comporte deux électrons. Règle de l’octet : un atome ou un ion est stable si la 2ème ou 3ème couche correspond à la couche externe et comporte huit électrons. Bon c’est bien joli ces règles mais comment on les applique ??

Règles du DUET et OCTET (Stabilité LEWIS) Seconde Physique-Chimie

Règle de lOctet / Règle du Duet ( Liaison Chimique )

Règles du duet et de loctet
|
Exceptions à la règle de loctet
Example: formation d'une liaison entre: Un acide de Lewis: susceptible d'accepter un doublet électronique car contient des orbitales p ou d (métaux de |
|
Schéma de Lewis
Règle du Duet. L'atome d'hydrogène possède 1 électron de valence et cherche à Il s'agit de la règle de l'octet réduit. Il manque donc 2 électrons de. |
|
Activité : Les règles du « Duet » et de l« Octet » I. Les Gaz Rares
b) En appliquant la règle de « l'Octet » à l'atome d'Aluminium prévoir quel ion stable va être formé ? ? 14°) L'atome de Fluor (F) a pour numéro atomique Z=9. |
|
Rappels seconde molecules
II) Règles du duet et de l'octet : Dans toutes les entités chimiques qu'ils forment (ions molécules) |
|
LES MOLECULES: REPRESENTATION CORRECTION
b) Règle de l'octet: les atomes cherchent à acquérir la structure électronique externe en octet des gaz rares. Règle du duet: les atomes de numéro atomique |
|
Sans titre
Règles du duet et de l'octet. Atome. Numéro atomique Z ils vérifient la règle de l'octet. ... Quelle règle respecte-t-il dans une molécule ? |
|
1. Les règles du duet et de loctet
Ils acquièrent un "duet" d'électrons c'est-à-dire une paire d'électrons. C. Règle de l'octet. ? Au cours de leurs transformations chimiques |
|
1 Théorie de Lewis
Exception : H ne s'entoure que de 2 électrons : règle du duet. Dans la règle de l'octet on compte les électrons en attribuant à un. |
|
Règle de loctet
A retenir : la règle de l'octet et du duet. Au cours d'une transformation chimique les atomes cherchent à obtenir la structure électronique du gaz rare le |
|
Chapitre 3 : Lélément chimique
Règle du « duet » et règle de l'octet. Lorsque les atomes subissent des transformations (transformation en ion monoatomique ou lorsque qu'ils. |
Quel est la règle de l'octet et du duet ?
Quelle est la règle du duet ?
Quel est la règle de l'octet ?
. Pour obtenir une configuration électronique stable, un atome cherchera à gagner ou à perdre un ou des électrons par ionisation.
Quel atome respect la règle du duet ?
. Seuls les premiers éléments de la classification périodique sont concernés par cette loi notamment l'hydrogène, l'hélium ou le lithium.
|
Règle de loctet
A retenir : la règle de l'octet et du duet Au cours d'une transformation chimique, les atomes cherchent à obtenir la structure électronique du gaz rare le plus |
|
Règle du duet et de loctet
Règle du duet et de l'octet I) Couches externes et couches internes Considérons deux éléments d'une même famille, par exemple le fluor et le chlore En vous |
|
Structure électronique dun atome Règles du duet et de loctet
Règles du duet et de l'octet I – Établir la structure électronique d'un atome Ou comment les électrons se placent-ils autour du noyau ? 1) Sur des couches |
|
Exceptions à la règle de loctet - EPFL
Example: formation d'une liaison entre: Un acide de Lewis: susceptible d' accepter un doublet électronique car contient des orbitales p ou d (métaux de |
|
1 Les règles du duet et de loctet - Canal Blog
b Atomes chimiquement stables ⇨ Les atomes dont la couche externe est déjà saturée (gaz rares ou nobles) ne donneront donc pas d'ion monoatomique et |
|
Activité : Les règles du « Duet » et de l« Octet » I Les Gaz Rares
Activité : Les règles du « Duet » et de l'« Octet » Chapitre Chimie N°5 : L'élément chimique Objectif du TP : ➢ Découvrir les règles de stabilités des atomes de |
|
Compétence C3 Japplique les règles du duet et de loctet pour
J'applique les règles du duet et de l'octet pour rendre compte des charges des ions monoatomiques usuels Exercice 1 On donne la structure électronique d'un |
|
2ème application des règles du duet et de loctet : formation des
1) Déterminer pour chaque atome le nombre d'électrons sur la couche externe, en déduire le nombre de liaisons covalentes à constituer 2) Déterminer |
|
Duet et octet - Ze Cancres
2 sept 2004 · 2 2 Règle de L'OCTET ET DU DUET • Au cours d'une réaction chimique les atomes ont tendance à adopter une structure électronique avec |