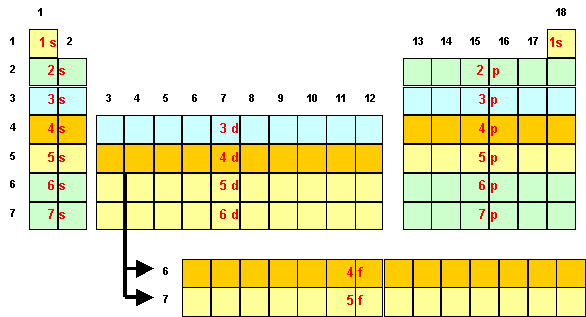
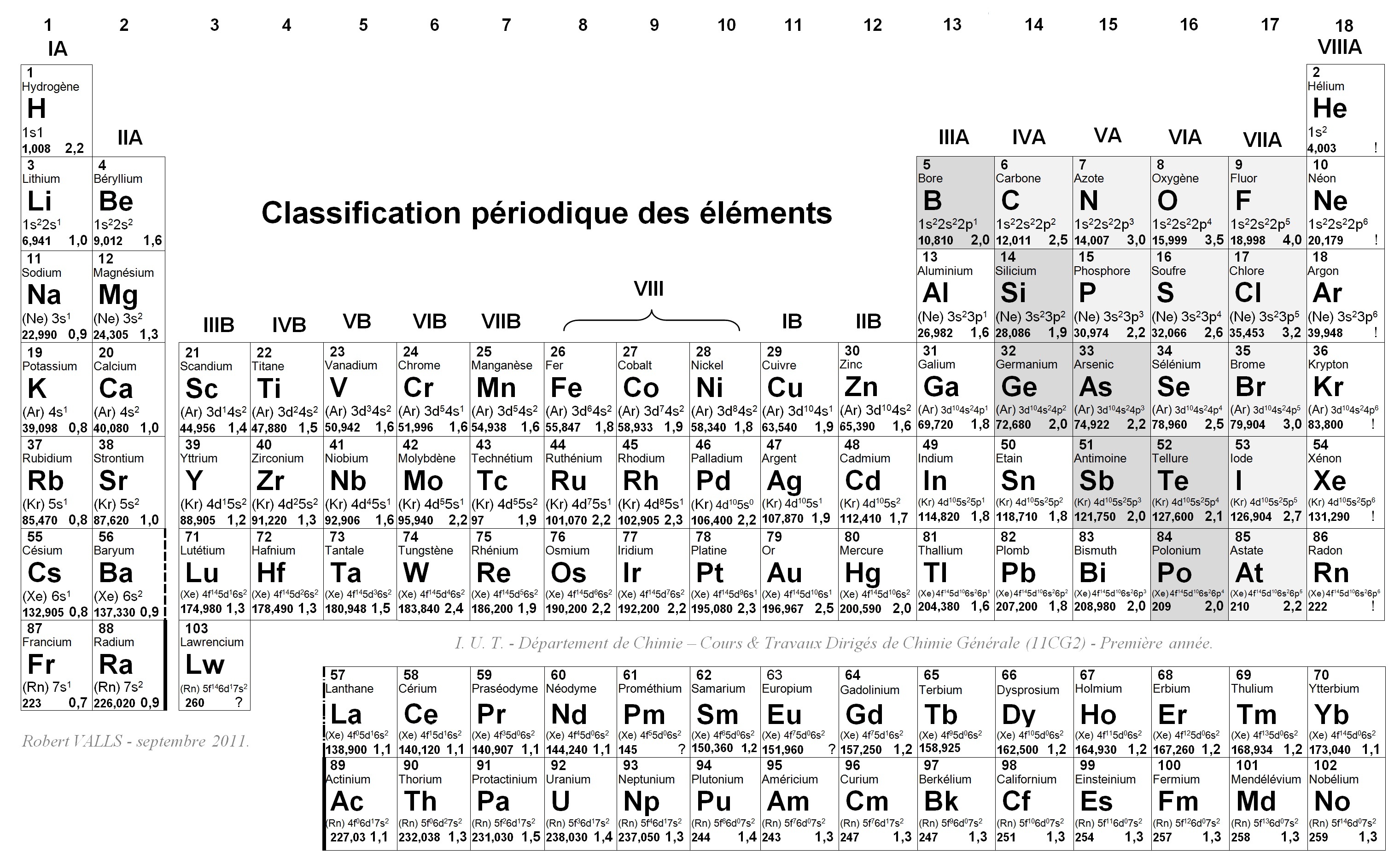
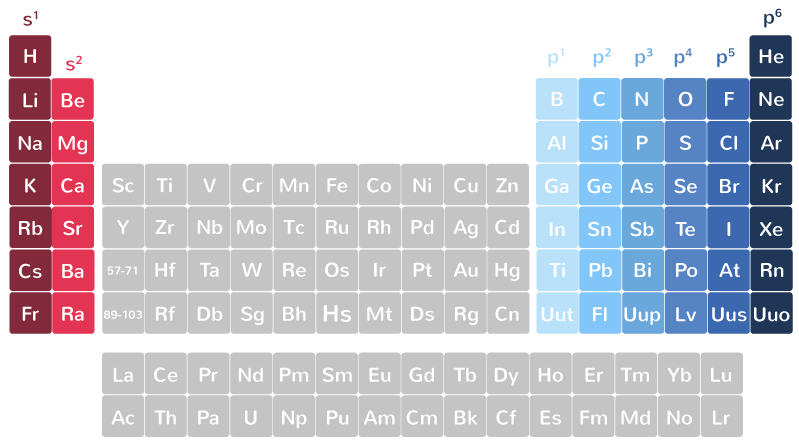
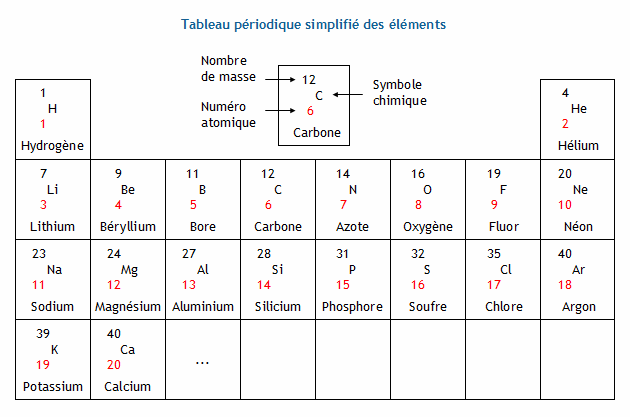
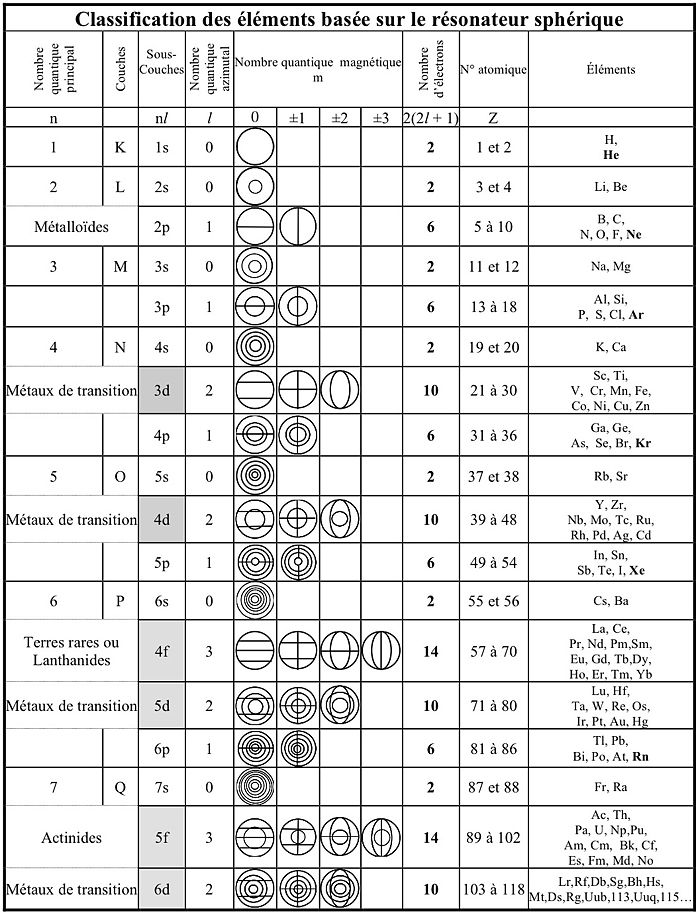
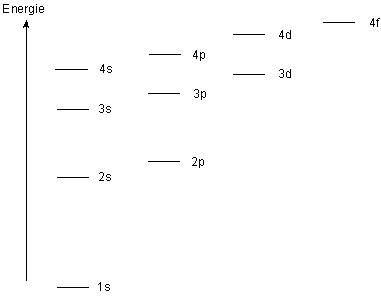structure electronique fer
|
Proposition de corrige – e preuve de chimie 2019
B - Étude de complexes du fer avec les ions cyanure 21 Page 5 5 [Fe(CN)6]4- est l'ion hexacyanoferrate(II) B 1 Structure électronique du complexe [Fe(CN)6] |
|
Chapitre III : Structure électronique des atomes
La configuration électronique définit l'énergie de l'atome à N électrons (dans l'approximation de champ moyen central) : cette énergie est donnée par la somme |
|
Chapitre 1: Structure de latome ; Constituants de la matière
5 Structure électronique des atomes poly-électronique (configuration électronique) - Triade du Fer : (Fe Co Ni) - Triade du palladium : (Ru Rh Pd) |
|
Structure électronique de latome
Ainsi l'atome de fer (Fe) est un atome paramagnétique (il possède un électron célibataire) tandis que l'atome d'hélium (He) ou encore l'atome de zinc (Zn) sont |
|
Structure électronique des atomes et classification périodique des
Structure électronique des atomes et classification périodique des éléments I 56Fe et les ions Fe2+ et Fe3+ correspondent tous à l'élément fer En effet |
|
Structure électronique des atomes
9 oct 2017 · On y ajoute quelques grains de limaille de fer solide Faire un bécher témoin Schémas de la transformation avec état initial et état final |
Le principe de Pauli stipule que deux électrons doivent différer par au moins un de leurs nombres quantiques.
Elle s'applique donc à toutes les particules de spin demi-entier, appelées fermions.
En plus des électrons, cela inclut également les protons et les neutrons.
Comment faire la structure électronique ?
Comment écrire la structure électronique d'un atome ? ✍�� Il faut dans un premier temps connaître le nombre total d'électrons que possède cet atome ce qui est indiqué par son numéro atomique Z.
Ensuite, il suffit d'écrire la première couche et d'y placer les 2 premiers électrons.
Quelle est la configuration électronique du fer ?
[Ar] 3d⁶ 4s²La configuration électronique de l'atome de fer est donc (puisque le gaz noble qui le précède est l'argon) : [Ar] 4s2 3d6 avec [Ar] : 1s2 2s2 2p6 3s2 3p6.
|
Calcul en LMTO-ASA de la structure électronique dimpuretés `` s-p
???/???/???? dans le fer ferromagnétique. C. Koenig P. Léonard et E. Daniel. Laboratoire de Magnétisme et de Structure Electronique des Solides (*) ... |
|
Ch.ci.1:structure de latome et configurations electroniques
25) et des ions Fer (+II) Fe2+ et Fer (+III) Fe3+ (Fe Z = 26). Ion Mn2+. • La configuration électronique du manganèse (Z = 25) est :. |
|
1. Propriétés du métal. 1.1.1. Configuration électronique 1.1.2
Dans les périodes inférieures la taille des ions métalliques aidant |
|
CCP Chimie 2 PC 2012 — Corrigé
fer et à la synthèse diastéréosélective d'un précurseur de l'acide berkelique. ions Fe2+ et Fe3+ on commence par écrire la configuration électronique. |
|
La structure électronique des complexes des métaux de transition :
Un complexe est un édifice polyatomique constitué d'un atome ou d'un cation central auquel sont liés des molécules ou ions appelés ligands. |
|
Lélément Cobalt
Le numéro atomique du fer est Z = 26. II - Structure électronique. II-1) Ecrire la configuration électronique d'un atome de fer dans son état ... |
|
Démixtion et ségrégation superficielle dans les alliages fer-chrome
DE LA STRUCTURE ÉLECTRONIQUE AUX MODÈLES THERMODYNAMIQUES par. Maximilien LEVESQUE 1.3 L'alliage binaire fer–chrome modèle des aciers ferritiques . 14. |
|
Cours de Chimie Structure de la matière
Chapitre 4 : Structure électronique de l'atome *2.5x1023 atomes de fer correspond à n = nombre d'atomes N= 0 |
|
Transport électronique polarisé en spin dans les contacts atomiques
???/???/???? transport des électrons `a travers un contact atomique de fer. ... directement la conductance `a la structure électronique du syst`eme. |
|
Sur la structure électronique des métaux et alliages de transition et
des métaux sont en effet des métaux de tran- sition et parmi eux |
| 1 Propriétés du métal 111 Configuration électronique 112 |
| Chapitre III : Structure électronique des atomes |
| L'élément Cobalt |
| Wikipedia : tableau périodique des éléments |
| Règles de remplissage pour les atomes polyélectroniques |
| Chapitre 1 - Configuration électronique |
| Structure électronique des atomes - Étienne Thibierge |
| Structure électronique des atomes - Étienne Thibierge |
| Cours de Chimie Structure de la matière - univ-ustodz |
Pourquoi l'ion Fe3+ est plus stable que Fe2+ ?
. Une couche à demi remplie est stable car le spin y est maximal.
|
1 Propriétés du métal 111 Configuration électronique 112
Étude des propriétés des ions ferreux et ferriques 2 1 Les complexes du fer 2 1 1 Structure Voici ci-dessous un |
|
Atomes polyélectroniques - UNF3S
➢valable pour la configuration électronique dans l'état fondamental ➢ordre croissant Fe 2+ et 26 Fe 3+ Fer Fe → Z=26 → 1s2 2s2 2p6 3s2 3p6 3d6 4s2 |
|
CCP Chimie 2 PC 2012 — Corrigé
Dans le cas des ions Fe2+ et Fe3+ on commence par écrire la configuration électronique du fer [Fe]: 1s2 2s2 2p6 3s2 3p6 4s2 3d6 On rétablit l'ordre des |
|
Chapitre 3 :Structure électronique des atomes
Chapitre 3 : Structure électronique des atomes Structure de la matière Page 1 sur 5 I Nombres quantiques A) Origine théorique La résolution de l'équation de |
|
LA STRUCTURE ELECTRONIQUE DES ATOMES
H ne possède qu'un seul électron, utilisé pour faire la liaison, il n'a donc aucun électron « inutile », donc aucun doublet non liant S, sur ses 6 électrons externes, |
|
Structure électronique des atomes - Étienne Thibierge
12 déc 2018 · Au programme Ce que vous devez savoir et savoir faire ⊳ Définir les nombres quantiques n, l, ml et ms et connaître les valeurs qu'ils peuvent |
|
Structure de latome - Free
couches et les sous- couches Exemples Al : aluminium Z=13, ce qui fait 13 électrons La structure électronique de l'aluminium est : (K)2 (L)8 (M)3 Fe : fer, Z= 26 |
|
Cours de Chimie Structure de la matière - USTO
Le quatrième et le cinquième chapitre représentent la structure électronique de l' atome, notion de la fer, 0 3 atome- gramme de fer 2 5x1023 atomes de fer |
|
Règles de remplissage pour les atomes polyélectroniques
Règle de Hund : pour une sous-couche donnée, la configuration électronique de plus basse énergie est obtenue en plaçant un maximum d'électrons de même |