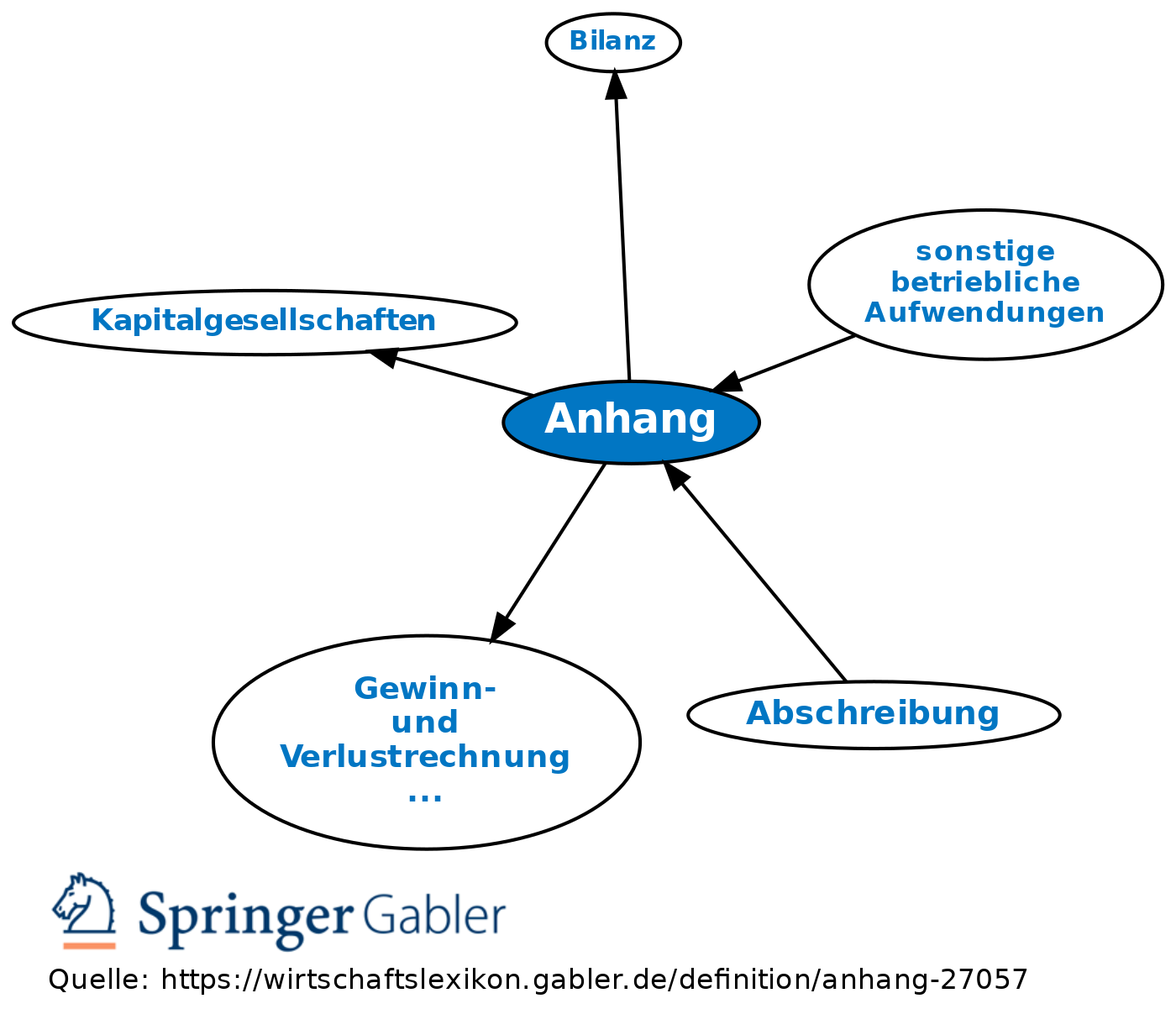
Anhang 19 zum EG -GMP Leitfaden
| Anhang 19 zum EG-Leitfaden der Guten Her |
|
Diese Richtlinie wurde durch die ICH
WebDer neue Anhang 20 zum EG-GMP Leitfaden entspricht der ICH Q9-Leitlinie zum Qualitäts |
|
Gute Herstellungspraxis gemäß Verordnung (EG) Nr. 2023/20
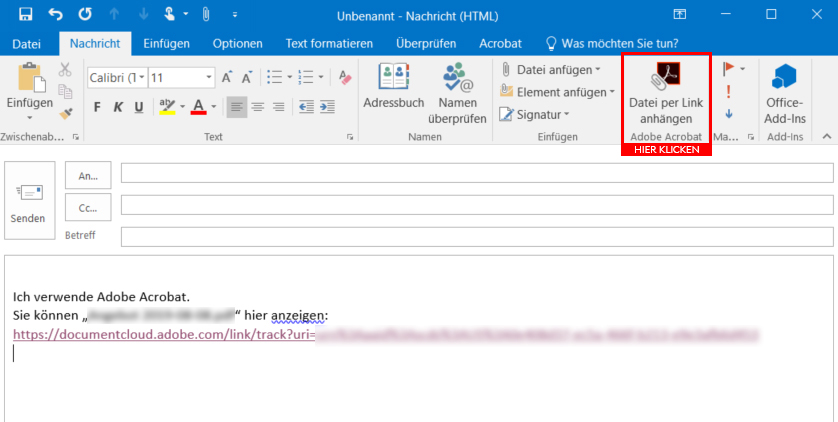
WebIm Anhang des Leitfadens findet sich neben dem Glossar eine Checkliste die bei der |
Was ist GMP und Wie funktioniert es?
Die Anforderungen an die Qualitätssicherung der Produktionsabläufe und -umgebung in der Herstellung von Arzneimitteln und Wirkstoffen mit dem Ziel einer Prozessüberprüfung sind von der Europäischen Kommission in den Grundsätzen und Leitlinien der Guten Herstellungspraxis (GMP) für Humanarzneimittel formuliert.
Was ist der GMP-Leitfaden?
Für Prüfpräparate, die zur Anwendung beim Menschen bestimmt sind, gelten die von der Europäischen Kommission festgelegten Grundsätze und Leitlinien für die Gute Herstellungspraxis bei Prüfpräparaten. Das Bundesministerium für Gesundheit stellt auf seiner Internetseite die deutsche Übersetzung des EU-GMP-Leitfadens zur Verfügung.
Wann tritt der GMP-Leitfaden in Kraft?
Februar 2022 in finaler Version veröffentlicht worden und tritt zum 21. August 2022 in Kraft. Der 6-seitige Anhang zum EU-GMP-Leitfaden fasst die GMP-Anforderungen an Inhaber einer Herstellungs/Einfuhrerlaubnis (Manufacturing Import Authorisation, MIA) von Human-, Prüf- und Tierarzneimitteln von außerhalb der EU/ des EWR zusammen.
Wie wird der EU-GMP-Leitfaden aktualisiert?
Englische Originale mit deutscher Übersetzung unserer Fachredaktion! Ihr EU-GMP-Leitfaden wird bei gesetzlichen Änderungen umgehend aktualisiert. Auch erhältlich als Personenlizenz inkl. Loseblattsammlung. inkl. Aktualisierung 1/2023




























![Hager Technischer Anhang - [PDF Document] Hager Technischer Anhang - [PDF Document]](https://i.ytimg.com/vi/0YaF_9xSkxI/maxresdefault.jpg)