sulfate de cuivre et zinc equation
|
Réactions doxydo-réduction
Il y a eu transfert d'électrons du zinc métal vers les ions cuivre Ici Zn a libéré des électrons : il est réducteur ; Cu2+ a capté des électrons : il est |
|
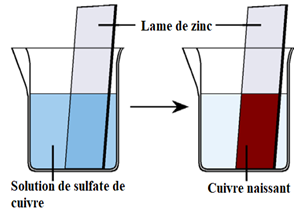
Expérience dune plaque de zinc plongée dans du sulfate de cuivre
Expérience 1: Matériel utilisé : - Une solution de sulfate de cuivre de concentration égale à 05 mol/L - Une lame de zinc (bien poncée pour enlever la |
|
1 But 2 Réaction entre le métal fer et une solution de sulfate de
“ Ecrire la demi-équation modélisant la transformation qui a eu lieu pour l'élément zinc ” Écrire l'équation chimique de la réaction en n'écrivant que les |
|
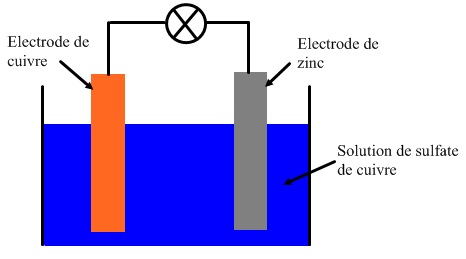
TP N°10 : LES PILES ELECTROCHIMIQUES
➢ Solution de sulfate de cuivre à 1 0 10-1 mol/L ➢ Solution de sulfate de cuivre à 1 0 mol/L ➢ Solution de sulfate de zinc à 1 0 10-1 Pile n° Equation de |
|
Pile et énergie I Réaction du zinc avec du sulfate de cuivre
Le sulfate de cuivre réagit avec le zinc: l'ensemble des réactifs (sulfate de cuivre et zinc) possèdent de l'énergie chimique Lors de la transformation |
|
Tp : comprendre et modeliser le fonctionnement dune pile
Equation chimique : Cu2+(aq) + Zn(s) = Cu(s) + Zn2+(aq) Faire un schéma avec une lame de zinc plongeant dans une solution de sulfate de cuivre Transfert |
|
Étude de la réaction entre la solution de sulfate de cuivre et le zinc
Quelles observations montrent que le zinc réagit avec la solution de sulfate de cuivre ? Ecrire le bilan de la transformation chimique puis son équation 10 |
|
Une lame de zinc un bécher contenant une solution de sulfate de
① Matériel : une lame de zinc un bécher contenant une solution de sulfate de cuivre ⑥ Equation de réaction de la transformation chimique + + Zn Zn Zn |
|
Réaction doxydoréduction
solution de sulfate de cuivre L'équation de la réaction qui a lieu entre la lame de zinc et la solution de sulfate de cuivre s'écrit donc : Cu ( ) 2+ + Zn |
ZnSO₄Le sulfate de zinc existe dans la nature à l'état anhydre.
Il s'agit du minéral zincosite orthorhombique.
L'heptahydrate de sulfate de zinc ZnSO4.
Quelle forme d'énergie est contenue dans le zinc et le sulfate de cuivre ?
L'énergie chimique contenue dans le Zinc et le sulfate de Cuivre s'est transformée en énergie thermique.
Est-ce que le cuivre attaque le zinc ?
Les quantités présentes dans le bois étant en général réduites, il est difficile d'évaluer le risque que le bois traité représente pour certains métaux.
Au contact direct de l'humidité, les sels de cuivre peuvent attaquer le métal (éléments de fixation par ex.) par substitution chimique du fer et du zinc.
|
? Zn2+
Les ions Cu2+ se transforment en cuivre Cu métal et la lame de zinc se transforme en ions Zn2+. La réaction inverse n'est pas possible. Oxydation : Zn. |
|
Oxydo-réduction et pile : commentaires scientifiques décrivant les
les demi-équations suivantes. La réaction globale entre le zinc et les ions cuivre. (II) est une réaction d'oxydoréduction. Elle se traduit par l'équation |
|
Observations : Identification des réactifs : Identification des produits
La réaction entre le sulfate de cuivre et le zinc : Observations : On admet que les ions SO42- ne participent pas à la réaction : on dit qu'ils sont. |
|
Pile et énergie I. Réaction du zinc avec du sulfate de cuivre.
Les transformations chimiques s'accompagnent généralement d'une libération d'énergie. Sous quelle forme est libérée cette énergie ? I. Réaction du zinc avec du |
|
Chapitre 6 : Les réactions doxydoréduction
1) Réaction entre les ions cuivre II et le métal zinc : ? Expérience : On plonge une lame de zinc dans une solution de sulfate de cuivre II (couleur bleue) |
|
Exercices de révisions : Physique-chimie
3. En déduire l'équation de la réaction étudiée (réaction de dismuation). On plonge une lame de zinc Zn?(s) dans une solution de sulfate de cuivre (II) ... |
|
Réaction doxydoréduction - Correction
sulfate de cuivre II de concentration c = 0.1 mol. Ecrire l'équation de la réaction qui a lieu entre la lame de zinc et la solution de sulfate de cuivre ... |
|
TP CHIMIE POUR SITE LYCEE
Equation de la réaction : Fe2+(aq) + 2 HO-(aq) ? Fe(HO)2(s) Solution aqueuse de sulfate de cuivre (II) (Cu2+(aq) + SO4. 2-(aq)) ... 4°) L'ion zinc Zn2+. |
|
? Matériel : une lame de zinc un bécher contenant une solution de
2- ne participent pas à la réaction : on dit qu'ils sont spectateurs. orangé pas présent au départ apparaît et la couleur du sulfate de cuivre (bleue). |
|
Un jardinier bien embété !!!
Hypothèses : soit réaction avec sulfate de cuivre chaux |
| I-Solution aqueuse de sulfate de cuivre et lame de zinc |
| I-Solution aqueuse de sulfate de cuivre et lame de zinc |
| Réaction d’oxydoréduction - Correction - AlloSchool |
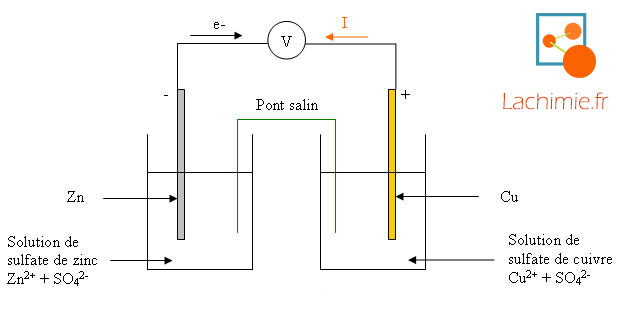
| 1) La pile Daniell : a)Description - AlloSchool |
| Réaction des acides et des bases – Exercices – Devoirs |
| Searches related to sulfate de cuivre et zinc equation filetype:pdf |
Quelle est la transformation chimique entre le zinc et le sulfate de cuivre?
- CONCLUSION : (page 138) Lors de la transformation chimiqueentre le zinc et le sulfate de cuivre, des ions cuivre II (Cu2+) sont transformés en atome de cuivre (Cu) et des atomes de zinc (Zn) sont transformés en ions zinc (Zn2+) : zinc + ion cuivre II ion zinc + cuivre Zn + Cu2+Zn2++ Cu II- Transformation chimique et énergie
Quels sont les ions qui donnent la couleur à la solution de sulfate de cuivre?
- Les ions qui donnent la couleur à la solution de sulfate de cuivre sont les ions cuivre II. 5.
. La décoloration de la solution est due à la disparition des ions cuivre II. 6.
. Cette couleur est caractéristique du métal cuivre.
Quels sont les réactifs du cuivre ?
- Le cuivre est l’un des réactifs.
. Lors de la transformation chimique les atomes de cuivre perdent deux électrons et se transforment en ions cuivre Cu2+
.Cette transformation chimique met en jeu le couple Cu2+ (aq)/ Cu (s).
. C’est une réaction d’oxydoréduction.
Est-ce que la lame de zinc est la borne négative de la pile?
- Donc la lame de zinc est la borne négative de la pile et la lame de cuivre la borne positive. 4.
. Le sens du courant électrique est en accord avec la polarité des bornes de la pile, car il va dans le sens inverse des électrons libres.
|
Chapitre 6 : Les réactions doxydoréduction - Physagreg
1) Réaction entre les ions cuivre II et le métal zinc : ➢ Expérience : On plonge une lame de zinc dans une solution de sulfate de cuivre II (couleur bleue) |
|
→ Zn2+
Dans une demi-équation rédox, on trouve l'oxydant et le réducteur d'un cuivre Cu Sulfate de zinc (Zn2+, SO4 2−) Lame de zinc Zn Sulfate de cuivre |
|
Chap4 Pile électrochimique et énergie chimique
Réaliser, décrire et schématiser la réaction entre une solution aqueuse de sulfate de cuivre et de la poudre de zinc en réalisant une pile I Comment fabriquer |
|
Pile et énergie I Réaction du zinc avec du sulfate de cuivre - Free
Les transformations chimiques s'accompagnent généralement d'une libération d' énergie Sous quelle forme est libérée cette énergie ? I Réaction du zinc avec du |
|
Observations : Identification des réactifs : Identification des produits
La réaction entre le sulfate de cuivre et le zinc : Observations : On admet que les ions SO42- ne participent pas à la réaction : on dit qu'ils sont spectateurs |
|
Expérience dune plaque de zinc plongée dans du sulfate de cuivre
En revanche les ions zinc ne peuvent pas attaquer une plaque de cuivre Les ions cuivre ayant pour formule 2+, La réaction se traduit par le fait qu'un ion |
|
Oxydo-réduction et corrosion
sulfate de cuivre II CuSO4 Solution aqueuse Equation de précipitation : Fe2+ + 2OH- Fe(OH)2 (p) Les ions cuivre Cu2+ ont oxydé le fer : l'ion Cu2+ est un oxydant Le fer a un autre bécher contenant une solution de sulfate de zinc à |
|
Exercice 14_07r
Dans 100 mL de solution de sulfate de cuivre à 0,1 mol L-1, on agite une masse m=0,8g de zinc Déterminer la composition de la solution V76,0 )Zn/ Zn(E2 0 |
|
Classification qualitative des couples oxydant réducteur - Fastef
Ecrire l'équation-bilan de la réaction de fonctionnement d'une demi ✓ Déterminer la f e m -Les ions zinc, cuivre (II) et sulfate dans les solutions des deux |
|
REACTIONS DOXYDATION ET DE REDUCTION
On peut décrire la transformation du zinc par l'équation : Zn°(s) - 2 e dans une solution de sulfate de cuivre, et une électrode d'argent plongeant dans une |