acide faible base faible
|
BASE FAIBLE *** COUPLE ACIDE-BASE
ACIDE FAIBLE – BASE FAIBLE *** COUPLE ACIDE-BASE 1 Notion d'acide faible 1 1 Expérience : On dissous 01 mol d'acide éthanoïque CH 3COOH dans un volume V |
|
Fiche de révisions sur les acides et les bases
Exemples de réactions de dissolution de bases et d'acides faibles : • L'acide 3°) Réaction entre une solution de base faible et une solution d'acide fort : |
|
PH et pKa
Formule générale pour le pH de solutions d'acide/base faible: [H3O+] = Ka (([AH] - [H3O+] + [OH-]) / ([A-] + [H3O+] - [OH-])) • pH d'une solution d'acide |
|
Chapitre 1 Acides et bases
L'acide conjugué d'une base faible est un acide faible Exemples : 1) L'ammoniaque est une base faible dans l'eau (cf plus haut) le pKa du couple ammonium |
|
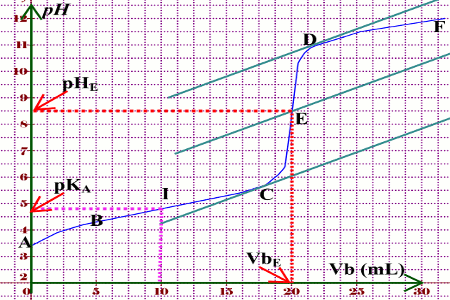
§ 7 (suite) Titrages acide-base
Considérons le titrage d'une solution d'un acide faible tel que l'acide acétique par exemple par une base forte comme NaOH La fonction pH = ƒ(!) dans ce cas |
|
Chapitre Chimie N°4 : Les Acides et les Bases faibles en solution
Q1/ Calculer la concentration en ions H₂O** Q2/L'acide chlorhydrique est-il un acide fort ou un acide faible? Q3/ Ecrire l'équation de la réaction de l'acide |
|
Lecon n° 7 : acides et bases faibles couples
L'étude des acides forts des bases fortes et leurs propriétés étant terminée nous abordons dans cette présente leçon les acides faibles et les bases faibles |
|
C7 : ACIDE FAIBLE
Généralisation : Un acide est faible en solution aqueuse si sa réaction avec l'eau est partielle ou limitée Pour une telle |
|
C7-acides-faibles-et-bases-faiblespdf
C7- ACIDES FAIBLES ET BASES FAIBLES Année Un indicateur coloré est un acide faible ou une base faible d'un couple acide base dont les formes acide et |
Un acide fort est un acide réagissant totalement avec l'eau.
Si sa concentration est c, alors .
Un acide faible AH réagit avec l'eau selon une réaction limitée .
Une base forte réagit avec l'eau selon une réaction totale.
Comment reconnaître un acide faible et une base faible ?
Comment savoir si on a un acide fort ou faible ? On peut savoir si on a un acide fort ou faible à partir de sa dissociation : S'il se dissocie totalement en solution, il s'agit d'un acide fort.
S'il ne se dissocie que partiellement, il est considéré comme un acide faible.
Quel est le pH de l'acide faible ?
On considère qu'un acide est faible lorsque son pKa est supérieur à −1,74 à 25 °C (pKa du cation hydronium H3O+).
Pour un pKa supérieur à 14, on dit qu'il est indifférent.
Quels sont les bases faible ?
Une base faible est une base qui ne se dissocie que partiellement en solution.
Une base forte est une base qui se dissocie complètement en solution.
K b est une constante d'équilibre modifiée pour la dissociation des bases faibles.
Elle est représentée par l'équation K b = [ B H ] + [ O H − ] [ B ] .
|
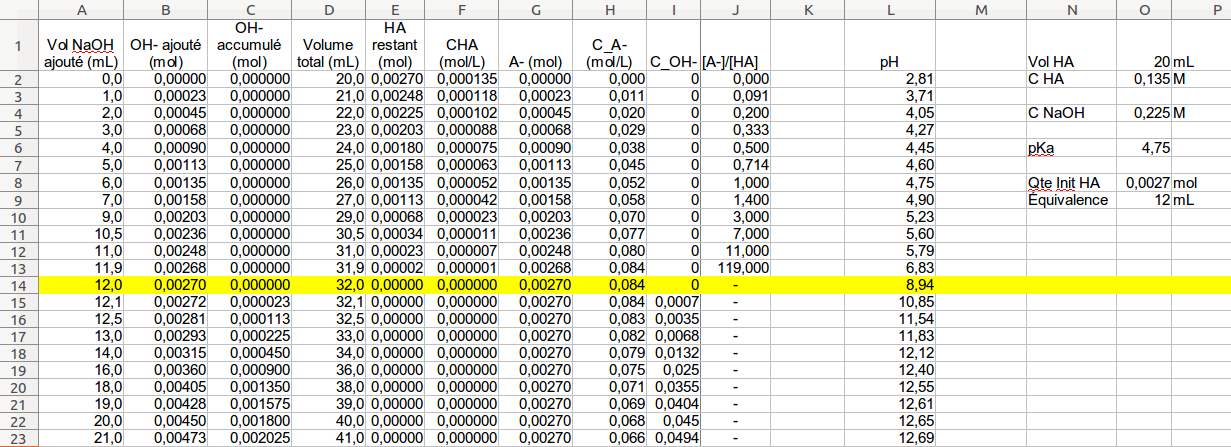
Dosage acide faible – base forte
Dosage acide faible – base forte. Les relations établies classiquement le sont pour : ? un acide suffisamment faible et pas trop dilué. |
|
Fiche de révisions sur les acides et les bases
donc la base la plus forte dans l'eau. Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et. 14. 10. |
|
§ 7 (suite) Titrages acide-base
Considérons le titrage d'une solution d'un acide faible tel que l'acide acétique par exemple |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
Cas d'une base forte. 2.4. Cas des bases faibles. 2.5. Cas d'un mélange d'un acide fort et d'un acide faible. |
|
Dosage acide faible-base forte
Dosage acide faible – base forte. Les relations établies classiquement le sont pour : ? un acide suffisamment faible et pas trop dilué. |
|
Chapitre 1 Acides et bases
L'acide conjugué d'une base faible est un acide faible. Exemples : 1) L'ammoniaque est une base faible dans l'eau (cf. plus haut) le pKa du couple. |
|
VI..Etude sommaire des mélanges
d'hydrolyse des acides et bases faibles augmente avec la dilution!) La réaction entre un acide faible et une base forte est complète si la constante ... |
|
7. Transferts de protons Equilibres acide-base
hydrolyse (réaction avec l'eau) est complète. Dans ce cas H2O capte le proton libéré par l'acide. H2O agit donc comme une base. NH3 est une base faible. Son. |
|
Solutions tampons
de la concentration (voir dosage acide fort - base forte) et ces solutions ne sont donc pas des tampons satisfaisants vis à vis de la dilution. |
|
Les couples acide-base conjuguées
dans un couple acide/base conjuguée si un acide est fort |
|
Révisions sur les acides et les bases - Nicole Cortial
base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d' |
|
PH et pKa - Eli Zysman-Colman
générale pour le pH de solutions d'acide/base faible: [H3O+] = Ka (([AH] - [H3O+] + [OH-]) / ([A-] |
|
Chapitre 1 Acides et bases
e est dit : — fort dans l'eau ssi il est totalement dissocié dans l'eau ssi Ka > 1 ssi pKa < 0; — faible |
|
VIEtude sommaire des mélanges
e calcule en négligeant la base faible Page 6 Acides et bases Chapitre VI 82 Cette |
|
Dosage acide faible – base forte
acide faible – base forte un acide suffisamment faible et pas trop dilué, ▫ ou un acide pas |
|
Les acides et bases en solution aqueuse - Groupe Transition
ient d'ionisation (de dissociation) d'un acide ou d'une base faible Pourcentage d'ionisation (de |
|
Cours 5 - Equilibres Acido-basiques
me totale AH H2O H3O+ A- Acide fort Acide faible Base forte (B, BH+, OH-), Base faible |