système homogène chimie
|
Thermochimie/equilibres chimiques
Dans le cas de systèmes homogènes gazeux la constante d'équilibre peut être exprimée en fonction : ➢ Des fractions molaires : On sait que l'expression de |
|
I Équilibre homogène
Calculer la constante d'équilibre Kp de cette réaction ? 15 À 350°C la pression du système à l'équilibre est 0105 atm Calculer les constantes d |
|
CHAPITRE-1-Generalitespdf
Chimie 02 THERMODYNAMIQUE ET CINETIQUE CHIMIQUE CHAPITRE 1 GENERALITES SUR LA Système homogène Un système est homogène s'il est constitué d'une seule |
|
Généralités sur les systèmes chimiques
UE pharmacie - Chimie – Chimie physique Année universitaire 2011/2012 Equation qui caractérise l'état du système homogène en reliant différentes |
|
Généralités sur les systèmes chimiques
Un système comportant une seule phase est dit homogène ou monophasé Un système comportant plusieurs phases est dit hétérogène ou polyphasé Page 11 11 |
|
Première partie SVI-STU corrigée
1/ Système homogène Dans ces conditions les constituants du système se trouvent dans la même phase (liquide ou gazeuse) Page 31 31 a) Loi d'action de |
|
Chapitre 1
Les variables d'état d'un système homogène qu'elles soient physiques ou chimiques se classent en deux catégories: • Variables extensives Yi Elles mesurent |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
chimie : la cinétique chimique I 2 Le Système I 2 1 Définition générale d'un étudié (on considérera un système homogène constitué de n constituants A;) |
|
Chimie des solutions et thermodynamique Cours
- Système homogène : C'est un système qui représente une seule phase Exemple : Eau + Alcool - Système hétérogène : Représente plusieurs phases Exemple |
|
Chimie Générale (Chimie 1)
23 déc 2020 · Le dernier chapitre (chapitre VIII) est réservé à la cinétique chimique ou on étudie l'évolution dans le temps des systèmes réactionnels Ce |
C'est quoi KP en chimie ?
Le symbole Kp désigne pour sa part la constante d'équilibre en termes de pressions partielles.
Un équilibre hétérogène est un équilibre chimique entre substances intervenant dans des phases différentes dont au moins une de ces substances se trouve dans une phase où sa concentration est constante.
Comment calculer la constante d'équilibre K ?
1Expression de la constante d'équilibre.
Kc=[NH3(g)]2[N2(g)]⋅[H2(g)]3.
2) Concentrations molaires à l'équilibre.
NH3:8moles2L=4moles1L=4,0M.
N2:48g2L=24g1L=24g28g/moldeN2=0,86M.
H2:10g2L=5g1L=5g2g/moldeH2=2,5M.
3) Calcul de la constante d'équilibre.
Kc=[4,0M]2[0,86M]⋅[2,5M]3=1,19.
Soit le système suivant : 2NH3(g)⇌N2(g)+3H2(g)
|
I Les concepts de la thermodynamique
Chim387 - Les surfaces et interfaces en chimie physique et biologie. 2012-2013. Un système physico-chimique est défini par la connaissance de toutes les |
|
Cinétique chimique Rappels
1 - Cinétique chimique en phase homogène. aA + bB ? mM + nN (système fermé à volume constant) ... Cinétique chimique en phase homogène. Nobel Chimie. |
|
Génie de la Réaction Chimique: les réacteurs homogènes
Jul 14 2022 chimie : notions de mole et de concentration |
|
FACULTE DE CHIMIE DEPARTEMENT DE CHIMIE ORGANIQUE
d'utilisation des données thermodynamiques (la thermochimie) les équations de base pour calculer les capacités calorifiques des systèmes homogènes |
|
Cinétique chimique
pour les réactions en système fermé isochore et homogène. v = k [A] [B] v = k. p. A. .p. B. k = constante de vitesse de la réaction. |
|
Travail dirigé 9 : Léquilibre chimique
quotient réactionnel (Q) et évolution du système. - constantes d'équilibres (Kc Kp). - équilibre homogène |
|
Chimie Inorganique Avancée Catalyse industrielle
+ chimie organométallique (cat. homogène) CMI chap. 8 2 réactions indépendantes pour décrire les évolutions du système. |
|
Reaction chimique - Thermodynamique - Cinétique
C'est la cas le plus fréquent en chimie. Lorsqu'un système évolue à pression constante la chaleur reçue par le système est égale à sa variation d'enthalpie |
|
I. Équilibre homogène
les concentrations des autres substances dans le système qui sont en général 1M ou plus faible d'où la concentration de l'eau varie très peu ou ne varie |
|
Doctorat en sciences en : Chimie Industrielle
acido-basique dans un système homogène (le dioxane-eau) par deux méthodes de exhaustive des principaux substituants à effet (+I) rencontrés en chimie ... |
| I Les concepts de la thermodynamique |
| Description et ?volution d'un syst?me physico- chimique vers un ?tat |
| Chimie g?n?rale |
| Fili?re Sciences de la Mati?re Chimie Cours Chimie des Solutions |
| ?tat et ?volution d'un syst?me chimique |
| Cin?tique chimique |
| Chapitre 8 :Le potentiel chimique - Melusine |
| Chapitre VI LES METHODES EN ANALYSE IMMEDIATE Volume |
| CHIMIE - Dunod |
Caractéristiques d'un Système homogène
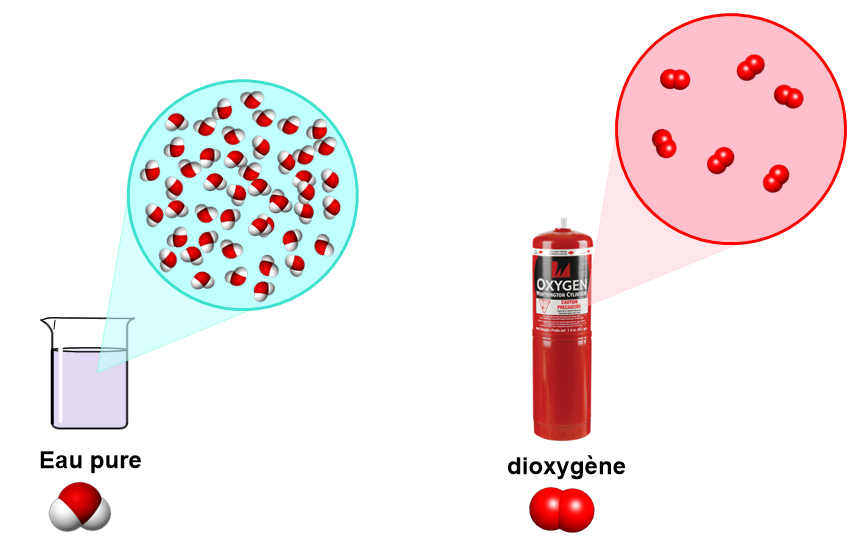
Quelles caractéristiques doit avoir un système homogène? -Il doit avoir une seule phase matérielle (liquide, solide ou gazeuse). -Lorsqu'il s'agit d'un mélange, ses composants doivent pouvoir former une seule phase uniforme. C'est le cas du café et du sucre. S'il y a des cristaux de sucre non dissous au fond du verre ou de la tasse, ils constituent...
L'échiquier et La subjectivité
Cette dernière caractéristique peut provoquer de la confusion et des vues contradictoires. L'échiquier (sans les pièces), par exemple, représente un point où des opinions différentes se posent à son sujet. Est-il homogène ou hétérogène? Et si les carrés noir et blanc alternent en rangées (un blanc, un noir, etc.), quelle serait la réponse dans ce s...
Classification
Les systèmes homogènes peuvent avoir de nombreuses classifications, qui dépendent de la branche de connaissance à laquelle ils appartiennent. En chimie, il ne suffit pas d'observer superficiellement un système, mais de trouver quelles particules le composent et ce qu'elles y font.
Solutions
Les solutions insaturées sont des mélanges ou des systèmes homogènes présents non seulement en chimie mais dans la vie quotidienne. La mer et les océans sont des masses gigantesques d'eau salée non saturée. Les molécules de solvant, généralement en phase liquide, entourent les molécules de soluté et les empêchent de s'agréger pour former un solide ...
Réactions homogènes
Les réactions homogènes sont peut-être les systèmes chimiques homogènes les plus importants. En eux, tous les réactifs sont dans la même phase, notamment la phase liquide ou gazeuse. Ils se caractérisent par des contacts et des collisions moléculaires plus importants entre les réactifs. Puisqu'il n'y a qu'une seule phase, les particules se déplacen...
Méthodes de Fractionnement
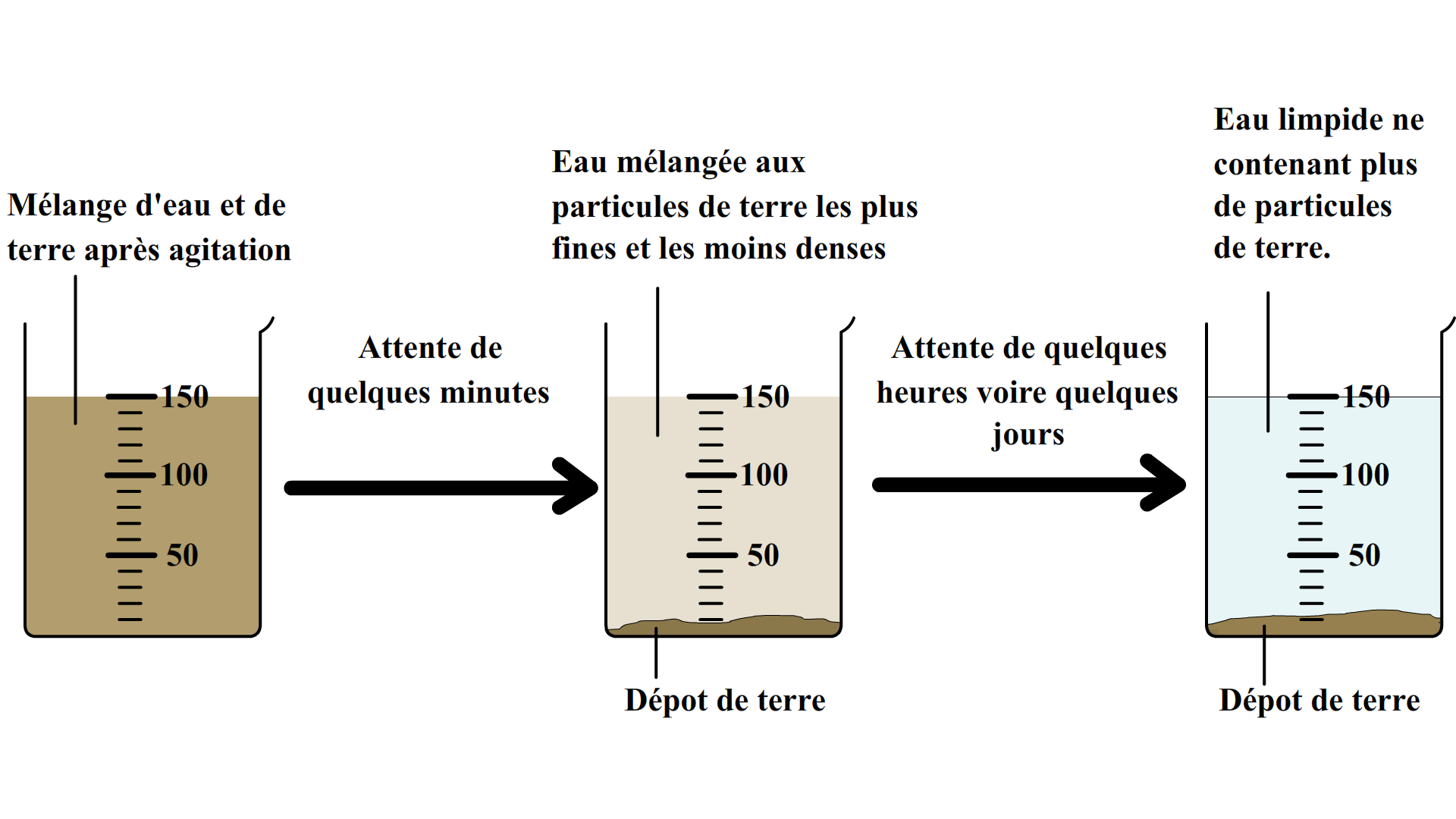
En principe, compte tenu de leur uniformité, il n'est pas possible de séparer les composants de systèmes homogènes par des méthodes mécaniques; et encore moins s'il s'agit d'une substance ou d'un composé pur, dont les fractionnements ses atomes élémentaires sont obtenus. Par exemple, il est plus facile (ou plus rapide) de séparer les composants d'u...
Évaporation
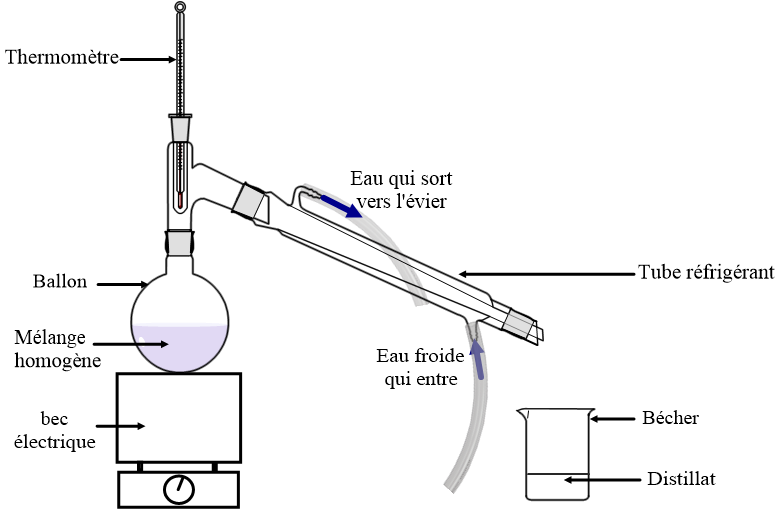
L'évaporation consiste à chauffer une solution jusqu'à ce que le solvant s'évapore complètement, laissant le soluté se déposer. Par conséquent, cette méthode est appliquée à des systèmes homogènes liquide-solide. Par exemple, lors de la dissolution d'un pigment dans un récipient d'eau, le système est initialement hétérogène, car les cristaux du pig...
Rotaévaporation
Cette méthode permet de récupérer des solvants organiques par application d'un vide. Il est très utile, en particulier lors de l'extraction d'huiles ou de graisses à partir de matières organiques. De cette manière, le solvant peut être réutilisé pour de futures extractions. Ces expériences sont très courantes dans l'étude des huiles naturelles obte...
C'est quoi une solution homogène ?
. Les mélanges homogènes présentent les caractéristiques suivantes : Ils comportent une seule phase visible.
. Cette phase est généralement à l'état gazeux, liquide, ou solide.
Comment savoir si une solution est homogène ?
C'est quoi homogène et hétérogène ?
. Dans le cas contraire il est dit hétérogène.
Comment obtenir un mélange homogène ?
- L'obtention d'un mélange homogène passe en général par une phase d'agitation, de « brassage », afin de forcer le déplacement des éléments des deux phases initiales et de les répartir uniformément. Dans le cas d'une mélange de poudres, on peut aussi passer par une phase de broyage,...
Quelle est la différence entre une phase et un système hétérogène ?
- Kubo définit une phase comme une substance physiquement et chimiquement homogène 3. Greiner définit une phase comme une des parties homogènes d'un système hétérogène 4, étant entendu qu'un système homogène constitue une unique phase.
Quelle est la différence entre un mélange homogène et un alliage homogène ?
- Au refroidissement, il peut se produire soit la solidification d'une seule phase, soit la solidification de plusieurs phases, voir l'article Diagramme de phase. Lorsque l'on a formation d'une seule phase, on ne parle pas de mélange homogène mais d'« alliage homogène », ou de « solution solide ».
Comment obtenir une homogénéité dans un mélange de liquide et de solide en poudre ?
- Si le solide ne se dissout pas, on peut obtenir une certaine homogénéité dans le mélange d'un liquide et d'un solide en poudre si l'application n'est pas trop « regardante ». La viscosité du liquide et son affinité chimique pour le corps en poudre sont les principaux paramètres de la stabilité du mélange, en plus de la granulométrie .
|
EQUILIBRES CHIMIQUES CINETIQUE CHIMIE EN SOLUTION
2) Réactions en milieu homogène / hétérogène 10 3) Avancement de la réaction pour un système fermé 11 4) Grandeurs dérivées de 12 II – La recherche |
|
Chimie générale - Dunod
Les mélanges sont soit homogènes, soit hétérogènes Un mélange homogène est un système dont les constituants sont uniformément mélangés, même à l' |
|
Thermodynamique chimique1 systemes ouverts 2a mp 2016 - Unisciel
Chimie plan du cours de thermodynamique chimique THERMODYNAMIQUE DES la même valeur en tout point) d'un système pouvant être hétérogène |
|
I Les concepts de la thermodynamique - u-psudfr
Chim387 - Les surfaces et interfaces en chimie, physique et biologie thermodynamique de définir le système sur lequel il va s'appliquer Mathématiquement, on dit que Z est une fonction homogène de degré 1 des quantités de matière ni |
|
THERMODYNAMIQUE CHIMIQUE - Faculté des Sciences – El Jadida
FILIERE: SCIENCES DE LA MATIERE CHIMIE SEMESTRE 4 (SMC4) DEPARTEMENT DE CHIMIE ANNEE PHASE, SYSTEME HOMOGENE SYSTEME |
|
Diagrammes de phases I – Notion de phases II – Variables dun
22 mai 1998 · s'assurer que le système est bien homogène (même composition chimique et mêmes propriétés en tout point) ▫ Phase gazeuse Tous les gaz |
|
FACULTE DE CHIMIE DEPARTEMENT DE CHIMIE - USTO
pour calculer les capacités calorifiques des systèmes homogènes, ainsi que les énoncés historiques du second principe de la thermodynamique Nous avons |
|
Chapitre 8 :Le potentiel chimique
volume du système, donc le calcul à partir de G est plus aisé B) Signification physique λ au lieu de λ , on dirait que c'est une fonction homogène du 2 ème ordre ) Nouvelle définition du gaz parfait (en chimie) : C'est un gaz pour lequel |