une solution s de volume v=150 ml
|
Exercice QM
Exercice QM - Chimie Physique |
|
Classe 3ème Chimie N°1 : Les Solutions Exercices résolus
Une perfusion de volume V sol = 15 L contient une quantité de matière n (G) = 417 mmol de glucose Calculer la concentration molaire en glucose de la perfusion Correction : - Concentration molaire en glucose de la perfusion - IV- Exercice 8 : Préparer une solution par dissolution Énoncé : |
|
Dosages par titrage direct 10 Extraits de sujets corrigés du
La solution titrante de concentration en diiode C 2 = (100 001)×10 –2 mol L-1 est ensuite ajoutée jusqu’à l’équivalence repérée par le changement de couleur du milieu réactionnel L’équivalence est obtenue après avoir versé un volume V E = (628 005) mL de solution de diiode L’équation support du dosage est : I 2(aq) |
Comment calculer le volume d’une solution titrante ?
D’après l’équation support du titrage, on a vu qu’à l’équivalence : V ’A est le volume de solution S’ titré, c’B est la concentration molaire de la solution titrante d’hydroxyde de sodium, VE le volume versé à l’équivalence. ' . V ' 3 . V ' VE = 2 . V D’après la verrerie disponible, V’A vaut au VE = 6×10–2 ×25,0 = 1,5 mL.
Comment calculer l’équivalence d’une solution titrante ?
La solution titrante, de concentration en diiode C2 = (1,00 0,01)×10–2 mol.L-1 est ensuite ajoutée jusqu’à l’équivalence repérée par le changement de couleur du milieu réactionnel. L’équivalence est obtenue après avoir versé un volume VE = (6,28 0,05) mL de solution de diiode. 1.1.
Comment déterminer la valeur du volume versé à l'équivalence ?
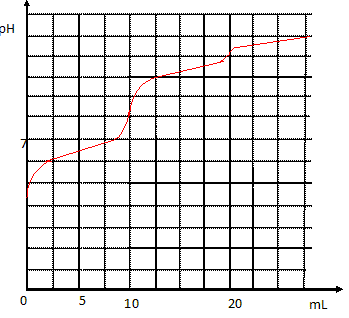
Il faut donc déterminer la valeur du volume versé à l’équivalence et en toute rigueur, il faudrait tracer la courbe représentative du pH en fonction du volume d’hydroxyde de sodium versé ; puis mettre en œuvre la méthode des tangentes parallèles (voir fin de la correction). aucune feuille de papier millimétré n’a été fournie avec le sujet.
|
Quantité de matière - Prophychi
La masse moyenne d'un morceau de sucre est 60g. saccharose) contenue dans un volume V=150mL de solution aqueuse de concentration. |
|
Td corriges biochmv 2014-2015.pdf
Nombre de moles (n) mol = Masse (m) g / Masse molaire (M) g/mol. Nombre de moles (n) mol = Concentration molaire (C) mol/L x Volume (V) L. Solution 1 : 250 mL |
|
Mélange de solutions électrolytiques Exercice n°2
V1 = 150 mL de solution S1 de chlorure de cuivre(II) Cu2+. (aq)+2 Cl- 3-Quel est le volume final V du mélange ? Donner l'expression de la concentration ... |
|
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
Masse molaire de l'acide tartrique noté H2A : M(H2A) = 150 g.mol-1 volume V = 15 |
|
Solutions aqueuses Ce quil faut retenir
où V est le volume de la solution souhaitée (en L) cm la concentration sirop commercial à prélever est donc : V = 1 |
|
Composition dun système chimique Prélever des quantités de
Calculer la quantité de matière contenue dans une masse m = 150 g d'acide sulfamique. On prépare un volume V=800 mL d'une solution détartrante d'acide ... |
|
Correction Ex 1) Le sucre est un solide moléculaire constitué de
dissout pour obtenir une solution aqueuse de volume 20 L. a) Dans la solution |
|
Accompagnement personnalisé – Physique-chimie Concentration
de deux solutions S1 et S2 telles que : ? V1 = 150 mL de solution S1 de chlorure de cuivre(II) Cu2+ ... 3- Quel est le volume final V du mélange ? |
|
Exercice 1 : 150 mL déthanol ont une masse de 120g 1) Calculer la
Le volume V = 150 mL à convertir car on veut un volume en Litres. On fait une phrase et on fait très attention à mettre les unités (s'il y en a )!. |
|
Untitled
Soit S la solution obtenue de volume V = 150 mL. 1. a. Lors de l'obtention de la solution S |
Comment calculer le volume V d'une solution ?
.V / C0.
. On veillera à exprimer les concentrations dans les mêmes unités et on obtiendra alors V0 dans l'unité utilisée pour exprimer V.
. Soit V0 = 50,0 . 0,020 / 0,10 = 10 mL.
Comment calculer V avec cm et m ?
Comment calculer V avec C et N ?
. On notera donc n(Ag+) cette quantité. 3.
. La concentration est donnée dans l'énoncé (C = 2,0 × 10–2 mol.
Comment faire une dilution au 1 50 ?
. Soit une dilution à 50% : cela signifie que la concentration est divisée par 2.
. On doit donc diviser par 2 le nombre de molécules présentes par litre de solution.
|
Travail dirigé 5 : La concentration dune solution - Unité AFO
Calculer la concentration molaire d'une solution dont un volume de 50 mL contient 0,01 mol de substance dissoute (R : 0,2 mol/L) 8 Comment préparer 100 |
|
Solutions aqueuses Ce quil faut retenir - Lycée Maurice Ravel
Il est aussi égal au rapport du volume de solution fille que l'on souhaite préparer de sirop commercial à prélever est donc : V = 1,5x10-1 L, soit environ 150 mL |
|
Calcul de la concentration massique dune solution - pontonniers
Soluté Volume de solution Solution 1 15g de chlorure de sodium 250 mL Solution 2 Il est conditionné sous forme de flacons de 150mL a Quel volume |
|
Télécharger ce fichier pdf - Labolycée
différencier le volume titré (prélèvement) du volume de la solution dont on cherche la Masse molaire de l'acide tartrique, noté H2A : M(H2A) = 150 g mol- 1 |
|
M 1 LA VERRERIE PRINCIPALE - AC Nancy Metz
Ex : une P200 pour prélever 150µL et non pas une P1000 Protocole d'utilisation Régler le volume à prélever et placer l'embout approprié Rincer l'embout ou |
|
31 Types de solutions - Pages
pourcentage en masse par volume ( m/V) de la solution ? m soluté = 4,00 g de NaCl se trouve dans une bouteille de 150 mL de cette solution ? m soluté = ? |
|
Volume molaire partiel, système eau-méthanol
22 402 5 0 35 150 82 174 67 806 6 0 5 150 103 846 46 154 Exemple de calcul pour la préparation de la solution 1: Fraction molaire en méthanol 0 05 |
|
DÉTERMINATION DE LA CONCENTRATION DUNE - Pierron
massique en sucre recherchée (g L-1) 0 50,0 100,0 150,0 200,0 250,0 300,0 350,0 400,0 Volume de la solution (mL) 100,0 100,0 100,0 100,0 100,0 100,0 |
|
Détermination du pourcentage massique en fer dune solution anti
Eprouvettes graduées de 10 et 20 mL ▫ 2 béchers de 150 mL ▫ 1 erlenmeyer de 200 mL Le volume de solution titrante versée à l'équivalence : U(Veq) = |