adiabatique isotherme
|
Le premier principe de la thermodynamique
Lors d'une compression adiabatique la température augmente Une transformation monotherme concerne un système mis en contact avec une seule source de chaleur |
|
Cours 5 : Transformations thermodynamiques Chaleurs molaires
○ Transformations iso (-therme -bare -chore) adiabatique ○ Chaleurs Transformation isotherme d'un gaz parfait T=cte ⇒ U=0 ⇒ 1 er pp ⇒ W A |
|
Diagramme de Clapeyron (corrigé)
– d'une compression isotherme avec V2 = V1/2 – d'une compression adiabatique avec V2 = V1/2 V P O V1 2V1 P1 P1 2 P1 2γ b) Tracé sur un même diagramme |
|
Chapitre III : Premier principe de la Thermodynamique Système
Transformation adiabatique : Le système n'échange pas de chaleur avec le milieu extérieur Transformation isochore : Le volume du système reste constant durant |
|
Thermodynamique NP
On peut constater sur un exemple simple ( compression isotherme d'un GP) qu Attention pour une transformation adiabatique irréversible il n'est pas possible |
|
THERMODYNAMIQUE
TRANSFORMATION ISOTHERME : elle se fait à température constante T = Cte • TRANSFORMATION ADIABATIQUE : elle se fait sans échange de chaleur avec l'extérieur |
|
THERMODYNAMIQUE
Dans un moteur diesel la compression adiabatique rapide de l'air par un facteur ~20 résulte en une élévation de température telle que lorsque l'essence y |
|
D] Premier principe de la thermodynamique
La transformation isotherme c'est une réaction qui s'effectue à Température constante contraire d'une paroi adiabatique ➢ Cas particulier du gaz parfait |
|
Transformations dun système 1 principe de la thermodynamique
Transformation adiabatique/diathermane : sans échange de chaleur entre le milieu Pour qu'une transformation soit isotherme il faut au contraire un récipient |
|
LES PRINCIPES THERMODYNAMIQUE
Une transformation adiabatique implique que la température du système varie (souvent très fortement) alors qu'une transformation isotherme n'est possible que si |
C'est quoi une détente isotherme ?
Au cours d'une détente isotherme d'un gaz contre une résistance extérieure, le système doit recevoir de la chaleur pour maintenir une température constante.
La transformation doit s'effectuer lentement pour permettre l'échange de chaleur.
Elle est considérée comme réversible.Comment réaliser une compression isotherme ?
On réalise la compression isotherme d'une mole de gaz parfait contenu dans un cylindre de section S.
On suppose que le poids du piston est négligeable devant les autres forces intervenant dans le problème.
La température To est maintenue constante par un thermostat.
P1et P2 sont les pressions initiale et finale.Est-ce que adiabatique implique isotherme ?
Dans le cas adiabatique le gaz est refroidi par la détente et sa température finale est plus basse que sa température initiale.
Dans le cas isotherme on laisse la chaleur entrer dans le système : le supplément de travail observé par rapport à la détente adiabatique correspond à la chaleur gagnée par le système.1.
Qui est imperméable à la chaleur. 2.
Se dit d'une transformation au cours de laquelle un système de corps n'échange pas de chaleur avec le milieu environnant ; relatif à une telle transformation.
|
Le premier principe de la thermodynamique
Détente adiabatique irréversible). ] Page 23. 12. Détente isotherme d'un gaz parfait. ( U/ |
|
Diagramme de Clapeyron (corrigé)
– d'une compression isotherme avec V2 = V1/2. – d'une compression adiabatique avec V2 = V1/2. V. P. O. V1. 2V1. P1. P1. 2. P1. 2γ b) Tracé sur un même diagramme. |
|
Chapitre VIII. Les diagrammes thermodynamiques
VIII.1.3 : Représentation des isothermes et adiabatiques réversibles : Les Compression adiabatique (ηs)c = (WTrev) / (WTirr) avec 0 < ηsc < 1. Détente ... |
|
بلا عنوان
3- Détente adiabatique et réversible. 4- Détente adiabatique et irréversible isotherme la température passant de 300k à 290k |
|
«EXERCICES ET PROBLEMES CORRIGES DE
Irréversible – Isotherme – Isochore – Isobare – Adiabatique – Sublimation –. Condensation – Vaporisation – Liquéfaction – Fusion – Solidification -. Enthalpie |
|
Le Son et la Thermodynamique
On remarquera que l'expression de la vitesse diff`ere du cas adiabatique par un facteur. √ γ. Distinction des cas isotherme - adiabatique. Lorsque le gaz se |
|
Cours 5 : Transformations thermodynamiques. Chaleurs molaires
○ Transformations iso (-therme -bare |
|
Chapitre 1 : Vocabulaire thermodynamique
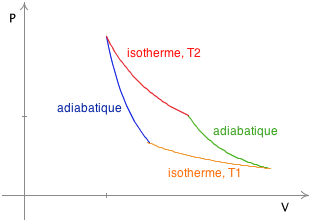
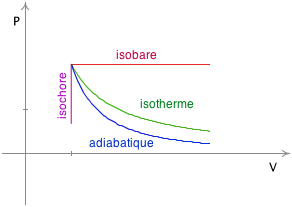
L'adiabatique. 0. L'isotherme. 0. 1. On conclut que dans le diagramme (P-V) l'adiabatique est plus raide que l'isotherme. (Fig. 3.11). Figure 3.11 : La pente |
|
Ch 13- Transformatio#664A63
5 – Pentes de l'adiabatique et de l'isotherme. On veut comparer les pentes des courbes adiabatiques et isothermes. Pour cela du point. A on fait passer une |
|
Sujets dexamens de thermodynamique avec solutions
a) Sur un même diagramme de Clapeyron représenter l'allure de cette transformation lorsqu'elle est : i) adiabatique ; ii) isotherme. b) i) Représenter |
|
Le premier principe de la thermodynamique
12. Détente isotherme d'un gaz parfait. 13. Enthalpie en fonction de T à V constant. 14. Détente adiabatique irréversible et réversible. |
|
Transformation adiabatique dun gaz parfait
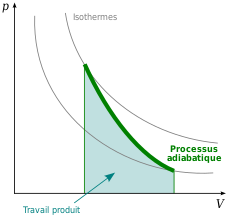
cessus isotherme). Au cours d'une compression adiabatique du travail s'effec- tue sur le gaz si bien que son ´energie interne augmente et que sa temp´ |
|
Chapitre VIII. Les diagrammes thermodynamiques
VIII.1.3 : Représentation des isothermes et adiabatiques réversibles : Les isothermes sont représentées par des courbes d'équation P.V = cte ou. P = Cte /V. |
|
THERMODYNAMIQUE
TRANSFORMATION ISOTHERME : elle se fait à température constante T = Cte. •. TRANSFORMATION ADIABATIQUE : elle se fait sans échange de chaleur avec. |
|
Cycles thermodynamiques des machines thermiques
18 jan. 2011 III.5.2 Compression isotherme avec transvasement . ... isothermes réversibles et de deux courbes adiabatiques réversibles. |
|
Exercice 1 Exercice 2 Exercice 4
1) Calculer le travail fourni par la détente isotherme d'une mole d'un gaz parfait de façon adiabatique et réversible jusqu'à la pression P0. |
|
Résumé de la thermodynamique
15 fév. 2012 2.9 Gaz parfait : processus adiabatiques ou isothermes . ... Chaque isotherme correspond `a une température donnée mais l'attribution d'une. |
|
Cours n° 3 : Les 4 transformations thermodynamiques de base. Le
transformation isotherme : la température du système reste constante lors de la transformation. • transformation adiabatique : aucune chaleur n'est échangée |
|
TD4 – Premier principe de la thermodynamique 2012
On réalise la compression isotherme d'une mole de gaz parfait contenu Or Q = 0 car les parois sont athermanes la transformation est donc adiabatique. |
|
Le Son et la Thermodynamique
Propagation dans un gaz parfait - Cas adiabatique. Dans le cas adiabatique l'équation d'état est donnée par Distinction des cas isotherme - adiabatique. |
|
Transformation adiabatique dun gaz parfait
isotherme) Au cours d'une compression adiabatique, du travail s'effec- tue sur le gaz si bien que |
|
THERMODYNAMIQUE
RMATION ISOTHERME : elle se fait à température constante T = Cte • TRANSFORMATION ADIABATIQUE : elle se fait sans échange de chaleur avec l' extérieur Q = 0 1 3 |
|
Chapitre 13 : Transformations réversibles dun gaz parfait
rmation adiabatique réversible en partant de l'état initial TVp ,, La pression extérieure est 3 – Transformations isothermes réversibles d'un gaz parfait a) Transformation |
|
Le premier principe de la thermodynamique
e isotherme d'un gaz parfait 13 Enthalpie en fonction de T à V constant 14 Détente adiabatique |
|
Chapitre VIII Les diagrammes thermodynamiques
3 : Représentation des isothermes et adiabatiques réversibles : la transformation adiabatique Q |
|
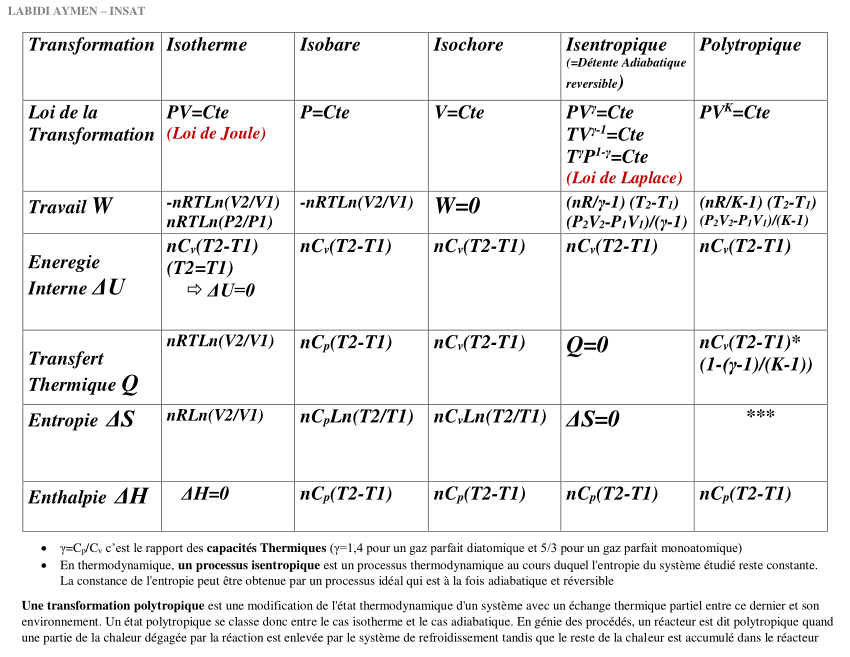
Thermodynamique
rmation réversibles gaz parfait ∆S Adiabatique 0 Isocore Isobare Isotherme nR −1 ln T f |
|
ELEMENTS DE THERMODYNAMIQUE ET THERMIQUE I
Cité 12 fois — pour une transformation isotherme et Cpoly→0 pour un transformation adiabatique) En pratique, la |
|
Le Son et la Thermodynamique
rmnPDF |
|
TD4 – Premier principe de la thermodynamique - Sayede Adlane
lise la compression isotherme d'une mole de gaz parfait contenu dans un cylindre de section S Or Q = 0 car les parois sont athermanes, la transformation est donc adiabatique |