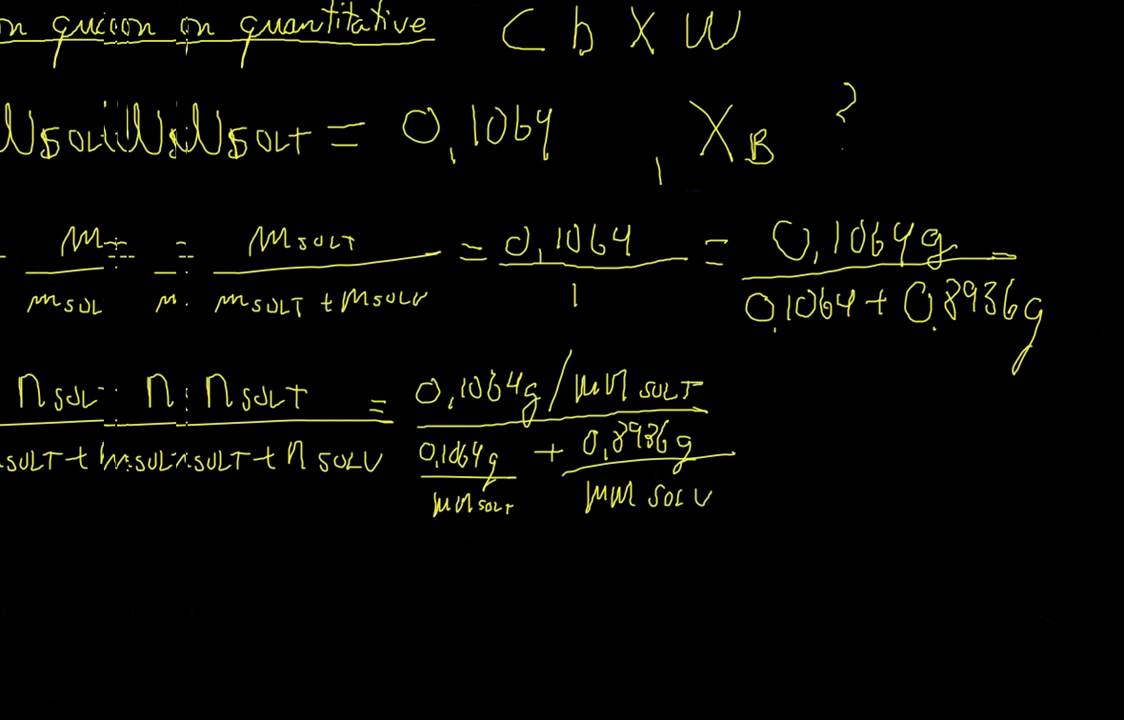exercice de molarité et normalité
|
Cours et exercices de chimie des solutions
La molarité ou concentration molaire d'une solution est le nombre de moles d'un soluté contenu dans l'unité de volume de la solution xi = = avec = 1 wi = = |
|
Partie 2
Exercice 1 a) Donner la définition de Molarité Molalité et Fraction Molaire (pour une solution avec une seule espèce dans un solvant) |
|
Définitions : MOLARITE : Cest le nombre de moles dun
Exercice N°1 a)- Définitions : MOLARITE : C'est le nombre de moles d'une substance molarité est égale à la normalité car X=1 c- La Normalité: N= neq / V |
|
Les solutions : pourcentage massique molarité normalité molalité
Les solutions : pourcentage massique molarité normalité molalité 1- Calculer le pourcentage massique d'une solution d'acide sulfurique H2SO4 qui contient |
|
Les solutions : pourcentage massique molarité normalité molalité
Les solutions : pourcentage massique molarité normalité molalité 1- Calculer le pourcentage massique d'une solution d'acide sulfurique H2SO4 qui contient |
|
TD-chimie-generale-et-organiquepdf
Déterminer: 1- La molarité et la molalité de la solution? 2- La normalité? 3- Combien faut-il prendre de ml de cette solution pour préparer 5 1 d |
Quelle est la relation entre la concentration et la normalité ?
La concentration équivalente est une unité de mesure chimique.
Elle est également appelée normalité. À présent désuète et éclipsée par la molarité, la normalité peut encore se trouver employée alors que le Système international de mesure est la mole, avec son dérivé pour les concentrations : la mole par litre.Comment calculer la molarité et la normalité ?
Dans le premier, vous utiliserez la formule N = b(n), dans laquelle b est la molarité et n le nombre de moles d'hydrogène ou d'hydroxyde.
Dans le second cas, il faudra utiliser une autre formule : N = éq ÷ V, dans laquelle éq est le nombre d'équivalents-grammes et V le volume de la solution.Équation : La molalité (��)
La molalité étant calculée en divisant la quantité de matière de soluté en moles par la masse de solvant en kilogrammes, l'unité de molalité sera donc mol/kg, mol⋅kg−1, ou simplement �� .
|
EXERCICES DE CHIMIE GÉNÉRALE
Exercice 1 a) Donner la définition de Molarité Molalité et Fraction Molaire (pour une solution avec une seule espèce dans un solvant). |
|
Cours et exercices de chimie des solutions
Exercice 2. Calculer (a) le titre pondérale (b) la molarité (c) la normalité (d) la molalité (e) les fractions molaires (f) les fractions massiques d'une |
|
Travail dirigé 5 : La concentration dune solution
Exercices : 1. On mélange deux volumes différents de solutions dont la teneur respective en glucose vaut. 7g/L. Que devient la concentration massique de |
|
Année 2020-2021 LE CORRIGEE TYPE DE LA SERIE I (TD01
Exercice N°1 a- La quantité de matière de KOH : (n) = masse KOH / masse molaire KOH. nKOH= 12g /56 (g/mol) =0 21 mol b- La Molarité (M) : M = n KOH |
|
Td corriges biochmv 2014-2015.pdf
EXERCICE 2 : Avant de réaliser une manipulation de Biochimie vous devez préparer les Sa molarité est x et sa normalité ... Sa molarité (M) est y et sa. |
|
C.C/ Dj.Taharchaouche Institut dHygiène et Sécurité Département
15 déc. 2020 Exercice 1 : On fait dissoudre 12g de KOH dans 250ml d'eau. 1- Calculer le nombre de mole de KOH dissoute la molarité |
|
Structure de la matière
dissoute la molarité |
|
1 CHIMIE II Chapitre I : les solutions
Calculer le pourcentage massique de CaCl2 et de H2O. 4- Calculer la normalité et la molarité de H3PO4 : 60% de masse d=1 |
|
EXERCICES DE CHIMIE GÉNÉRALE
Exercice 1 a) Donner la définition de Molarité, Molalité et Fraction Molaire (pour une solution avec une seule espèce dans un solvant) b) On a une solution |
|
Corrigé de la série 1_2012
MH3PO4 est la masse molaire de H3PO4 égale à 98 g/mol La relation qui lie la molarité et la normalité est : p N C = Où p est le nombre d'équivalent mis en |
|
Molarité, molalité - e-fisio
Une solution qui contient une mole par kg d'eau est une solution molale exercice 2 : osmolarité, coefficient osmotique a) Qu'est-ce l'osmolarité d'une solution ? |
|
Les solutions : pourcentage massique, molarité, normalité, molalité
Les solutions : pourcentage massique, molarité, normalité, molalité 1- Calculer le pourcentage massique d'une solution d'acide sulfurique H2SO4 qui contient |
|
Les solutions - Editions Ellipses
(molarité), [ ] ou C mol L-1 nombre de moles de composé dissous dans un litre de solution, mol L-1 ≡ mol dm-3 ≡ M concentration massique ou pondérale, Cm |
|
Cours et exercice chimie des solution Mr hebbar nordinepdf
Exercice 2 Calculer (a) le titre pondérale (b) la molarité (c) la normalité (d) la molalité (e) les fractions molaires (f) les fractions massiques d'une solution d' acide |
|
Travail dirigé 5 : La concentration dune solution - Unité AFO
Exercices : 1 Quelle est la molarité d'une solution de H3PO4 préparée en diluant 10 mL d'acide concentré 15 M 1°/ Molarité ou Concentration molaire C |
|
Solution Des Exercices
Masse d'ammoniac : L'avancement maximal est atteint lorsque tout le diazote est consommé, dans ce cas xmax = 5,0 103 mol Chaque heure la masse |
|
Filière Sciences de la Matière Chimie Cours Chimie des Solutions
La normalité est liée à la molarité par l'équation : Exercice On considère une solution d'acide faible de concentration initiale C0, et de constante d'acidité Ka |