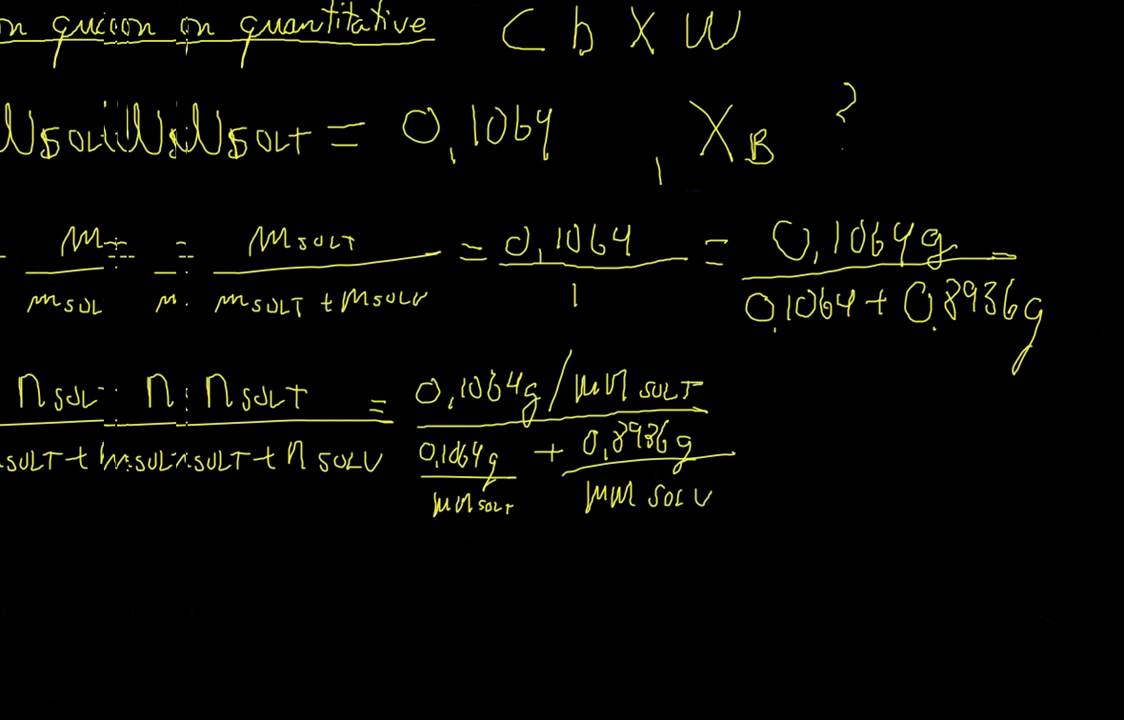exercices corrigés sur la normalité et la molarité
|
Les solutions : pourcentage massique molarité normalité molalité
: Cu = 635 ; S = 32 ; O = 16 ; N = 14 ; H = 1 9- Calculer la normalité de l'acide phosphorique qui contient : a- 98 g de soluté par 500 mL de solution |
|
Les solutions : pourcentage massique molarité normalité molalité
: Cu = 635 ; S = 32 ; O = 16 ; N = 14 ; H = 1 9- Calculer la normalité de l'acide phosphorique qui contient : a- 98 g de soluté par 500 mL de solution |
|
Partie 2
Exercice 2 On dissout 1 05 g d'un composé inconnu (non-électrolyte) dans 100g de CCl4 Le point d'ébullition normal de la solution est abaissé de 0 31 K par |
|
Cours et exercices de chimie des solutions
La normalité ou concentration équivalente d'une solution est le nombre d'équivalent gramme 6- Chimie MPSI ; cours méthode et exercices corrigés ; Le nouveau |
|
Cours et exercices de chimie des solutions
On utilise parfois la notion de normalité pour simplifier les calcules lors des problèmes 6- Chimie MPSI ; cours méthode et exercices corrigés ; Le nouveau |
Comment on calcule la normalité ?
Pour calculer simplement la quantité ou le poids d'une substance nécessaire pour une solution normale souhaitée, la formule suivante peut être utilisée : Poids en grammes = normalité souhaitée x volume nécessaire en litres x PMG/valence (W = N x V x PMg/valence).
Donc la solution de KMnO4 dont la concentration est connue n'a pas une normalité assurée.
Si on travaille en milieu acide, la demi-équation est : MnO4^ + 8 H+ + 5 e- --> Mn2+ + 4 H2O.
Donc une solution de KMnO4 0.
1) M est 0.
5) N en milieu acide, 0.
3) N en milieu neutre et 0.
1) N en milieu basique.
Quelle est la relation entre la concentration et la normalité ?
La concentration équivalente est une unité de mesure chimique.
Elle est également appelée normalité. À présent désuète et éclipsée par la molarité, la normalité peut encore se trouver employée alors que le Système international de mesure est la mole, avec son dérivé pour les concentrations : la mole par litre.
|
Année 2020-2021 LE CORRIGEE TYPE DE LA SERIE I (TD01
Exercice N°1 a- La quantité de matière de KOH : (n) = masse KOH / masse molaire KOH. nKOH= 12g /56 (g/mol) =0 21 mol b- La Molarité (M) : M = n KOH |
|
EXERCICES DE CHIMIE GÉNÉRALE
Exercice 1 a) Donner la définition de Molarité Molalité et Fraction Molaire (pour une solution avec une seule espèce dans un solvant). |
|
Cours et exercices de chimie des solutions
Relation entre la normalité et la molarité 6- Chimie MPSI ; cours méthode et exercices corrigés ; Le nouveau précis Bréal. |
|
Td corriges biochmv 2014-2015.pdf
EXERCICE 2 : Avant de réaliser une manipulation de Biochimie vous devez préparer les Sa molarité est x et sa normalité ... Sa molarité (M) est y et sa. |
|
TRAVAUX DIRIGES CHIMIE ANALYTIQUE
Combien faut-il prendre de ml de cette solution pour préparer 5 L d'une solution de normalité 010 N. Exercice 02 : Calculer la masse de soluté nécessaire à la |
|
Travail dirigé 5 : La concentration dune solution
Exercices : 1. On mélange deux volumes différents de solutions dont la teneur respective en glucose vaut. 7g/L. Que devient la concentration massique de |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
d'électrons susceptibles d'être libérés par un litre de solution. La normalité est liée à la molarité par l'équation : N=P×M. N : Normalité ;. |
|
TP CHIMIE-1 & TP CHIMIE-2
effectué la détermination par dosage de la normalité la molarité et la concentration pondérale d'une solution de NaOH inconnue. |
|
EXERCICES DE CHIMIE GÉNÉRALE
r la Molarité, Molalité et Fraction Molaire de HCl dans cette solution Exercice 2 On dissout 1 05 g |
|
Les solutions : pourcentage massique, molarité, normalité
utions : pourcentage massique, molarité, normalité, molalité 1- Calculer Corrigé de la série 1 |
|
TD + corrigés BiochMV 2014-2015 - Le site BioInteractif est en
alité N d'une solution acide est le nombre de moles d'ions H+ Sa molarité (M) est y et sa EXERCICE 2 : Calculer le pH d'une solution 0,1 mol/L d' acide butyrique dont le Ka |
|
Molarité, molalité - e-fisio
rité est la concentration exprimée en moles par litre de solution Une solution qui b) On rajoute à la solution de NaCl précédente (exercice 2 c) ( 600 mg d'urée (PM = 60) |
|
Cours et exercices de chimie des solutions
t exercices de chimie des solutions Relation entre la normalité et la molarité ⇒ Remarque: 6- Chimie MPSI ; cours, méthode et exercices corrigés ; Le nouveau précis Bréal |
|
Travail dirigé 5 : La concentration dune solution - Unité AFO
es : 1 Quelle est la molarité d'une solution de H3PO4 préparée en diluant 10 mL d'acide |
|
Solution Des Exercices
'ammoniac : L'avancement maximal est atteint lorsque tout le diazote est consommé, dans ce |