exercice sur la loi des gaz parfaits
|
Gaz parfaits et Thermodynamique – Exercices – Devoirs
Gaz parfaits et Thermodynamique – Exercices – Devoirs Exercice 1 corrigé disponible 5 Lorsqu’un système de masse m échange de la chaleur avec le milieu extérieur sans changement d’état sa température peut varier de T1 à T2 selon la loi : T a 2−T Q= 1 mc b Q= mc T 2−T 1 c Q=mc (T2−T1) d |
Quelle est la valeur de la constante des gaz parfaits ?
V est le volume de gaz en mètres cubes (m³). n est la quantité de substance en moles (mol). R est la constante des gaz parfaits, qui a une valeur de 8,314 J/ (mol·K). T est la température absolue en kelvin (K).
Comment calculer le produit d’un gaz parfait ?
Pour un gaz parfait, le produit P.V ne dépend que de la température P.V = f (T). La relation précédente à température constante peut s’écrit P = Cte/ V , ce qui conduit à un second énoncé de la loi de MARIOTTE Seconde forme de la loi de MARIOTTE.
Qu'est-ce que la loi des gaz parfaits ?
La loi des gaz parfaits est une relation mathématique qui décrit le comportement des gaz lorsqu'ils sont dans des conditions idéales. Cette loi établit qu'à température et quantité de gaz constantes, la pression (P) d'un gaz est directement proportionnelle à son volume (V) et inversement proportionnelle à sa température absolue (T).
Comment calculer le volume d’un gaz parfait ?
Loi de GAY-LUSSAC. A pression constante, l’augmentation de volume d’un gaz parfait (dilatation ou détente) est proportionnelle à la température absolue. V/T = Cte Ou V=Cte.T loi de GAY-LUSSAC. Si on considère deux états différents d’une même masse gazeuse à la même pression avec : T 1 et V 1 température et volume à l’état (1).
définition
Un gaz parfait est un fluide idéal qui satisfait à l’équation d’état p.v=n.RT, ou encore c’est un gaz qui obéit rigoureusement aux trois lois. MARIOTTE, GAY .LUSSAC et CHARLES. On désigne par ‘v’ le volume d’une unité de masse, de gaz parfait et par ‘Vm’ le volume molaire d’un gaz parfait avec : 1 mole =6,023.1023 Molécules = A (nombre d’Avogadro)
Loi de Mariotte.
A température constante, le produit de la pression d’une masse gazeuse par son volume est constant (cette loi est d’origine expérimentale) Sous faibles pressions, tous les gaz se comportent de la même manière quelque soit leur nature. Par définition, un gaz parfait sera un gaz pour lequel, P.V = Cte loi de MARIOTTE. Pour un gaz parfait, le produit
Loi de Gay-Lussac.
A pression constante, l’augmentation de volume d’un gaz parfait (dilatation ou détente) est proportionnelle à la température absolue. V/T = Cte Ou V=Cte.T loi de GAY-LUSSAC. Si on considère deux états différents d’une même masse gazeuse à la même pression avec : 1. T1 et V1température et volume à l’état (1). 2. T2 et V2 température et volume à l’ét
Loi de Charles (ou 2eme Loi de Gay-Lussac).
A volume constant, l’augmentation de pression d’un gaz parfait est proportionnelle à l’élévation de la température. On a : P/T = Cte Si on considère deux états différents d’une même masse gazeuse dans lesquelles elle occupe le même volume. La pression et la température sont : 1. P1 et T1pression et température à l’état (1). 2. P2 et T2pression et t
Caractéristiques d’un Gaz Parfait
On recherche l’équation qui lie les paramètres d’état (p, v,T). On considère une (U.D.M) d’un gaz parfait dans deux états différents : 1. Etat (1) : (P, V, T) 2. Etat (2) : (P’, V’, T’) Imaginons un 3èmeétat où la pression est P, la température est T’. Etat (3) : (P, V’’, T’). On passe à pression constante de l’état (1) à l’état (3), on a donc en v
Mélange Des Gaz Parfaits
On considère un mélange de gaz chimiquement inerte (mélange qui ne donne pas lieu à une réaction chimique). Soit V, le volume occupé par le mélange. Chaque gaz occupe le volume V comme s’il été seul sous une pression Piappelée pression partielle. La pression du mélange est égale à la somme des pressions partielles des gaz composants. Mélange de 2 g
Exercices Corrigés Sur Les Gaz Parfaits
On donne R = 8,31 SI. 1) Quelle est l’équation d’état de n moles d’un gaz parfait dans l’état P, V, T ? En déduire l’unité de R. 2) Calculer numériquement la valeur du volume molaire d’un gaz parfait à une pression de 1 bar et une température de 0°C. On donne 1 bar = 105Pa. 1 – L’équation d’état d’un gaz parfait est : PV = nRT. On en déduit que R=P

La loi des gaz parfaits

Application du Premier Principe aux transformations gaz parfait

Loi des gaz parfaits : Exemple 2
|
Santé
Mélange de gaz parfaits – Loi de Dalton (1801). La pression totale exercée par un mélange de gaz parfaits est égale à la somme des. |
|
EXERCICES DE CHIMIE GÉNÉRALE
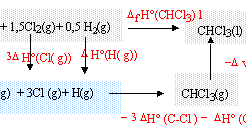
Utiliser la loi du gaz parfait. Exercice 4. Considérer l'explosion de 23.4g de nitroglycérine à 25°C: 4 C3H5(NO3)3(l) |
|
Terminale générale - Gaz parfaits et thermodynamique - Exercices
la loi : a. Q= T2?T1 mc b. Q= mc. T2?T1 c. Q=mc(T2?T1) d. Q=mc(T1?T2). Exercice 2 corrigé disponible. Exercice 3 corrigé disponible. 1/7. Gaz parfaits |
|
«EXERCICES ET PROBLEMES CORRIGES DE
Exercices et problèmes corrigés de thermodynamique chimique. 11. CHAPITRE I. LOI DES GAZ PARFAITS ET LE PREMIER. PRINCIPE DE LA THERMODYNAMIQUE |
|
Révision Stœchiométrie et Gaz parfaits
Etre capable de résoudre des problèmes faisant intervenir la stœchiométrie et la loi des gaz parfaits. ————————————————————————. Exercices. Exercice 1. |
|
Série de TD n°01 Thermodynamique
Exercice 2. 1. Citer les lois des gaz parfaits. 2. Un cylindre contient 765 mL de gaz de propane à la pression de 125·105 Pa. Quel serait le. |
|
Chapitre 13 : Les gaz parfaits
Loi des gaz parfaits : P×V = n×R×T. 3) Exercices d'application : a. Un récipient de 200 L contient 1 |
|
La loi des gaz parfaits
Loi des gaz. Exercices. AdM. 1. La loi des gaz parfaits. 1. a) A la surface de Vénusla pression atmosphérique est de 75 atm. Transformer cette pression. |
|
Exercices sur les gaz parfaits (chapitre 4)
Données pour tous les exercices: Constante des gaz parfaits R = 8314 Donner l'équation d'état d'un gaz parfait en indiquant le nom et l'unité de chaque ... |
|
Exercices Comment faire varier la température dun gaz sans le
Loi des gaz parfaits pour une mole : pV = RT. (D'après sujet de Bac Pro PSPA Session juin 2003). Exercice 6. L'isobutane ou R600a est un fluide frigorigène |
|
EXERCICES DE CHIMIE GÉNÉRALE
EXERCICES DE CHIMIE GÉNÉRALE Un pneu (volume constant, rempli d'un gaz parfait) est chauffé jusqu'à ce que la pression Utiliser la loi du gaz parfait |
|
Les gaz parfaits - Physagreg
Loi des gaz parfaits : P×V = n×R×T 3) Exercices d'application : a Un récipient de 20,0 L contient 1,7 mol de gaz On désire que la pression du gaz soit égale à |
|
Exercices sur les gaz parfaits - [Physiqueenstifreefr]
Données pour tous les exercices: Constante des gaz parfaits R = 8,314 J·K–1· mol–1 Donner l'équation d'état d'un gaz parfait en indiquant le nom et l'unité de |
|
CINFORMELLE_exercice13 - Exercices : corrigé
Le diazote est le seul gaz, c'est un gaz parfait alors à t : « pV= nRT » s'écrit pV= ξRT Ainsi si la température et la pression sont constantes, le volume V est bien |
|
Exercice 2 Etude dun mélange de gaz parfaits
Exercice 2 Etude d'un mélange de gaz parfaits Mélange initial pour l'ensemble des 2 expériences : Un mélange gazeux est constitué de diazote N2 et de |
|
Exercices PP349-357
Exercices 7 5 min chrono Si vous ne trouvez pas la bonne réponse, reportez- vous auß Utiliser la loi du gaz parfait et les unités Si dans le calcul |
|
La loi des gaz parfaits
Loi des gaz Exercices AdM 1 La loi des gaz parfaits 1 a) A la surface de Vénus,la pression atmosphérique est de 75 atm Transformer cette pression en torrs |
|
Quest-ce quun gaz parfait - Dunod
Mélange de gaz parfaits – Loi de Dalton (1801) Exercices Le récipient (1) contient du diazote à la pression P1 = 1,5 bar et à la température u1 = 15 ◦ |
|
Gaz parfait
2) Valeur du volume molaire 3) Exercice Déterminer le volume molaire des gaz si la pression est de 1013 hPa et la température 20,0 °C V) LOI DE MARIOTTE |



















![PDF] Exercices corrigés sur le gradateur triphasé en PDF PDF] Exercices corrigés sur le gradateur triphasé en PDF](https://cdn.pass-education.fr/wp-content/uploads/images-posts/181576-thumb-plus-que-parfait-cm2-bilan-a-imprimer.jpg)