Cas d'un cide fort Bac Chimie
|
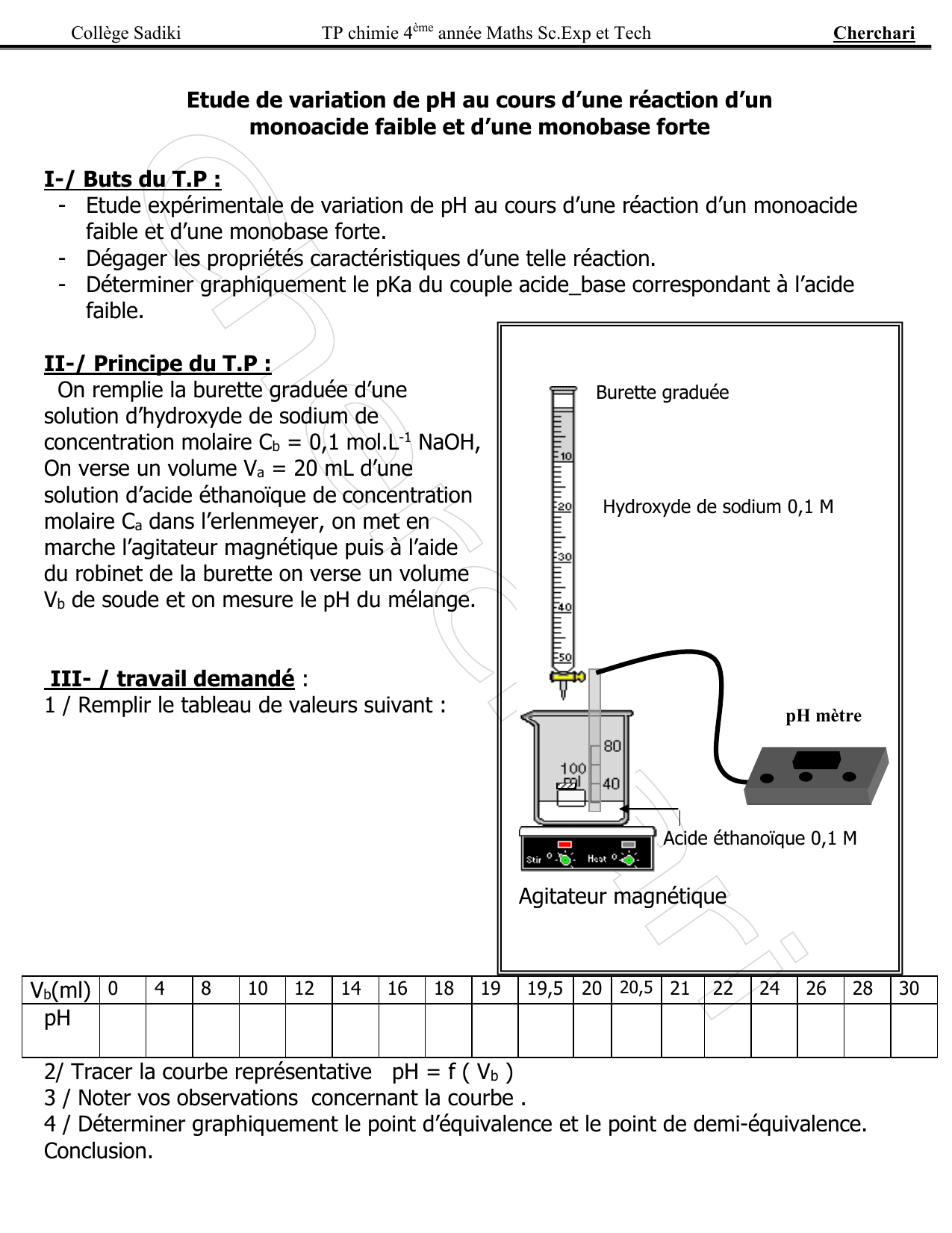
Fiche de révisions sur les acides et les bases
acide: espèce chimique capable de libérer un (ou plusieurs) proton (s) base: espèce chimique capable de capter un (ou plusieurs) proton (s) Attention ! solution acide ≠ acide Dans une solution acide : [H3 O+]>[OH −] acide fort: c’est un acide qui réagit entièrement avec l’eau |
Quels sont les acides forts en chimie ?
Les acides forts sont complètement dissociés, de sorte qu'il y a beaucoup d' ions oxonium dans la solution. Plus il y a d' ions oxonium dans une solution, plus le pH est bas. L' acide chlorhydrique H C l , l' acide nitrique et l' acide sulfurique sont des exemples d' acides forts en chimie.
Quels sont les exercices corrigés de bac physique chimie ?
Lunette astronomique, satellites, diffraction. Corrections disponibles. Plus de 800 Exercices corrigés de bac physique chimie, classés par thème, centre d'examen et année, des QCM pour réviser tout au long de l'année.
Quels sont les différents types d’acides forts ?
Il n’y a que quelques acides forts, mais beaucoup d’acides faibles. Les acides forts se dissocient complètement dans l’eau en leurs ions et produisent un ou plusieurs protons ou cations hydrogène par molécules. Les acides minéraux ou inorganiques ont tendance à être des acides forts. Il n’existe que 7 acides forts courants.
Comment se dissocier d'un acide fort?
Un acide fort va toujours se dissocier en libérant une grande quantité d'ion hydronium ce qui va avoir pour conséquence de baisser le pH d'une solution. Par définition, plus une solution contient des ions hydroniums, plus elle est acide.
|
Chapitre 1 Acides et bases
Dans le cas d'un acide fort totalement dissocié dans l'eau |
|
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
EXERCICE 2 – UN EXEMPLE DE CHIMIE VERTE : LA SYNTHÈSE DE L'IBUPROFÈNE. ACCÈS CORRECTION À quel couple acide/base appartient l'ion hydroxyde HO– ? |
|
PHYSIQUE-CHIMIE- TECHNOLOGIE
S.A.2 : CHIMIE DES SOLUTIONS AQUEUSES. ANNEXES DE LA S.A.2 Cas particulier des acides forts et des bases fortes ... Collection Union Bac. |
|
Corrigé du bac 2016 : Physique- Chimie Spécialité Série S
Dans le cas de l'acide fumarique les liaisons ne peuvent pas être intramoléculaires |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
CALCUL DE PH DES SOLUTIONS AQUEUSES. 2.1. Cas d'un acide fort. 2.2. Cas d'un acide faible. 2.3. Cas d'une base forte. 2.4. |
|
Corrigé du bac Spécialité Physique-Chimie 2022 - Polynésie 2
8 may. 2022 Exercice 1 — Le sel d'oseille. 1. Première hypothèse : l'acide oxalique est un diacide fort. 1.1. Selon Brönsted un acide est une espèce ... |
|
ANNALES SCIENCES PHYSIQUES Terminale D
Chapitre 6 : L'étude de la réaction entre un acide faible et une base Mécanique Physique nucléaire |
|
Sujet du bac Spécialité Physique-Chimie 2022 - Polynésie 2
Première hypothèse : l'acide oxalique est un diacide fort. Données : En déduire que dans le cas de l'hypothèse précédente |
|
Filière Sciences de la Matière Chimie Cours Chimie des Solutions
Cas d'un mélange d'un acide fort et d'un acide faible. 2.6. Cas d'un mélange de deux acides faibles. 3. Solutions tampon. 3.1. Définition de la ST. |
|
Analyse didactique du programme de chimie au Baccalauréat
Baccalauréat Marocain: Cas de l'évolution des systèmes chimiques. Ali Ouasri chimie au Baccalauréat Marocain en termes de rapports didactiques entre. |
Comment justifier que c'est un acide fort ?
. Un acide A appartenant à un couple acide-base de pKa positif ne sera que partiellement transformé en ions H3O+ : on dit qu'il s'agit alors d'un acide faible.
Quand un acide est dit fort ?
Quels sont les acides forts en chimie ?
Comment savoir quel est l'acide le plus fort ?
|
Chapitre 1 Acides et bases
Dans le cas d'un acide fort, totalement dissocié dans l'eau, la concentration finale ABC du BAC, Physique-Chimie spécifique et spécialité, Ed Nathan (2013) |
|
Révisions sur les acides et les bases - Nicole Cortial
donc la base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et 14 10 |
|
Sujet officiel complet du bac S Physique-Chimie - Sujet de bac
Ce sujet comporte deux exercices de PHYSIQUE et un exercice de CHIMIE Donner l'expression de la constante d'acidité KA du couple acide lactique / ion dans ce cas, l'équation horaire du mouvement du centre d'inertie G du boulet est |
|
PHYSIQUE-CHIMIE - TEL archives ouvertes
S A 2 : CHIMIE DES SOLUTIONS AQUEUSES ANNEXES DE LA S A 2 Cas particulier des acides forts et des bases fortes Collection Union Bac Terminales |
|
Les acides et les bases Corrigés des exercices
OS Chimie - Corrigé Acides-Bases Mais, en pratique, H2SO4 est un acide tellement fort qu'on doit considérer sa ce cas précis, il n'y aura pas de réaction |
|
Exercice de révision pour le bac : chimie Contrôle de la qualité par dos
Exercice de révision pour le bac : chimie Contrôle de la On admettra que l' acidité du lait est uniquement due à l'acide lactique 1 18°D, ce qui est le cas ici |
|
SPC annales zro sujet 2 lments de correction - mediaeduscol
Baccalauréat général - Épreuve obligatoire de physique-chimie série S- Exemple de sujet spécifique Pour une solution d'acide fort, pH = - log c donc ici : |
|
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
EXERCICE 2 – UN EXEMPLE DE CHIMIE VERTE : LA SYNTHÈSE DE L' limpide très peu coloré en vert pâle, 4 mL d'acide sulfurique incolore et 1 mL La « neutralisation ›› au dioxyde de carbone s'impose dans la plupart des cas comme la solution la En conséquence, plus le pH du lait est faible et moins il est frais |
|
Terminale générale - Réactions Acido-basiques - Physique et Maths
Préciser dans chacun des 2 couples la forme acide et la forme basique 2 COMPORTEMENT DE HA EN Physique – Chimie Terminale générale - Année scolaire 2020/2021 Il s'agit d'un acide fort, la variation du pH sera rapide et fluctuations Dans le cas contraire, de fortes fluctuations nuiraient gravement à la santé |
|
Corrigé- Série 2- Travaux dirigés de Chimie des Solutions
(a) HCl est un acide fort (pKa < 0) Ca = 0,01 M : La solution est suffisamment concentrée (b) De même dans le cas de l'acide formique, qui est un acide faible : |