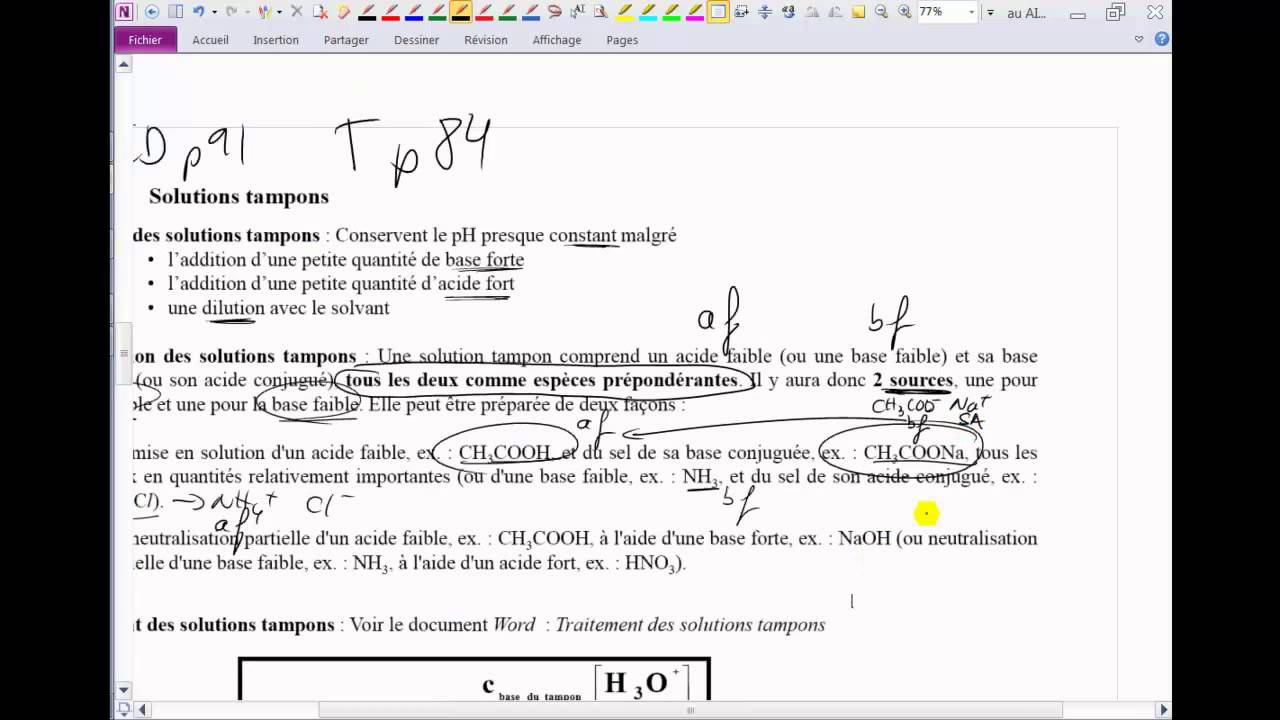
solution tampon exercice corrigé
|
(exercice 2 solution tampon énoncé et correction)
Exercice : Donnée Conclusion: De l'acide a été ajouté à la solution le pH est passé de 92 à 90 il a donc peu varié : il s'agit d'une solution tampon |
|
Chimie Exercice I: solution tampon (7 points) Un flacon contient de
Un flacon contient des cristaux solides de chloure d'ammonium: NH4Cl Données : on dispose du matériel suivant :-flacon contenant des cristaux de chlorure |
|
Corrigé
Exercice 3 : On prépare une solution tampon de pH = 45 à partir d'acide acétique CH3COOH (pKa = 48) et d'acétate de potassium CH3COOK (1) Calculer le |
|
CORRIGE
Exercice 01 : (10 pts) 1- L'ammoniac est une base faible dans l'eau 7- En principe une solution tampon a un pH qui varie très peu par ajout modéré d'un |
|
EPREUVE DEXERCICES DAPPLICATION
Comment préparer 1 litre de solution tampon 04 M de pH 55 à 25° C avec de l'acétate de sodium CH3 COONa 3 H2O et de l'acide acétique pKa de l'acide |
Comment déterminer la solution tampon ?
Dans une solution tampon, la valeur du pH est égale à la valeur du pKA du couple : pH = pKA.
On dispose d'une solution constituée par le couple acide éthanoïque/ion éthanoate CH3COOH / CH3COO–.
Dans cette solution, on a 0,10 mol/L.Quel est le pKa du couple CH3COOH ch3cook ?
Le pKa du couple CH3COOH / CH3COO– vaut 4,8 à 25◦C.
Quel est le rôle de la solution tampon ?
Une solution tampon est un mélange d'acide faible et de sa base conjuguée ou d'une base faible et de son acide conjugué.
On utilise des solutions tampons pour maintenir stable la valeur du pH d'une autre solution mélangée avec le tampon.- De quelle valeur est proche le pH d'une solution tampon ? Il est neutre, pH = 7.
Il est acide, pH = 5.
|
CORRIGE
Exercice 01 : (10 pts). 1- L'ammoniac est une base faible dans l'eau 7- En principe une solution tampon a un pH qui varie très peu par ajout modéré d'un. |
|
Exercice 2 solution tampon énoncé et correction.pdf
On ajoute à cette solution 00200 mol d'acide nitreux HNO2 |
|
2atp
13 févr. 2020 Exercice 2: On prépare 500mL à l'aide d'ion formate (HCOO-) et d'H3. O+ une solution tampon de pH = 41. Dans cette solution on a introduit 0 ... |
|
2010/2011 Matière : Chimie Exercice I: solution tampon (7 points
L'usage d'une calculatrice non programmable est autorisé. Exercice I: solution tampon (7 points). Un flacon contient des cristaux solides de chloure d |
|
Corrigé- Série 2- Travaux dirigés de Chimie des Solutions
Exercice 3 : On prépare une solution tampon de pH = 45 à partir d'acide acétique CH3COOH (pKa = 4 |
|
Untitled
EPREUVE D'EXERCICE D'APPLICATION. Exercice N° 1 (40 points). Comment préparer 250 mL de tampon B phosphorique 010 M par simple dilution de la solution de |
|
Mai 2012 Exercice 1 Enoncé : Pour tous les tests choisir un risque
Comment préparer 1 litre de solution tampon 04 M de pH 5 |
|
2011- ZONE NORD PROPOSITION DE REPONSES Exercice 4 1
Exercice 4 (suite). 2) HCOO. – est formé stoechiométriquement par l'addition de KOH Le pH est de 475 |
|
F2School
Calculez la concentration nécessaire de NaHCO3 pour avoir une solution tampon à pH = 65. Réponse : Le couple acide / base conjuguée est : H2CO3 / HCO3. – (pKa |
|
Corrigé du baccalauréat STL spécialité biotechnologies Métropole
18 juin 2019 EXERCICE 1. (5 points). Dans une solution tampon (solution dont le pH varie peu ou ne varie pas lors de l'ajout d'un acide ou d'une base ... |
|
CORRIGE
CORRIGE. Exercice 01 : (10 pts). 1- L'ammoniac est une base faible dans l'eau On obtient alors une solution tampon dont les concentrations sont (si les ... |
|
Td corriges biochmv 2014-2015.pdf
EXERCICE 2 : Calculer le pH d'une solution 01 mol/L d'acide butyrique dont le b) On prépare ensuite une solution tampon acétate en dissolvant dans 1 L ... |
|
Corrigé- Série 2- Travaux dirigés de Chimie des Solutions
Exercice 3 : On prépare une solution tampon de pH = 45 à partir d'acide acétique CH3COOH (pKa = 4 |
|
(exercice 2 solution tampon énoncé et correction)
Exercice : Donnée : pKa( NH4. +/NH3)=92. On dispose de 100 mL d'une solution contenant 0 |
|
HATIER prof
[H3O+]éq > [HO–]éq donc la solution est acide. Exercice 29 corrigé à la fin du manuel de l'élève. donc le pH de la solution tampon ainsi préparée est. |
|
2atp
13 févr. 2020 Quel est le rapport entre la concentration et la pouvoir tampon ? ... Exercice 1: Dans une solution A on met 250 mL contenant. |
|
2011- ZONE NORD PROPOSITION DE REPONSES Exercice 4 1
Exercice 4. 1) Pour préparer un tel tampon de pH = 350 |
|
F2School
Corrigés des exercices Acides-bases 14 : Calcul du pH des solutions d'un acide ou d'une base dans ... Acides-bases 18 : Les solutions tampons . |
|
SERIE 7 ET 8 : ACIDES ET BASES FAIBLES – SOLUTION TAMPON
Calculer la concentration Ca de cette solution. EXERCICE 6 : CALCUL DU pH D'UN ACIDE FAIBLE A PARTIR DU pKa ET DE SA CONCENTRATION Ca. |
|
Corrigé exercice 10 - LsACIDE ACÉTIQUE EN SOLUTION AQUEUSE
Une solution tampon possède les deux propriétés fondamentales suivantes : - avoir un pH qui varie peu si on ajoute des quantités modérées d'acide ou de base ;. |
|
CORRIGE
CORRIGE Exercice 01 : (10 pts) 1- L'ammoniac est une base faible dans l'eau On obtient alors une solution tampon dont les concentrations sont (si les |
|
Chimie Exercice I: solution tampon (7 points) Un flacon contient de
Cette épreuve est constituée de trois exercices Elle comporte trois pages numérotées de 1 à 3 L'usage d'une calculatrice non programmable est autorisé |
|
Solution tampon - Terminale - Exercices corrigés - PDF à imprimer
Exercice 01 : On souhaite préparer une solution tampon à Pour cela on prélève un volume d'une solution d'acide éthanoïque à la concentration On y |
|
Corrigé- Série 2- Travaux dirigés de Chimie des Solutions Aqueuses
Exercice 1 : (1) Calculer le pH des solutions suivantes : (a) Acide chlorhydrique HCl de concentration 10-2 M (pKa = -37) (b) 10 mL de HCl 10-5 M + 990 mL |
|
(exercice 2 solution tampon énoncé et correction)
Exercice : Donnée : pKa( NH4 +/NH3)=92 On dispose de 100 mL d'une solution contenant 0100 mol d'ammoniac NH3 et 0100 mol d'ion ammonium NH4 |
|
Ue11 chimie analytique 2atp
13 fév 2020 · Exercice 2: On prépare 500mL à l'aide d'ion formate (HCOO-) et d'H3 O+ une solution tampon de pH = 41 Dans cette solution on a introduit 02 |
|
EPREUVE DEXERCICES DAPPLICATION - Mai 2012
Enoncé et question: Comment préparer 1 litre de solution tampon 04 M de pH 55 à 25° C avec de l'acétate de sodium |
|
Corrigé exercice 7 - LsACIDE ACÉTIQUE EN SOLUTION AQUEUSE
Une solution tampon possède les deux propriétés fondamentales suivantes : - avoir un pH qui varie peu si on ajoute des quantités modérées d'acide ou de base ; |
|
Exercice I: solution tampon (7 points) - PDF Téléchargement Gratuit
Exercice I: solution tampon (7 points) Un flacon contient des cristaux solides de chloure d'ammonium: NH 4 Cl Données : on dispose du matériel suivant |
|
EXERCICES – SÉRIE 8 Acides polyprotiques solutions tampons
EXERCICES – SÉRIE 8 Acides polyprotiques solutions tampons courbes de titrage 8 1 Calculer la concentration en H+ d'une solution de H2S 0 10 M Les |
Comment préparer une solution tampon PDF ?
Dissoudre les solides dans environ 100 mL d'eau distillée. Agiter. Quand tout est dissous, ajuster au trait de jauge avec de l'eau distillée; homogénéiser. Cette solution constitue la solution tampon.Comment calculer la solution tampon ?
Dans une solution tampon, la valeur du pH est égale à la valeur du pKA du couple : pH = pKA. On dispose d'une solution constituée par le couple acide éthanoïque/ion éthanoate CH3COOH / CH3COO–. Dans cette solution, on a 0,10 mol/L. C'est donc une solution tampon.- * Prendre 50 ml de solution tampon pH = 9,3 dans un petit becher. Mesurer son pH. Ajouter 0,5 ml (burette) de solution 1 M d'acide chlorhydrique et mesurer le nouveau pH.
| Solutions tampons - Pouvoir tampon - Le Mans University |
| Les solutions tampons - Le Mans University |
| EXERCICES – SÉRIE 8 Acides polyprotiques solutions tampons |
| TP 10 : LES SOLUTIONS TAMPONS - fiskimcom |
| Exercice 1: Préparation d’une solution tampon - WebSelf |
| Searches related to solution tampon exercice corrigé filetype:pdf |
Quels sont les deux courbes d'un tampon?
- Pour le pouvoir tampon, deux courbes, correspondant aux relations approchée et exacte sont présentées.
|
Corrigé- Série 2- Travaux dirigés de Chimie des Solutions
Exercice 1 : (1) Calculer le pH des Corrigé : (a) HCl est un acide fort (pKa < 0) Ca = 0,01 M : La solution est suffisamment concentrée pour qu'on On prépare une solution tampon de pH = 4,5 à partir d'acide acétique CH3COOH (pKa = 4,8) |
|
EXERCICES – SÉRIE 8 Acides polyprotiques, solutions tampons
EXERCICES – SÉRIE 8 Acides polyprotiques, solutions tampons, courbes de titrage 8 1 addition de 5⋅10–5 mol de NaOH à 100 ml de solution tampon ? |
|
CORRIGE - essa-tlemcendz
CORRIGE Exercice 01 : (10 pts) 1- L'ammoniac est une base faible dans l'eau, elle On obtient alors une solution tampon, dont les concentrations sont (si les |
|
EPREUVE DEXERCICES DAPPLICATION - 2011- ZONE - CNCI
Exercice 4 1) Pour préparer un tel tampon de pH = 3,50, on ne pourra utiliser que le couple HCOOH / HCOO – K + soit x le nombre de mL de solution HCOOH |
|
Les acides et les bases Corrigés des exercices
Acides-bases 14 : Calcul du pH des solutions d'un acide ou d'une base dans l' eau 30 Soit une solution tampon d'acide carbonique 0,2 mol·L-1 avec de |
|
Solution tampon - AzureWebSitesnet
Exercice I: solution tampon (7 points) 2- Préparation d'une solution tampon On mélange 60 mL de la solution (A) NH3 de concentration 0,1 mol/L et 40 mL de |
|
Exercices 2012 - MedShake
1) On mélange 75 mL d'une solution aqueuse de cet acide 10-2 M avec 25 mL d' une solution tampon imposant à la solution finale un pH de 5,00 Quelles sont les |
|
TSTI2D et TSTL Thème : les acides et les bases énoncé Exercice 1
Thème : les acides et les bases Corrigé Exercice 1 : Préparation d'une solution tampon 1 1 Une espèce acide est une espèce capable de céder un ion H+ |
|
Couples acide faible/base faible Solution tampon - Free
Déterminer le pH de la solution tampon ainsi réalisée 5) pH des milieux biologiques Travail à effectuer 1) Etudier livre p 329 à337 2) Exercices corrigés p338 |