pka base faible
|
§ 7 (suite) Titrages acide-base
Nous avons donc une solution d'une base faible et le pH peut être estimé à partir de l'équation approchée : pH = 7 + 1/2 pKa + 1/2 log ( ca· "a / c0 ) – pour ! |
Comment trouver le pKa d'une base faible ?
Le pKa d'un couple acide base est défini par la relation suivante : pKa = - Log (Ka).
Comment savoir si une base est fort ou faible pKa ?
Une base B appartenant à un couple acide-base de pKa supérieur à 14 sera donc totalement transformée en ions OH- : on dit qu'il s'agit alors d'une base forte.
Une base B appartenant à un couple acide-base de pKa positif ne sera que partiellement transformé en ions OH- : on dit qu'il s'agit alors d'une base faible.Quelle est le pKa d'un acide faible ?
On classe les acides faibles en fonction de leur constante d'acidité, c'est-à-dire en fonction de leur capacité à plus ou moins se dissocier en présence d'eau.
On considère qu'un acide est faible lorsque son pKa est supérieur à −1,74 à 25 °C (pKa du cation hydronium H3O+).- Pour interpréter le pKa : Si le pKa est près de zéro, la substance est acide.
Si le pKa est près de 14, la substance est basique.
|
PH et pKa
pH d'une solution de base forte. pH = 14 + log [B]. 8. Calcul de pH. Formule générale pour le pH de solutions d'acide/base faible: [H3O+] = Ka. |
|
Chapitre 1 Acides et bases
L'acide conjugué d'une base faible est un acide faible. Exemples : 1) L'ammoniaque est une base faible dans l'eau (cf. plus haut) le pKa du couple. |
|
§ 7 (suite) Titrages acide-base
Nous avons donc une solution d'une base faible et le pH peut être estimé à partir de l'équation approchée : pH = 7 + 1/2 pKa + 1/2 log ( ca· "a / c0 ). |
|
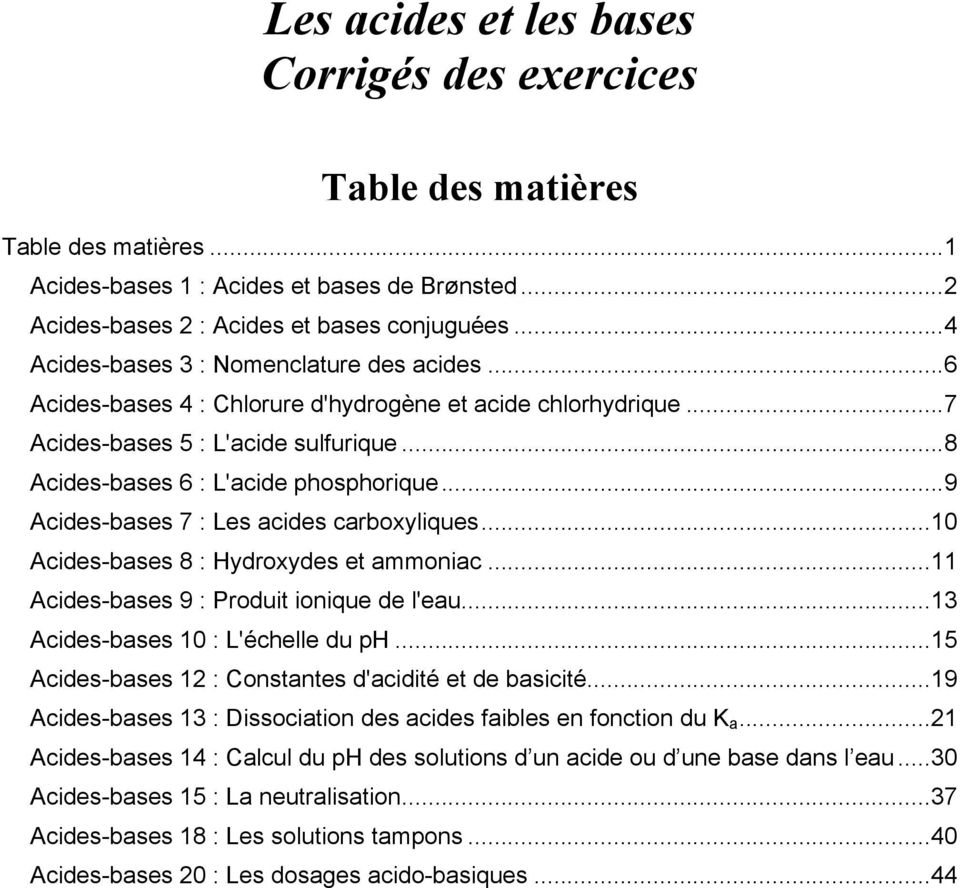
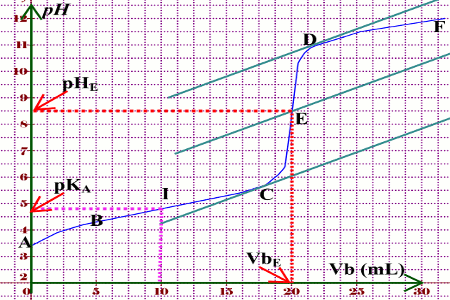
Dosage acide faible – base forte
dosage d'un acide faible (pKa=3 ca=0.01 mol.L-1) par une base forte (cb=0.01 mol.L-1) x = n base versé / n acide initial. |
|
Fiche de synthèse n°2 - Réactions acido-basiques en solution
Lien entre le pH et le pKa d'un couple. Le pH d'une solution contenant un acide faible AH et sa base conjuguée A? est lié au pKa du couple AH/A?par la |
|
Cours de chimie en solution Les acides et les bases
L'acide conjugué d'une base forte est faible et celui d'une base faible est fort. Acide. Base. Fort (e) pKa faible pKb faible. Faible. pKa grand pKb grand. |
|
§ 7 (suite) Calcul du pH de solutions
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pKa ou pKb également suffisamment grand |
|
TD7 + Corrigé (Equilibres Acide-basique) Rappel : • Selon Bronsted
7 + 1/2 (pKa + log Cb) e) Sels : -d'acide fort et de base forte. -d'acide fort et de base faible. -base forte et acide faible. -acide faible et base faible. |
|
Faculté de Médecine / Département de Médecine /1 année de
-14 ==? pKa + pKb = 14. Espèces chimiques. Exemples. pH a) Acide fort b) Acide faibe. HCl. CH3COOH. -logCa. 1/2 (pKa – logCa) c) Base forte d) Base faible. |
|
PH et pKa - The Zysman-Colman Group
Plus la valeur de pKa est faible plus le Ka est grand plus l'acide est fort Formule générale pour le pH de solutions d'acide/base faible: |
|
Chapitre 1 Acides et bases
L'acide conjugué d'une base faible est un acide faible Exemples : 1) L'ammoniaque est une base faible dans l'eau (cf plus haut) le pKa du couple |
|
§ 7 (suite) Calcul du pH de solutions - EPFL
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pKa ou pKb également suffisamment grand |
|
Fiche de révisions sur les acides et les bases - Nicole Cortial
L'hydroxyde de sodium (ou soude) est une base forte : base faible : c'est une base dont la réaction sur l'eau n'est pas totale |
|
BASE FAIBLE *** COUPLE ACIDE-BASE
ACIDE FAIBLE – BASE FAIBLE *** COUPLE ACIDE-BASE 1 Notion d'acide faible 1 1 Expérience : On dissous 01 mol d'acide éthanoïque CH 3COOH dans un volume |
|
VIEtude sommaire des mélanges
éloigné de la base pour que la différence de leurs pKa dépasse 3 2) réaction entre un acide fort et une base faible Un acide fort fournit en solution |
|
Chapitre 8 : Propriétés acide-base
Sel de base faible ( acide faible) et d'acide fort ( base nulle) Le pH est Base faible : ( ) ( ) 1 1 7 log 7 1 92 1 7 46 2 2 pH pKa |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
Titrage d'un acide faible par une base forte Constantes d'acidité et pKa des couples acide/base usuels en solution aqueuse à 25°C |
|
Fiche de synthèse n°2 : réactions acido-basiques en solution aqueuse
Le pH d'une solution contenant un acide faible AH et sa base conjuguée A? est lié au pKa du couple AH/A?par la relation: Cette relation découle de la |
Comment trouver le pKa d'une base faible ?
Le pKa d'un couple acide base est défini par la relation suivante : pKa = - Log (Ka). Le pKa va permettre de déterminer la force d'un acide.Quelle est le pKa d'un acide faible ?
On considère qu'un acide est faible lorsque son pKa est supérieur à ?1,74 à 25 °C (pKa du cation hydronium H3O+). Pour un pKa supérieur à 14, on dit qu'il est indifférent. Un acide est d'autant plus faible que son pKa est élevé. Sa base conjuguée est donc d'autant plus forte et moins stable que ce même pKa est élevé.Comment savoir si une base est fort ou faible pKa ?
Une base B appartenant à un couple acide-base de pKa supérieur à 14 sera donc totalement transformée en ions OH- : on dit qu'il s'agit alors d'une base forte. Une base B appartenant à un couple acide-base de pKa positif ne sera que partiellement transformé en ions OH- : on dit qu'il s'agit alors d'une base faible.- On utilise généralement le Pka plutôt que le Ka pour déterminer la force d'un acide. On remarque que plus l'acide est fort plus le pKa est petit. En effet, si celui est fortement dissocié, la concentration [AH] devient faible.
| PKa Values of Common Bases - University of Windsor |
| About pKa's |
| Functional group pka - Indiana University Bloomington |
| Tables des pKa |
| PKa's of Inorganic and Oxo-Acids Chem 206 |
| Images |
What is an example of a pKa unit?
- Each pKa unit represents a 10-fold difference in acidity or basicity.
. The weaker an acid, the stronger is its conjugate base; the stronger an acid, the weaker is its conjugate base.
. For example, HCl is a very strong acid; it gives up its proton readily; its conjugate base, Cl–, has very little affinity for H+.
What is the pKa of a functional group?
- Approximate pKa chart of the functional groups: values to know 1.
. Protonated carbonyl pKa = ?7 Other important pKa’s 2.
. Protonated alcohol or ether pKa = ?2 to ?3 H2 = 35 3.
. Carboxylic acid pKa = 4?5 4.
. Ammonium ion pKa = 9?10 5.
. Phenol pKa = 10 6.
. Thiol pKa = 10 7.
. Alcohol pKa = 16?18 8.
. Water pKa = 15.7 9.
What is stable at a pH above or below pKa?
- At a pH above the pKa of an acid, the conjugate base will predominate and at a pH below the pKa the conjugate acid will predominate.
. At a pH well above the pKa, we say only the conjugate base is stable.
. At a pH well below the pKa, we say only the conjugate acid is stable.
What is the pKa of acetic acid?
- Weak acids have large pKa's (2 — 50); they are stable because they have high affinity for their protons and want to stay bound to them.
. The pKa of acetic acid is 4.76.
. Acetic acid is a moderately weak acid; it dissociates partly when dissolved in water.
. Each pKa unit represents a 10-fold difference in acidity or basicity.
|
PH et pKa - Eli Zysman-Colman
pKa = -log Ka Plus la valeur de pKa est faible, plus le Ka est grand, plus l'acide est fort Formule générale pour le pH de solutions d'acide/base faible: [H3O+] |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKb > 0 ssi pKa < pKe Dans le cas d'une base forte, totalement dissociée dans l'eau, la concentration |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
Titrage d'un acide faible par une base forte CHAPITRE III Constantes d'acidité et pKa des couples acide/base usuels, en solution aqueuse, à 25°C Acide |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
CLASSEMENT DES ACIDES ET DES BASES SUR UNE ECHELLE DE PKA 11 4 Une base forte est la base d'un couple tel que pKA > 14 L'acide conjugué |
|
Les acides et bases en solution aqueuse - Groupe Transition
Echelle et table des constantes d'acidité Ka (pKa) 4 5 Coefficient d'ionisation ( de dissociation) d'un acide ou d'une base faible Pourcentage d'ionisation (de |
|
Force des acides et des bases - Lycée dAdultes
4 1 1 Constante d'acidité d'un couple acide-base 4 1 3 Relation entre le pH et le pKa 4 3 1 Acide fort ou faible - Base forte ou faible |
|
§ 7 (suite) Calcul du pH de solutions - EPFL
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pKa ou pKb également suffisamment grand, |
|
Révisions sur les acides et les bases - Nicole Cortial
base faible : c'est une base dont la réaction sur l'eau n'est pas totale pKA H3O + H2 O H2 O OH - KA Bases de plus en plus fortes Acides de plus en |