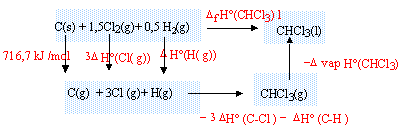
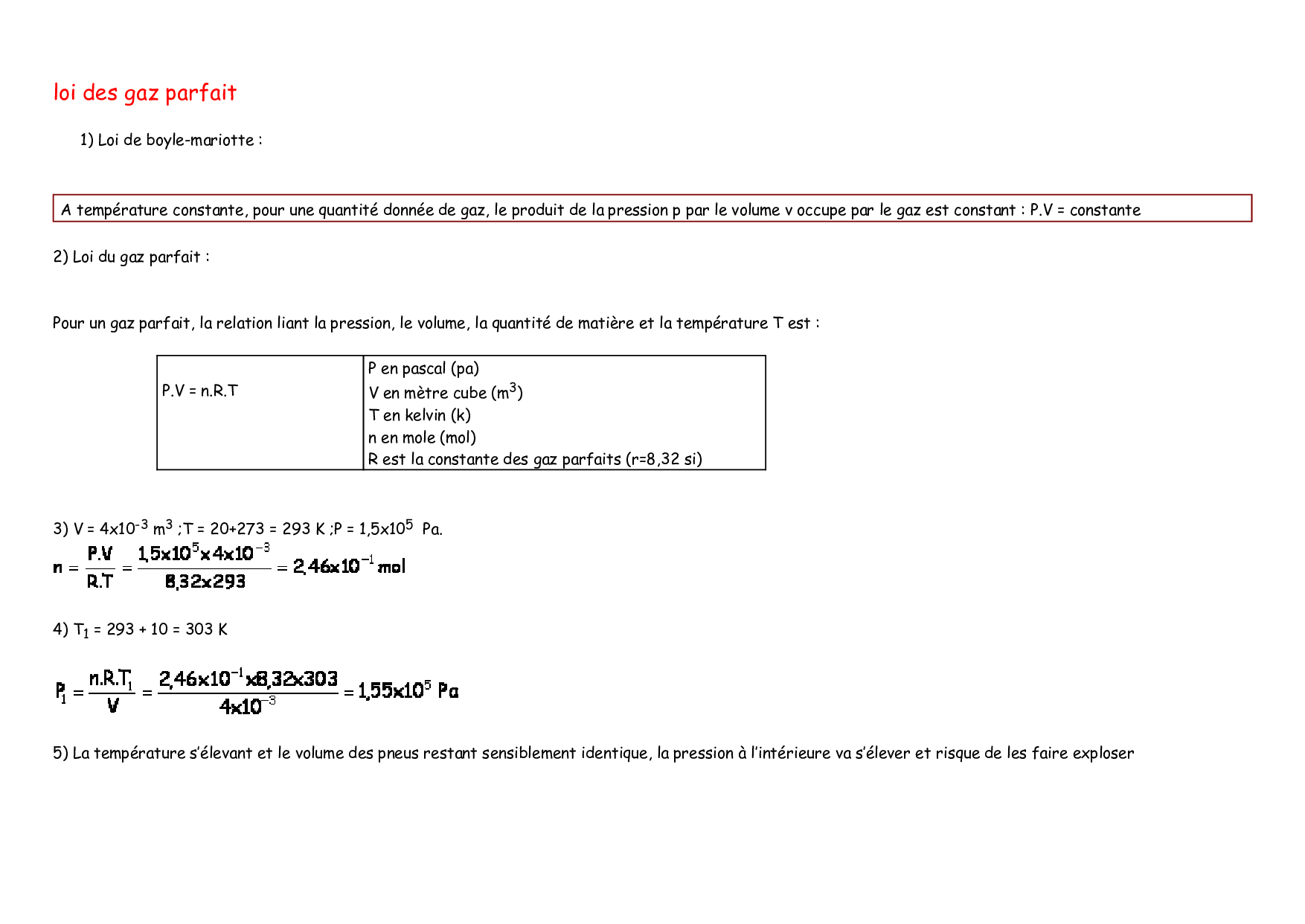
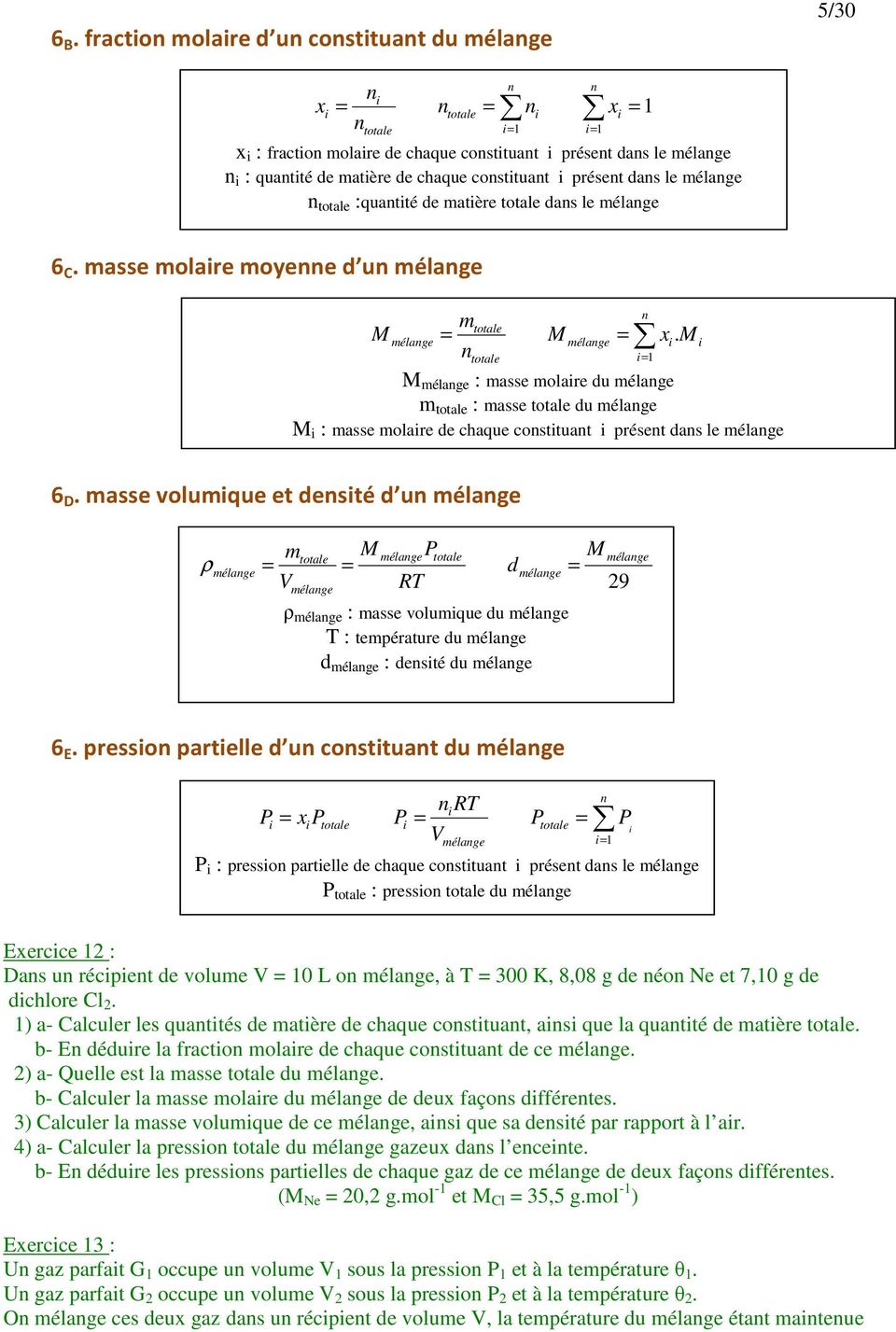
exercices sur les lois des gaz parfaits
|
Série de TD n°01 Thermodynamique
Exercice 2 1 Citer les lois des gaz parfaits 2 Un cylindre contient 765 mL de gaz de propane à la pression de 125·105 Pa Quel serait le volume occupé |
Le volume molaire d'un gaz est la mesure du volume d'une mole de gaz.
Nous pouvons utiliser l'équation volume = moles \\times volume molaire pour calculer les moles et le volume en utilisant le volume molaire d'un gaz à température et pression ambiantes.
Comment calculer la quantité de chaleur d'un gaz parfait ?
V2 V- −PdV = / V2 V- (−nRT/V ) · dV = nRT ln(V1/V2).
La température ne variant pas, l'énergie interne reste constante : dU = δW + δQ = 0.
La chaleur reçue est donc Q = −W.
|
La loi des gaz parfaits
Loi des gaz. Exercices. AdM. 1. La loi des gaz parfaits. 1. a) A la surface de Vénusla pression atmosphérique est de 75 atm. Transformer cette pression. |
|
«EXERCICES ET PROBLEMES CORRIGES DE
Exercices et problèmes corrigés de thermodynamique chimique. 11. CHAPITRE I. LOI DES GAZ PARFAITS ET LE PREMIER. PRINCIPE DE LA THERMODYNAMIQUE |
|
EXERCICES DE CHIMIE GÉNÉRALE
Exercice 2. Un pneu (volume constant rempli d'un gaz parfait) est chauffé jusqu'à ce que la pression à Utiliser la loi du gaz parfait. Exercice 4. |
|
Exercices de Thermodynamique
Rép : 1) UH2O(g) ne vérifie pas la première loi de Joule : H2O(g) ne se comporte pas comme un gaz parfait. Modélisation de VdW : a = 923.10?1 J.m?3.mol?1 et |
|
Série de TD n°01 Thermodynamique
Exercice 2. 1. Citer les lois des gaz parfaits. 2. Un cylindre contient 765 mL de gaz de propane à la pression de 125·105 Pa. Quel serait le. |
|
Chapitre 13 : Les gaz parfaits
Loi des gaz parfaits : P×V = n×R×T. 3) Exercices d'application : a. Un récipient de 200 L contient 1 |
|
RESUME EXERCICES LOI DAMONTONS OBJECTIF
La validité de la loi d'Amontons pour les gaz parfaits est démontrée à l'exemple de l'air. Pour cela à l'aide d'un bain d'eau |
|
Santé
Chapitre 4 • Le gaz parfait. L'équation d'état des gaz parfaits résume l'ensemble des propriétés des gaz connues sous le nom de : • Loi de Boyle-Mariotte |
|
Terminale générale - Gaz parfaits et thermodynamique - Exercices
la loi : a. Q= T2?T1 mc b. Q= mc. T2?T1 c. Q=mc(T2?T1) d. Q=mc(T1?T2). Exercice 2 corrigé disponible. Exercice 3 corrigé disponible. 1/7. Gaz parfaits |
|
MECANIQUE DES FLUIDES. Cours et exercices corrigés
La dernière partie de chaque chapitre est consacrée à des exercices corrigés. 2 Equations d'etat d'un gaz parfait . ... Lois des gaz parfaits . |
|
EXERCICES DE CHIMIE GÉNÉRALE
Exercice 2 Un pneu (volume constant, rempli d'un gaz parfait) est chauffé jusqu'à ce que la pression à l'intérieur du pneu soit 2 2 Utiliser la loi du gaz parfait |
|
Les gaz parfaits - Physagreg
Loi des gaz parfaits : P×V = n×R×T 3) Exercices d'application : a Un récipient de 20,0 L contient 1,7 mol de gaz On désire que la pression du gaz soit égale à |
|
La loi des gaz parfaits
Loi des gaz Exercices AdM 1 La loi des gaz parfaits 1 a) A la surface de Vénus,la pression atmosphérique est de 75 atm Transformer cette pression en torrs |
|
CINFORMELLE_exercice13 - Exercices : corrigé
Le diazote est le seul gaz, c'est un gaz parfait alors à t : « pV= nRT » s'écrit pV= ξRT Ainsi si la température et la pression sont constantes, le volume V est bien |
|
Exercices PP349-357
Exercices 7 5 min chrono Si vous ne trouvez pas la bonne réponse, reportez- vous auß Utiliser la loi du gaz parfait et les unités Si dans le calcul |
|
EXERCICES SUR LES LOIS DES GAZ Pour chacun des problèmes
EXERCICES SUR LES LOIS DES GAZ lois des chiffres significatifs volume doit-on ramener ce gaz pour diminuer la pression jusqu'à 127,0 kPa? 2 |
|
Gaz parfait
2) Valeur du volume molaire 3) Exercice Déterminer le volume molaire des gaz si la pression est de 1013 hPa et la température 20,0 °C V) LOI DE MARIOTTE |
|
La loi des gaz parfaits - Physicus
Le Sport – Chapitre 9 – La loi des gaz parfaits Un gaz contenant n (en mol) moles de molécules, à la pression p (en pascal), occupant un Exercice 10 p 300 |
|
Quest-ce quun gaz parfait - Dunod
Mélange de gaz parfaits – Loi de Dalton (1801) Exercices Le récipient (1) contient du diazote à la pression P1 = 1,5 bar et à la température u1 = 15 ◦ |